рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Производство
- /
- Искусственные продукты питания
Реферат Курсовая Конспект
Искусственные продукты питания
Искусственные продукты питания - раздел Производство, ...

УДК 541.182.637.52.664
Искусственные продукты питания. Новый путь получения пищи и его перспективы. Научные основы производства. Толстогузов В. Б. М., «Наука», 1978, 232 с.
Монография представляет собой первую попытку обобщения и систематизации литературных данных и собственных результатов автора в области разработки искусственных продуктов питания. В пен впервые рассмотрены научные и научно-технические основы переработки белка в искусственные продукты питания. Книга содержит описание способов получения различных форм искусственной пищи и анализ существа научных проблем новой области производства.
Книга предназначена для научных и инженерно-технических сотрудников, аспирантов, преподавателей и студентов старших курсов, работающих в областихимии, физической химии, биологии, полимерной и пищевой технологии и ряда смежных областей пауки.
Таблиц 51. Иллюстраций 35. Библ. 818 назв.
Ответственный редактор академик А. Н. НЕСМЕЯНОВ
20504-200
-169-78 Издательство «Наука», 1978 i.
055(02)-78
ПРЕДИСЛОВИЕ
В настоящее время можно считать общепризнанным, что мировое производство продуктов питания не является достаточным для удовлетворения биологических потребностей населения нашей планеты ч прежде всего потребностей в белках и калориях. Современное состояние мировой продовольственной проблемы характеризуется, однако, не только недостаточным по объему производством продовольствия, но также чрезвычайно неравномерным распределением производства и потребления пищи между различными районами мира, странами и группами населения. Более 60% человечества питается неудовлетворительно, не получая, в частности, достаточного количества белка. От голода и неполноценного питания прежде всего страдает население развивающихся стран Азии, Африки и Латинской Америки.
Проблема недостаточного и неполноценного питания — это в первую очередь проблема социально-экономическая и политическая. Неблагоприятные социально-экономические условия для ее решения в развивающихся странах созданы колониализмом и навязываются неоколониализмом. Наследие колониальной системы хозяйствования, а именно общая экономическая отсталость, отсутствие развитой индустрии, финансовых средств, слабая технологическая и транспортная база, обычно монокультурный характер сельского хозяйства, очень малое число специалистов и низкая культура населения, препятствует использованию достижений современной науки и техники в этих странах для производства пищи и ликвидации голода и недоедания. С другой стороны, при капиталистической форме хозяйствования в ряде развивающихся стран использование новых методов ведения сельского хозяйства (например, использование методов и средств «зеленой революции») приводит к углублению неравенства в распределении доходов, быстрому разорению мелких хозяйств, снижению занятости в этих странах с преимущественно сельским населением, обнищанию населения и снижению платежеспособного спроса на пищу. Поэтому выгоды от внедрения новой технологии получают не все группы населения.
В промышлепно развитых капиталистических странах существуют значительные группы населения, питающиеся неудовлетворительно вследствие недостаточного платежеспособного спроса на пищу, в то время как эти развитые страны являются основными экспортерами продовольствия. Кроме того, правительства этих стран в целях стимулирования экспорта и поддержания цен регулярно затрачивают значительные средства на уничтожение продуктов питания и выплачивают премии за невозделывание земли.
Предисловие
Напротив, в социалистических странах голод полностью отсутствует, а уровень питания населения непрерывно повышается. Стремление социалистических стран поставить на службу народу безграничные возможности науки и техники, использовать их для перевооружения сельского хозяйства имеет целью повысить благосостояние населения. В нашей стране первостепенное значение придается поэтому совершенствованию аграрной политики и осуществлению огромного комплекса мероприятий, обеспечивающих повышение эффективности производства продовольствия.
Общий мировой дефицит продовольствия, особенно острый в развивающихся странах, есть, следовательно, в первую очередь, результат капитализма и колониализма. Высокие же темпы роста населения в развивающихся странах не являются первопричиной обострения мировой продовольственной проблемы. Они, однако, осложняют решение этой проблемы, требуя принятия срочных и эффективных мер.
Эффективность решения этой по существу социально-экономической и политической проблемы в значительной мере определяется возможностью широкого применения достижений современной науки и техники в интересах общества. Необходимый темп расширения объема производства пищи может быть достигнут при наличии благоприятных социально-политических условий, за счет одновременного использования как традиционных, так и качественно новых методов производства пищи. Необходимые для этого предпосылки создаются в ходе современной научно-технической революции.
Традиционные пути решения проблемы питания связаны с повышением продуктивности земледелия, животноводства, птицеводства, рыболовства, а также со снижением потерь при производстве и хранении пищевого сырья и продуктов питания. Однако недостаточно высокая эффективность традиционных способов производства пищи приводит к ситуации, парадоксальной в условиях острого дефицита белка: наличию значительных потенциальных ресурсов пищевого белка, не используемого совершенно или используемого крайне нерационально. Это прежде всего относится к белкам масличных, бобовых и зерновых культур, белкам обрата молока, дрожжей, других одноклеточных организмов, белкам зеленых листьев и зеленой массы растений, белкам малоценных пород рыбы, других морепродуктов и т. д.
Основная причина, затрудняющая широкое применение белков для питания, состоит в их низкой привлекательности для потребителя. Белки, будучи высокомолекулярными соединениями, лишены запаха, вкуса и обычно бесцветны. Поэтому практически невозможно широко использовать изолированные белки для питания в видесухих порошков, растворов или паст. Применение белков в качестве добавок к традиционным пищевым продуктам
Предисловие
ограничено, в частности, тем, что добавление значительных количеств белка обычно приводит к искажению уникальной структуры обогащаемого продукта, ухудшая его вкусовые и потребительские качества. Отсюда возникла задача разработки приемов получения пищи на основе белков различного происхождения, задача, которая не может быть эффективно решена традиционными методами.
В последние несколько лет в процессе научно-технической революции возникло и быстро приобрело большое значение качественно повое направление в производстве пищи. Оно заключается и получении искусственных продуктов питания и характеризуется использованием промышленных методов переработки белка. Оспоипая задача производства искусственных продуктов питания состоит в том, чтобы белок сделать привлекательной пищей и, таким образом, обеспечить его широкое потребление. Иначе говоря, существо нового направления в производстве пищи состоит в переработке белков и других пищевых веществ в недорогие, полноценные и привлекательные для человека продукты питания. Это направление производства получило быстрое развитие в про-мышленио развитых странах и в настоящее время складывается в новую крупнотоннажную отрасль промышленности.
Хотя практическое освоение производства искусственных продуктов питания началось сравнительно недавно, полученные результаты однозначно свидетельствуют о чрезвычайной перспективности нового направления в плане резкого расширения объема производства белковой пищи. Уже на начальном этапе развития производства искусственной пищи, т. е. в ближайший период времени, появится возможность добиться резкого увеличения эффективности сельскохозяйственного производства, прежде всего за счет комплексной переработки сельскохозяйственного сырья и получения искусственных продуктов питания, например, на основе растительных белков, белковых отходов сельскохозяйственного производства и пищевой промышленности. Речь, следовательно, не идет о замене сельскохозяйственного производства, а напротив,— о более полной, более рациональной и экономически эффективной переработке его продукции, прежде всего белковой. В более отдаленной перспективе, на втором этапе, когда производство искусственных продуктов питания станет сопоставимо по объему с традиционным производством пищи, возможно существенное изменение соотношений между отдельными видами традиционных производств и сокращение ряда его отраслей. Расширение земледелия позволит, в частности, увеличить производство растительного белка и его прямую переработку п искусственные продукты питания, имитирующие мясные и молочные изделия. На этом этапе традиционные и искусственные продукты питания, очевидно, будут успешно дополнять друг друга в рационе
Предисловие
питания человечества и будут способны обеспечить питание во много крат большего населения планеты. И на этом этапе не возникает, следовательно, вопроса о замене традиционного производства на производство искусственной пищи. Оба эти направления будут еще более тесно связаны. Наконец, на третьем этапе развитие индустрии искусственной пищи на базе белков и других пищевых веществ, получаемых микробиологическими методами, откроет принципиальную возможность производства пищи несельскохозяйственным путем.
Идеи о принципиально неограниченных возможностях получения пищи промышленными методами и своевременности практических работ в этом направлении были сформулированы в 1961 г. академиком Л. Н. Несмеяновым. В результате этого в Институте элементоорганических соединений ЛН СССР под руководством А. Н. Несмеянова были впервые развернуты комплексные исследования по проблеме искусственной нищи, начата разработка научных основ новой области производства и убедительно показаны ее перспективы.
Основные вопросы, решаемые новой областью крупнотоннажного производства, сводятся к резкому увеличению масштабов и удешевлению производства пищи, обеспечению требуемого количественного и качественного уровня белкового питания, организации детского, лечебного и профилактического питания, а также питания в новых и необычных условиях, возникающих в ходе развития научно-технической революции.
Всесторонняя научная разработка многочисленных сложных проблем, относящихся к получению и переработке пищевых веществ в искусственные продукты питания, начата 10—15 лет назад. При этом научные основы переработки белков различного происхождения в разнообразные формы искусственной пищи впервые начали разрабатываться в нашей стране.
Настоящая книга представляет собой первую попытку обобщения и систематизации многочисленных литературных данных, а также экспериментальных результатов, полученных в Институте элементоорганических соединений АН СССР, в области разработки искусственных продуктов питания. В книге рассмотрены научные и научно-технические проблемы переработки белка в искусственные продукты питания, современное состояние и перспективы развития новой области производства.
Задача данной книги заключается в том, чтобы показать научную проблематику этой новой области и существование научно-технических предпосылок для организации нового направления в производстве пищи, позволяющего резко увеличить ресурсы пищи, повысить качество и экономические показатели ее производства и потребления.
ГЛАВА ПЕРВАЯ
ИСКУССТВЕННЫЕ ПРОДУКТЫ ПИТАНИЯ -НОВОЕ НАПРАВЛЕНИЕ В ПРОИЗВОДСТВЕ ПИЩИ
ТРАДИЦИОННЫЕ ПРОДУКТЫ ПИТАНИЯ
Предполагается, что человек существует па Земле около 2 млн. лет [1, 2]. Долгое время численность населения возрастала приблизительно на 2% за тысячелетие, т. е. на 0,002% в год. С начала нашей эры в течение первых 16 веков темпы роста составляли 0,1% в год, но в последнее время достигли 2%. Скорость роста народонаселения увеличилась, следовательно, на три порядка. Этот беспрецедентный рост населения произошел во второй половинеXX в. и получил название демографического
взрыва [1—8].
К началу нашей эры мировое население составляло около
200 млн. человек. Оно достигло одного миллиарда через 18 веков (1830 г.). Второй миллиард потребовал уже около 100 лет и был достигнут к 1930 г., третий — всего 30 лет (1960 г.). Добавление четвертого миллиарда заняло 15 лет (1976 г.), а пятимиллиардный рубеж, как ожидается, будет пройден уже в 1985—1989 гг. По прогнозам ООН, к концу века мировое населенно увеличится
более чем в 1,5 раза [6, 7].
Демографический взрыв произошел в основном за счет резкого увеличения темпа роста населения развивающихся стран,
где он составляет 2,2—4% в год.
Между тем уже современный уровень питания человечества
крайне неудовлетворителен как в количественном, так и в качественном отношении. Количественный недостаток продуктов питания затрагивает до 15% мирового населения, в основном в развивающихся странах [6—14]. Он связан в первую очередь с дефицитом калорий. Потребность в калориях (покрываемая в основном за счет потребления углеводов и липидов — энергетических компонентов пищи) зависит от характера деятельности человека, возраста, пола, климатических и других условий, и ее средние величины поэтому существенно различаются для населения различных районов мира. При средней потребности в калориях, оцениваемой, согласно принятым нормам питания, 3000 ккал па человека в день, эта величина составляет 2300 ккал для занятого умственным трудом человека при малоподвижном образе жизни, 3000 ккал — при средней физической нагрузке и достигает
10 Глава первая
4000 ккал при тяжелом физическом труде [15, 16]. В развитых странах среднее потребление энергетических компонентов пищи превышает 3000 ккал на человека в день, т. е. в известной степени избыточно, особенно, если учесть расширение сферы интеллектуального труда в этих странах. Возрастающая калорийная избыточность рационов приводит к избыточному весу и ожирению, что способствует развитию ряда заболеваний, приводит к снижению работоспособности и сокращению средней продолжительности жизни. Напротив, развивающиеся страны производят, в пересчете на калории, не более 60% необходимых продуктов [8], и среднее потребление не превышает здесь 2150 ккал на человека в день.
Таким образом, если в развивающихся странах, особенно для наиболее бедных слоев населения, существует проблема острого дефицита калорий, то в развитых странах возникает противоположная задача снижения калорийности питания и разработки рационов и продуктов для терапии веса.
Если борьбе с голодом — количественным недостатком пищи посвящены тысячелетние усилия человечества, занятого преимущественно тяжелым физическим трудом и потому испытывающего повышенную потребность в источнике энергии, то второй аспект — качество пищи, приобрел особое значение в последнее время в условиях научно-технической революции в связи с резко возросшей ролью умственного труда.
Качественный аспект проблемы питания связан с дефицитом полноценного белка в рационе питания. Он затрагивает около Уз населения планеты, преимущественно в развивающихся странах Азии, Африки и Латинской Америки, и ситуация здесь существенно хуже, чем с дефицитом калорий. Качественная сторона проблемы питания в значительной мере обусловлена неполноценное гыо большинства потребляемых растительных белков вииду несбалансированности их состава по содержанию отдельных аминокислот. Из 20 аминокислот, содержащихся в белках, 8—9 аминокислот являются незаменимыми, так как организм должен получать их с ппщей, в то время как остальные он способен синтезировать сам. Незаменимая аминокислота, содержащаяся в белке в минимальном (в сравнении с потребностью) количестве, определяет степень использования организмом других аминокислот, т. е. биологическую ценность белка. Животные белки по аминокислотному составу в большей мере отвечают потребностям организма в незаменимых аминокислотах [15—19]. В этом одна из причин развития животноводства, позволяющего получать более полноценный, животный белок путем скармливания животному растительных белков, в том числе белков, входящих в состав многих растительных продуктов (травы, сена, жмыхов и т. п.), не находящих применения для питания человека.
ИПП — новое направление в производстве пищи11
Таблица 1 Потребление белка в промышленно развитых и развивающихся странах. ФАО ООН…ВОДЯ
|
|
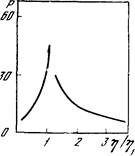
Рис. 6. Зависимость степени асимметрии частиц дисперсной фазы (Р) от соотношения вязкостей дисперсной (т) и дисперсионной (T]i) фаз
Температура 32,5° С; скорость сдвига 3,9 сек-'; объемная доля дисперсной фазы 0,4
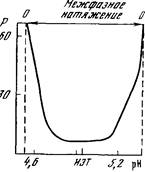
Рис. 7. Зависимость степени асимметрии частиц дисперсной фазы (Р) от рН (межфазного натяжения) системы декстран (8%)—желатина (10%)— вода при 32,5° и скорости сдвига 3,9 сек~1
условиях степень асимметрии частиц возрастает с увеличением их объема.
Процесс получения и поведение индивидуальных жидких цилиндров в жидкой среде при постоянной и переменных темпе-
* Дисперсная фаза систем содержит преимущественно первый из указанных компонентов, например в системе желатина—декстран—вода дисперсная фаза обогащена желатиной, а в обратной системе декстран—желатина—вода желатина содержится преимущественно в дисперсионной среде.
Физико-химические основы переработки белка вИПП 57
ратурах, а также возможность фиксации формы жидкого цилиндра путем перевода в студнеобразное состояние были исследованы на примере системы желатина—поливиниловый спирт—вода. Существо метода [74] состоит в вытягивании с постоянной скоростью одной из жидких фаз (фаза желатины) в виде нити в объем другой жидкой фазы (раствор поливинилового спирта). Стабильность жидкого цилиндра оценивают, измеряя его длину в момент отрыва от капилляра в процессе вытягивания. После отрыва от капилляра жидкий цилиндр сохраняет форму в течение определенного хорошо воспроизводимого времени (время жизни жидкого цилиндра), а затем самопроизвольно распадается на большое число сферических частиц [62, 70].
Исследование поведения жидкого цилиндра в условиях охлаждения системы показало, что перевод фазы желатины в студнеобразное состояние позволяет фиксировать форму жидкого цилиндра при условии, что время перехода в студнеобразное состояние не превышает времени жизни жидкого цилиндра. Это условие выполняется, например, при выливании жидкой двухфазной системы желатина (10%)—поливиниловый спирт (5%)—вода с температурой 28° в виде струи в воду, предварительно охлажденную до 2°. Одновременно с образованием и фиксацией формы жидких цилиндров происходит разбавление водой дисперсионной среды. В результате получают ансамбль тонких (5—10 мкм) студнеобразных волокон желатины [62]. Микрофотография таких волокон приведена на рис. 8.
Результаты исследования закономерностей поведения двухфазных жидких систем при застудневании в потоке [62, 71] позволили представить общую схему переработки таких систем в различные анизотропные материалы (рис. 9). Их морфология определяется преимущественно структурой исходной жидкой ге-терофазной системы в потоке и соотношением скоростей перехода фаз в студнеобразное состояние. Так, для получения тонких волокон целесообразно использовать двухфазные системы с одним студнеобразователем, сосредоточенным преимущественно в дисперсной фазе. Состав фаз должен обеспечивать их близкую вязкость и достаточно высокую скорость перехода дисперсной фазы в студнеобразное состояние. При этом необходимо, чтобы концентрация студнеобразоватсля в дисперсионной среде была ниже критической концентрации студнеобразования. Если же частицы дисперсной фазы деформируются в потоке, но не застуд-невают, а в студнеобразное состояние переходит дисперсионная среда, то возникают студни капиллярной структуры. Это достигается при переработке двухфазных систем со студнеобразователем, сосредоточенным преимущественно в дисперсионной среде системы. Отметим, что анизотропные студни капиллярной структуры могут быть получены но только на основе эмульсий, но

Рис. 8. Микрофотография студнеобразных волокон желатины
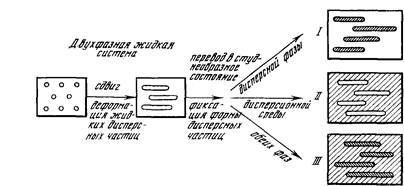
Рис. 9. Общая схема переработки двухфазных жидких систем
I—волокна; 11— студни капиллярной структуры; III— студни, наполненные подокнами
также па основе пен и концентрированных суспензий с пластичными взаимодействующими (непрерывная фаза системы) частицами, так как образованию таких студней благоприятствует высокая вязкость дисперсионной среды, многократно превышающая вязкость дисперсной фазы. Наконец, возможен переход обеих фаз в студнеобразное состояние с образованием студней, наполненных либо армированными волокнами, ориентированными в направлении деформации системы. Это достигается при исполь-
Физико-химические основы переработки белка в ИПП 59
зовании одного студнеобразователя, распределенного в обеих фазах за счет его сорастворимости с другим макромолекулярным компонентом, или же с помощью двух студнеобразователей, сосредоточенных в разных фазах системы и обеспечивающих перевод обеих фаз в студнеобразное состояние в сходных условиях. Несколько более подробно переработка двухфазных жидких систем белок—полисахарид—вода в анизотропные материалы будет рассмотрена в разделе, посвященном анизотропным студням.
Таким образом, установление общего характера явления несовместимости белков и полисахаридов в водных средах, закономерностей деформации двухфазных систем, а также выяснение принципиальной возможности фиксацииих форм при переводе одной или обеих фаз системы в студнеобразное состояние в потоке создают предпосылки для разработки эффективных методов переработки белка в составе многокомпонентных двухфазных систем в искусственные продукты питания анизотропной макроструктуры, прежде всего в искусственные мясопродукты.
ЭЛЕКТРОСТАТИЧЕСКОЕ ВЗАИМОДЕЙСТВИЕ БЕЛКОВ И ПОЛИСАХАРИДОВ В ВОДНЫХ СРЕДАХ
В рамках рассматриваемой проблемы переработки белка исследование электростатического взаимодействия белков и кислых полисахаридов, как отмечено выше, представляется необходимым прежде всего в связи с задачей получения гомогенных стабильных систем, содержащих белки, и регулирования физико-химических свойств таких многокомпонентных жидких систем. Эта задача, в частности, сводится к выяснению условий получения растворимых в водных средах комплексов белков с кислыми поли-сахаридами и возможности направленного регулирования функциональных свойств белков. Другой важный аспект проблемы взаимодействия белков и кислых полисахаридов обусловлен тем, что оба эти вещества представляют собой важнейшие пищевые студнеобразователи. Поэтому условия образования, структура и свойства комплексов в значительной мере определяют условия перевода перерабатываемой многокомпонентной жидкой системы в студнеобразное состояние и свойства студней, в том числе и условия получения комплексных студней (см. следующий раздел). Еще один аспект рассматриваемого взаимодействия связан с проблемой пищевой ценности искусственных продуктов питания, поскольку атакуемость компонентов продукта пищеварительными ферментами может зависеть не только от его состава, но и от физической структуры. Образование электростатических комплексов белка с полиэлектролитами (кислые полисахариды, нуклеиновые кислоты), по-видимому, может сопровождаться изменением конформации белка и его атакуемости ферментами. Кроме того,
60 Глава вторая
учитывая возможность взаимодействия полиэлектролитных компонентов продукта с белками — ферментами желудочно-кишечно-го тракта, что может сопровождаться изменением их активности, возникает необходимость исследования свойств белков (в том числе и ферментов) в комплексах с полиэлектролитами.
Таким образом, в связи с проблемой получения искусственных продуктов питания важное значение приобретают вопросы изучения условий образования, состава, структуры и свойств электростатических комплексов белков с кислыми полисахаридами и другими полиэлектролитами, а также свойств белка в таких комплексах.
Если термодинамическая совместимость белков и полисаха-ридов до последнего времени оставалась практически неизученной и исследуется в течение последних лет, прежде всего в связи с проблемой искусственной пищи, то в области электростатического взаимодействия этих макромолекулярных веществ выполнены многочисленные исследования как физико-химического, так и биохимического характера. К тому же электростатическое взаимодействие белков и полисахаридов — лишь частный случай явления взаимодействия противоположно заряженных макромолекул в растворах, рассмотренного в ряде обзоров и монографий [30, 31, 33].
Явление фазового расслоения в смесях противоположно заряженных белков и кислых полисахаридов, названное позднее комплексной коацервацией, было впервые обнаружено еще в конце прошлого века. По-видимому, впервые это явление наблюдали Паули и Рон [75], а также Тьюбакс [76] при смешении растворов желатины и гуммиарабика в присутствии уксусной кислоты. Позднее Спиро [77] наблюдал фазовое расслоение в смесях подкисленных растворов желатины и гуммиарабика. Систематически это явление было исследовано Бунгенберг де Йонгом и его школой [35, 36, 78, 79]. Широкие исследования явления комплексной коацервации были проведены в связи с предложенной А. И. Опариным разработкой теории возникновения и начального развития жизни [80—83]. Теоретическое и экспериментальное исследование природы явления комплексной коацервации было выполнено Овербиком и Борном [84, 85], а также Вайсом с сотр. [86—89].
В противоположность явлению несовместимости белков и полисахаридов (см. предыдущий раздел), при котором макромо-лекулярные компоненты сосредоточиваются в разных фазах, явление комплексной коацервации при смешении растворов белков с растворами противоположно заряженных кислых полисахаридов приводит к их концентрированию в одной из фаз комплексного коацервата (концентрированная фаза), в то время как другая фаза представляет собой их разбавленный раствор (рав-
Физико-химические основы переработки белкав ИПП
новесная жидкость). В зависимости от условий смешения и природы макромолекулярных компонентов образующаяся концентрированная фаза представляет собой вязкую жидкость (комплексный коацерват по Бунгенберг де Йонгу; см. примечание на стр. 44) или же студнеобразный осадок. Причины, приводящие в одном случае к образованию осадка студнеобразных частиц, а в другом — вязкой жидкости, окончательно не выяснены. Майкле полагал, что агрегатное состояние и морфология концентрированной фазы определяются в основном плотностью зарядов взаимодействующих макроионов [90]. Однако это не единственная причина, так как известно влияние на агрегатное состояние концентрированной фазы других факторов, например, концентрации макромолекулярных компонентов и температуры
[82, 91].
Количество (по весу или объему) концентрированной фазы,
образующейся при данном значении рН системы, зависит от соотношения макромолекулярных компонентов в исходной смеси. Соотношение концентраций, при котором наблюдается максимальный выход концентрированной фазы, называют эквивалентным [78, 86]. Для систем, содержащих в качестве белкового компонента гибкий макроион желатины, эквивалентное соотношение макромолекулярных компонентов отвечает равенству суммарного положительного заряда макроионов желатины и суммарного заряда полианионов кислого полисахарида [92—96]. Для систем глобулярный белок—кислый полисахарид подобного соответствия не наблюдается [86]. При отклонении состава смеси от эквивалентного концентрированная фаза обогащается растворителем.
Температура системы оказывает существенное влияние на фазовое расслоение [82, 97]. Повышение температуры приводит к сближению составов концентрированной фазы и равновесной жидкости, и по достижении некоторой температуры система может стать однофазной. Например, концентрированная фаза, образующаяся при смешении растворов желатины и гуммиарабика при рН 3,5, полностью растворяется при температуре около 60° [82]. Верхняя критическая температура смешения для системы бычий фибриноген—декстрансульфат составляет 48° [98].
Введение солей, т. е. увеличение ионной силы системы, приводит к подавлению фазового расслоения [79, 86]. По мере увеличения концентрации соли количество концентрированной фазы и ее концентрация снижаются. Критическая концентрация соли, т. е. концентрация, необходимая для полного подавления фазового расслоения, обычно не превышает 0,5—1,0 М и зависит от вида соли в соответствии с правилом Шульца—Гарди [99]. В случае, если соль содержит ионы, специфически связываемые одним из макромолекулярных компонентов, наблюдается изменение состава концентрированной фазы [82, 100].
| Глава вторая |
Белки и кислые полисахариды в определенных условиях образуют комплексы, растворимые в водных средах [101—107 ]. Растворимые комплексы обычно регистрируют по возникновению нового пика на электрофореграмме [102—104, 106] или седимен-тограмме [104] системы. Установлено, что растворимые комплексы образуются при соотношениях макроионов, сильно отличающихся от эквивалентного, иих состав зависит от состава исходной смеси. Обычно при концентрации хлористого натрия до 0,2—1,0 М растворимые комплексы разрушаются.
Конформация белка и кислого полисахарида оказывает существенное влияние как на фазовое расслоение, так и на образование растворимых комплексов. В работе [107] показано, что электростатическое взаимодействие гепарина и конканавалина А подавляется при изменении нативной конформации белка. Авторы связывают это явление с изменением расположения ионогеп-ных групп белка при изменении его конформации. Роль расположения ионогенных групп взаимодействующих макроионов иллюстрируют также данные Андерсона [105].
Взаимодействие белков и кислых полисахаридов не только зависит от конформации макроионов, но, в свою очередь, по-видимому, способно вызывать их конформационные изменения [101].
Анализ факторов, приводящих к расслоению смесей слабых противоположно заряженных полиэлектролитов, наиболее подробно выполнен для двух систем: желатина — гуммиарабик и кислотная желатина — щелочная желатина. Отметим, что обе предложенные в связи с этим теории развиты лишь для случая полиионов с конформацией статистического клубка [84—89].
Согласно теории Вайса [86—89], первой стадией комплексной коацервации является образование электронейтрального комплекса в результате электростатического взаимодействия между противоположно заряженными полиионами по следующей схеме:
Р+ОН- + H+Q- -> PQ + НаО,
где Р4' и Q~ — соответственно поликатион и полианион. Движущей силой процесса является уменьшение свободной электростатической энергии. При этом рассматриваются две модели электронейтрального комплекса PQ. Первая отвечает совпадению центров тяжести полиионов, вторая — образованию ионных пар между противоположно заряженными функциональными группами взаимодействующих макромолекул, причем предполагается, что образование ионных пар предпочтительнее, так как обеспечивает наибольший выигрыш электростатической энергии при комплексообразовании.
Вторая стадия процесса комплексной коацервации заключается в агрегации электронейтральных комплексов с образованием новой фазы, т. е. концентрированной фазы комплексного коацер-
Физико-химические основы переработки белка в ИПП
вата. Согласно Вайсу, фазовый переход обусловлен, с одной стороны, ухудшением качества растворителя в процессе комплексо-образования, а с другой — выигрышем энтропии за счет хаотиза-ции распределения компонентов комплекса в концентрированной фазе. Теория Вайса хорошо описывает явление комплексной коацервации гибких полиионов. В частности, она показывает, что состав комплексного коацервата определяется составом электронейтрального комплекса и потому не зависит от состава исходной смеси. Иными словами, эквивалентное соотношение макроионов в процессе комплексной коацервации определяется требованием взаимной компенсации их зарядов. Кроме того, предположение об участии на второй стадии процесса — агрегации электронейтральных комплексов, сил иной природы, чем электростатические, позволяет объяснить в рамках этой теории влияние температуры на комплексную коацервацию.
Детальный анализ взаимодействия глобулярных белков и кислых полисахаридов не проводился. Некоторые авторы считают, что связь между компонентами комплекса осуществляется за счет ионных пар между противоположно заряженными функциональными группами [105, 107 ]. Для глобулярных белков известна способность к образованию растворимых комплексов. В определенных условиях возможно образование нерастворимых комплексов, осаждающихся из раствора в виде концентрированной
фазы — комплексного коацервата.
Изучение механизма электростатического взаимодействия в основном, следовательно, ограничено рассмотрением фазового расслоения систем в результате образования нерастворимых комплексов. Теория этого явления развита для взаимодействия гибких противоположно заряженных полиионов. Образование растворимых комплексов установлено при этом лишь для глобулярных белков, а существование таких комплексов для белков с неупорядоченной конформацией, например для желатины, до недавнего времени не было известно. В то же время образование растворимых комплексов желатины с кислыми полисахаридами, очевидно, может привести к получению новых студнеобразующих систем, что существенно с точки зрения рассматриваемой проблемы. Хотя в ряде работ [109—117] показано изменение свойств белка в результате взаимодействия с полиэлектролитами, в том числе и изменение ферментативной активности под влиянием полианионов, природа этих эффектов оставалась неисследованной
[118].
Необходимо также отметить, что большинство работ по взаимодействию белков и кислых полисахаридов выполнено на водорастворимых белках — альбуминах (по этому признаку к альбуминам может быть формально отнесена и желатина), в то время как глобулины и глютелины оставались вне поля зрения. Вместе
| Глава вторая |
с тем к последним, как отмечено выше, относятся основные виды белков, перерабатываемых в искусственные продукты питания.
Таким образом, несмотря на большое число работ, посвященных взаимодействию белков и кислых полисахаридов в водных средах, ряд аспектов, имеющих важное практическое значение в плане проблемы получения искусственных продуктов, требовал дополнительного изучения [1, 2, 118, 119]. В последние годы были предприняты исследования в указанных направлениях с привлечением широкого круга белков (в том числе и ферментов) и полисахаридов с различными молекулярными и физико-химическими характеристиками [118—131 ], а также разработан ряд методических вопросов исследования стехиометрии нерастворимого комплекса и свойств белка в растворимых и нерастворимых комплексах [10, 18, 118, 119, 125, 126, 130].
Было показано, что в кислой области рН относительно ИЭТ белка, в определенной области составов системы (вблизи эквивалентного) взаимодействие белка (альбумина) и кислых полисахаридов приводит к расслоению системы на концентрированную фазу и равновесную жидкость. Если при этом суммарная концентрация макромолекулярных компонентов превышает Ю"20/), то концентрированная фаза выделяется в виде крупных дисперсных частиц, легко коалесцирующих с образованием макрослоя комплексного коацервата. При более низкой суммарной концентрации белка и кислого полисахарида (Ю-2—Ю"30/)) концентрированная фаза выделяется в высокодисперсном состоянии. Размер частиц, определенный методом спектра мутности, составляет 0,5— 1,2 мкм. Оптическая плотность системы при постоянном рН линейно зависит от суммарной концентрации макромолекулярных компонентов вплоть до 7•i0~зo/o. Поэтому при фазовом расслоении в разбавленных системах их оптическая плотность может служить мерой концентрации частиц концентрированной фазы, т. е. использоваться для определения выхода нерастворимого комплекса. Принимая величину оптической плотности в качестве критерия выхода нерастворимого комплекса и рассматривая процесс взаимодействия белка и кислых полисахаридов как моноядерную ассоциацию, оказалось возможным использовать для определения стехиометрии нерастворимого комплекса метод непрерывных изменений при пефелометрических исследованиях. Данные о составе нерастворимого комплекса, полученные химическим анализом состава концентрированной фазы, совпадают с результатами определения его стехиометрии нсфелометрическим методом [10,119].
Установлено, что концентрированная фаза комплексного коацервата содержит основное количество белка (альбумина) и кислого полисахарида в постоянном соотношении, не зависящем от состава системы до расслоения. Отношение концентраций макромолекулярных компонентов в концентрированной фазе (т. е. в
Физико-химические основы переработки белкав ИПП 65
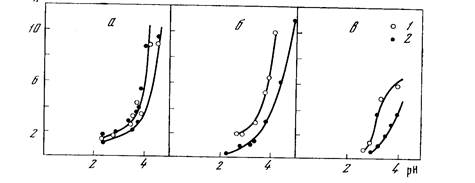
Рис. 10. Зависимость состава (га — соотношение весовых концентраций белка и альгината) нерастворимых комплексов от рН системы
а — желатина— апьгинат—вода (.?), эдестин—альгинат—вода (2); б—бычий сывороточный альбумин (БСА)—альгинат—вода; в—лизоцим—альгинат—вода: 1—экспериментальные данные; 2 — рассчитанные для условий электронейтральности комплекса
нерастворимом комплексе) зависит от рН, причем понижение рН системы сопровождается уменьшением доли белка в комплексе. Для проверки предположения о электронейтральности нерастворимого комплекса его состав рассчитывали исходя из условия равенства суммы зарядов макроионов белка и кислого полисаха-Рида в системе. Результаты расчета состава нерастворимых комплексов, получаемых при различных значениях рН, выполненные на основе предположения о его электронейтральности, совпадают с экспериментальными данными лишь в случае белков с неупорядоченной конформацией, а именно, желатины и эдестина, денатурированного кислотой (рис. 10). Для глобулярных белков (альбуминов) — лизоцима и сывороточного альбумина — подобного совпадения не наблюдается (см. рис. 10). Иными словами, если белок имеет неупорядоченную конформацию, то нерастворимый комплекс электронейтрален. В случае же глобулярных белков нерастворимый комплекс заряжен и содержит относительный избыток белка. Последнее, по-видимому, обусловлено стабильностью компактной пространственной структуры белка, вследствие чего часть положительно заряженных групп белка не может образовывать ионные пары с карбоксильными группами жесткоцепного кислого полисахарида, например альгината, по чисто стерическим причинам. При введении в систему 0,2—0,5 М хлористого натрия фазовое расслоение подавляется [121].
Исследование взаимодействия желатины и альгината натрия показало, что вне области, отвечающей фазовому расслоению, т. е. при язбытке кислого полисахарида и рН ниже ИЭТ белка,
3 В. Б. Толстогузов
| Глава вторая |
образуются растворимые комплексы желатина—альгинат, которые, по данным свободного электрофореза, являются полианионами. Введение в систему, содержащую растворимые комплексы, хлористого натрия приводит сначала к ее расслоению (при концентрации соли около 0,05Af) с образованием концентрированной фазы, что сопровождается увеличением рассеяния света, затем к снижению рассеяния за счет агрегации частиц концентрированной фазы и, наконец, к растворению концентрированной фазы (при концентрации соли около 0,2 М) и переходу системы в однофазное состояние. Концентрация соли, необходимая для расслоения, может служить мерой заряда анионных комплексов. Она снижается при увеличении доли желатины в системе. Анализ состава концентрированной фазы, полученной при введении соли в систему, содержащую растворимые комплексы, подтверждает, что состав анионных комплексов зависит от состава исходной системы. По мере увеличения доли желатины в системе заряд анионных комплексов стремится к нулю, а их состав — к составу нерастворимого электронейтрального комплекса [122]. Показано, что мочевина при концентрации 6М и выше может подавлять фазовое расслоение в системе желатина—альгинат— вода, но не разрушает при этом электростатические комплексы. Иначе говоря, мочевина препятствует агрегации комплексов и образованию концентрированной фазы. Напротив, хлористый натрий при концентрации 0,2 М и выше подавляет образование как растворимых, так и нерастворимых комплексов.
Полученные данные согласуются с двухстадийной схемой процесса комплексной коацервации, предложенной Вайсом [86— 89], и показывают ее применимость к системе белок—кислый полисахарид, т. е. не только к случаю двух гибких полиионов.
Процесс образования нерастворимого электронейтрального комплекса можно представить как серию последовательных реакций связывания макроионом кислого полисахарида (ядро комплекса) макроионов белка (лиганды) с образованием макро-анионных комплексов, отрицательный заряд которых снижается при присоединении очередного лиганда на величину суммарного заряда макроиона желатины. Процесс завершается образованием электронейтрального комплекса, в котором противоположно заряженные группы белка и кислого полисахарида связаны в ионные пары. Вторая стадия процесса заключается в агрегации электронейтральных комплексов с их выделением в отдельную концентрированную фазу. Агрегация комплексов осуществляется, по-видимому, за счет их гидрофобного взаимодействия и образования водородных связей. Для глобулярных белков характерно то, что нерастворимый комплекс не элсктронойтралеп. Отсутствие эквивалентности можно объяснить исходя из представления
Физико-химические основы переработки белкав ИПП 07
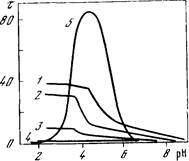
|
Рис. 11. Влияние декстран-сульфата на осаждение казеина. Зависимость мутности (т) от рН системы казеин (3-10~2 %) —декстрансульфат— вода с различным содержанием декстрапсульфата в системе:
1 — 2,3 • 10-'%; 2 — 3,8 • 10~i%;
д_5 . 10-'%;4—1 • 10-'%; Д--0
о том, что минимум свободной энергии системы достигается при полной компенсации заряда кислого полисахарида (см. рис. 10). Нерастворимость заряженных комплексов глобулярных белков с кислыми полисахаридами, по-видимому, определяется условием максимальной гидрофобности такого комплекса.
Вопрос об образовании заряженных и электронейтральных комплексов желатины с кислыми полисахаридами имеет существенное практическое значение, так как здесь возникает возможность регулирования свойств студней и получения новых студ-необразующих систем. Эта возможность будет продемонстрирована ниже, на примере получения комплексных и смешанных студней. Эффект образования комплексов желатины с альгинатом и пектином использован также для получения второй, устойчивой к нагреву оболочки на зернах искусственной зернистой икры, что позволило повысить температурную стабильность продукта и улучшить его консистенцию (см. гл. IV). Кроме того, эти комплексы были использованы также для получения ряда других искусственных продуктов питания [120].
При исследовании взаимодействия кислых полисахаридов и белков, осаждающихся в изоэлектрических условиях (глобулины и глютелины), показано, что при рН ниже ИЭТ белка поведение этих систем аналогично поведению рассмотренных выше систем, содержащих альбумины. Однако при смешении растворов макро-модекулярных компонентов при рН выше ИЭТ белка и последующем введении в систему кислоты и смещении величины рН в кислую область (рис. 11, система казеин—декстрансульфат—вода) вместо экстремального характера изменения рассеяния света, характерного для процесса коагуляции этих белков в изоэлектри-ческой точке, зависимость светорассеяния от рН описывается кривой с насыщением [123—125 ]. По мере увеличения содержания в системе кислого полисахарида интенсивность рассеяния падает, а кривая сдвигается в область более низких рН. Выше некоторой критической концентрации кислого полисахарида в си-
з*
68 Глава вторая
стеме ее титрование кислотой вообще не сопровождается осаждением белка во всем исследованном интервале рН. Взаимодействие глобулинов и глютелинов с кислыми полисахаридами при рН выше ИЭТ белка приводит, следовательно, к образованию электростатических комплексов, которые по мере увеличения содержания в системе кислого полисахарида осаждаются при все более низких значениях рН, а затем и вовсе не осаждаются из раствора. Иначе говори, при смешении глобулинов или глютелинов с кислыми полисахаридами в щелочной области рН они ведут себя в дальнейшем подобно альбуминам и не осаждаются при ИЭТ. Обнаруженный эффект позволяет регулировать физико-химические свойства растворов белков при их переработке в искусственные продукты питания. Это же явление может быть, по-видимому, использовано и для выделения белков из различных источников, а также для их очистки.
Для изучения свойств белков, связанных с различными кислыми полисахаридами и другими полиэлектролитами, удобным объектом оказались ферменты, так как кинетические параметры катализируемых ими ферментативных реакций чрезвычайно чувствительны как к изменению конформаций макромолекул белка — фермента, так и к свойствам окружающей среды. Исследования, выполненные в этом направлении, показали, что ни на одной из большого числа исследованных систем не обнаруживается каких-либо эффектов, указывающих на изменение «собственных» свойств белка в комплексе с кислым полисахаридом. Исследованные ферменты сохраняли активность как в составе растворимых, так и нерастворимых комплексов с кислыми нолисаха-ридами. Поскольку такие электростатические комплексы к тому же разрушаются при повышении ионной силы (примерно до 0,2М), исследованные полисахариды и другие полиэлектролиты при их введении в пищевые продукты не должны изменять ата-куемость белков и других компонентов пищи ферментами желу-дочно-кишечного тракта [118, 126].
Наблюдаемое влияние полиэлектролитов на свойства связанных с ними белков может быть полностью объяснено изменением распределения компонентов системы в сфере действия электростатического поля полиэлектролита. В случае, когда компонентом реакции является ион водорода, введение полиэлектролита приводит к изменению рН микроокружения белка по сравнению с рН окружающего раствора. Для комплексов фермент— полианион значение рН-оптимума ферментативной реакции сдвигается в щелочную область, а для комплексов с поликатионом — в кислую. Другими словами, полиэлектролит, изменяя локальную концентрацию ионов водорода вблизи комплекса, оказывает на свойства белка то же действие, что и изменение рН системы: полианион — аналогичное уменьшению рН, а полика-
Физико-химические основы Переработки белкав ЙПО 69
тион — аналогичное увеличению рН. Все эти эффекты подавляются при повышении ионной среды [126, 129—131 ].
Таким образом, в результате изучения систем белок—полиса-харид—вода выявлены условия получения как двухфазных, так и однофазных систем, содержащих различные виды белков и полисахаридов, предложена общая схема переработки белков в виде двухфазных систем и выяснены условия взаимодействия белков и полисахаридов, что открывает возможности регулирования физико-химических свойств растворов белков при их переработке в искусственные продукты питания.
Другая важнейшая физико-химическая задача, возникающая в связи с проблемой получения искусственных продуктов питания, заключается в разработке приемов получения студней, позволяющих регулировать их состав, структуру, механические и другие физико-химические свойства. Этот вопрос будет рассмотрен в следующих разделах данной главы.
СТУДНЕОБРАЗНОЕ СОСТОЯНИЕ И ПРОБЛЕМА ПОЛУЧЕНИЯ ИСКУССТВЕННЫХ ПРОДУКТОВ ПИТАНИЯ
Широкие и разносторонние структурно-физические исследования студней макромолекулярных веществ выполнены в связи с важной ролью студнеобразного состояния в организации и функционировании биологических структур, практическим использованием студней в виде желейных кондитерских, других пищевых продуктов и кулинарных изделий, большим значением студнеобразного состояния в процессах переработки технических полимеров через растворы, а также при получении различных мембран, сорбентов, включая материалы для хроматографии, и при иммобилизации ферментов. Структура и свойства студней пищевых полимеров анализируются в ряде обзоров [32, 34, 37, 132—146], а также в монографии Папкова [38]. Условия получения и свойства студней пищевых студнеобразоватслей рассмотрены в работах [147—154].
Следует, однако, отметить, что практическое применение студней в различных областях техники и пищевой технологии резко опережает их изучение и понимание природы студнеобразного состояния. Несмотря, например, на многочисленные научные работы (многие десятки тысяч публикаций) в области пищевых студнеобразователей, получение желейных кондитерских изделий до сих пор основывается преимущественно на практическом опыте, а подбор студнеобразующих систем и рецептур продуктов осуществляется эмпирически [155]. Состояние проблемы студнеоб-
70 Глава вторая
разного состояния в общем такое, что ее нельзя считать в достаточной степени решенной [38].
Вопрос о природе студнеобразного состояния служил предметом многочисленных дискуссий [156—160]. Его подробное обсуждение, однако, выходит за рамки рассматриваемой нами проблемы. Как отмечено выше, переработка белка связана с получением многокомпонентных пищевых студней с необходимым составом и свойствами [1, 2, 161—164]. Поэтому основная задача физико-химических исследований, возникающая в связи с проблемой получения искусственных продуктов питания, заключается в разработке путей получения студней с регулируемым составом, структурой, механическими и другими физико-химическими свойствами [1, 2]. По своему характеру она, очевидно, тесно примыкает к другим физико-химическим задачам получения изделий с необходимым комплексом свойств, возникающим, в частности, при получении желейных пищевых продуктов и технических полимерных материалов. (Возможность широкого использования при получении искусственных продуктов питания опыта и техники мокрого прядения, экструзии и гранулирования, а также опыта применения студнеобразователей в пищевой промышленности будет показана в гл. IV.) В то же время проблема получения искусственных пищевых продуктов весьма специфична и выдвигает физико-химические задачи, существенно отличные от возникающих в указанных двух областях. Поэтому она требует иного подхода к исследованию студней. Кратко остановимся на характерных особенностях области получения искусственных продуктов питания.
Аналогия между процессами получения искусственных пищевых продуктов и технических изделий из полимеров отмечена в ряде работ [1, 2, 34, 164]. Она основана на том, что искусственные продукты получают переработкой пищевых полимеров — белков и полисахаридов — с помощью технологических процессов, применяемых при производстве текстильных волокон, пленок, клеев, пластмасс и т. п. Это позволяет использовать научно-технический опыт, накопленный в области переработки технических полимеров. Рассмотренная аналогия является, однако, далеко неполной. Различие между двумя областями связано, в частности, с ярко выраженной многокомпонентностью перерабатываемых пищевых систем, разнообразием функций биополимеров в процессахих переработки и в составе готовых искусственных пищевых продуктов, а также высокой гетерогенностью перерабатываемых белков по составу, молекулярным характеристикам и физико-химическим свойствам, преимущественно полиэлектролитной природой и особенностями конформации биополимеров. Так, белки имеют преимущественно глобулярную конформацию, не характерную для технических полимеров. Далее, хотя получение
Физико-химические основы переработки белка в ИПП 71
технических материалов путем переработки растворов полимеров (волокна, пленки, клеи, покрытия) протекает через стадию студнеобразного состояния [34, 37, 38], для готовых технических полимерных изделий это состояние не характерно. Напротив, в случае искусственной пищи студнеобразное состояние присуще не только промежуточным, но и конечным продуктам. Отсюда возникает ряд требований к механическим и другим физико-химическим свойствам пищевых студней как готовых искусственных продуктов питания.
Основной прием получения искусственных пищевых продуктов, т. е. прием смешения пищевых веществ со студнеобразова-телем и перевода жидких систем в студнеобразное состояние, широко используют в пищевой промышленности. Оставляя в стороне получение пудингов, муссов, заливных и других кулинарных изделий, отметим, что опыт производства желейных и взбив-иых пищевых продуктов (кондитерские желе, мармелады, пастила, зефир и т. п.) представляет определенную ценность для получения искусственной пищи. Прежде всего, в обоих случаях используют одни и те же студнеобразователи. В отечественной кондитерской промышленности применяют желатину, пектин, агар-агар, агароид, крахмал и его производные [154, 156]; в других странах — также альгинаты, каррагенин, производные целлюлозы и различные камеди [147—154]. Отсюда следует возможность использования в производстве искусственных пищевых продуктов технологического опыта приготовления растворов пищевых студнеобразователей, их формования и перевода в студнеобразное состояние для фиксации формы изделий и приданияимнеобходимых свойств. В то же время между производством кондитерских изделий и искусственных продуктов питания существуют принципиальные различия. Они вытекают из различия в назначении обоих типов продуктов и их места в рационе питания. Кондитерские изделия представляют собой вкусовые продукты и в большинстве случаев содержат лишь углеводы в сочетании с вкусовыми и ароматизирующими добавками. Они практически не содержат белка и имеют низкую пищевую ценность. Напротив, искусственные пищевые продукты предназначены играть важную, если по решающую, роль в рационе человека, будучи продуктами массового потребления.
Искусственные продукты питания содержат большое количество полноценных белков и обладают высокой биологической ценностью, а по структуре, органолептическим и потребительским свойствам должны имитировать различные традиционные пищевые продукты, в том числе и те, которые подвергаются кулинарной обработке при нагреве. Поэтому решающее отличие искусственных продуктов от желейных кондитерских изделий заключается в их составе (высокое содержание белка) и комплек-
| Глава вторая |
се свойств (пригодность для кулинарной обработки и т. п.) Еще одно отличие вытекает из различия в масштабах производства. Производство искусственных пищевых продуктов уже в ближайшие годы будет исчисляться многими миллионами тонн (см. гл. V). Иными словами, речь идет о развитии новой крупнотоннажной отрасли промышленности, которая по объему превысит производство пластмасс и полимерных материалов. Очевидно, что такое различие в' масштабах диктует принципиально иные требования к сырью, с точки зрения его качества и стандартности, а также к технологии. Задача получения искусственных продуктов питания может быть решена лишь путем создания высокоавтоматизированных непрерывных производственных процессов на основе доступного, дешевого и высокостандартного по функциональным свойствам сырья.
Таким образом, сравнение с двумя ближайшими по характеру физико-химических задач и технологии областями производства показывает, что специфика области получения искусственной пищи связана с составом, комплексом свойств конечных продуктов и приемами их получения. При этом критерии выбора студнеобразователей, способов получения студней и подход к их исследованию определяются требованиями к составу, свойствам искусственных продуктов и объемомих производства.
Отметим также, что в связи с получением искусственных пищевых продуктов большой интерес представляют работы в области моделирования биологических тканей. Здесь следует отметить, что натуральная пища и многие виды сырья для получения традиционных продуктов питания представляют собой биологические ткани, растительные или животные. Поэтому задача получения искусственной пищи, хотя бы частично, может быть сведена к моделированию некоторых особенностей макроструктуры и свойств таких тканей. Этой цели служат исследования растворов и студней белков и полисахаридов, т. е. важнейших биополимеров, выполняющих структурные функции, а также изучение студней анизотропной структуры.
Перейдем теперь к рассмотрению требований к студнеобразо-вателям с позиций проблемы получения искусственной пищи.
С точки зрения состава искусственных пищевых продуктов, студнеобразоватсль должен обеспечивать высокое содержание белка и других пищевых веществ в продукте. Пищевые белки, как правило, растворимы в воде (альбумины), солевых (глобулины) или же щелочных (глютелины) средах. Белковое сырье, перерабатываемое в искусственные продукты питания (см. гл. III), обычно представляет собой сложную смесь указанных фракций. Ввиду того что белки не во всех случаях могут выполнять функции студнеобразователей, а также вследствие ограниченности сырьевой базы и сравнительно высокой стоимости многих бед-
Физико-химические основы переработки белкав ЙПП 73
ковых студнеобразователей (желатина, яичный альбумин, белки семян масличных, клейковина) представляется целесообразным использовать для получения искусственных пищевых продуктов студнеобразователи небелковой природы, особенно при переработке белкового сырья с низкими функциональными свойствами (плохая растворимость, неспособность к образованию студней). И этом случае пищевым белкам отводится роль наполнителей студней [I]. В связи с этим большое значение имеет совместимость и характер взаимодействия студнеобразователей, в первую очередь кислых полисахаридов, с белками и их способность образовывать студни в присутствии различных белков при учете гетерогенности белкового сырья. Эти вопросы рассмотрены выше. В качестве небелковых студнеобразователей наиболее широко используют кислые полисахариды (альгинат, пектин и др.),
а также крахмал.
Подход к получению искусственных продуктов питания как к рационально^ организованной переработке белка определяет потребность в студнеобразователях, «универсальных по белку», т. е. способных образовывать студни в присутствии разнообразных пищевых белков, а также в широком диапазоне условий. К числу таких студнеобразователей можно отнести желатину, образующую студни в широком интервале рН и в присутствии большого числа солей и других веществ. Показано [167—173], что желатина способна образовывать студни и в присутствии ряда пищевых белков. Еще больший интерес в этом отношении представляют наполненные белками студни полисахаридов, а также комплексные и смешанные студни белков и полисахаридов (см.
ниже).
Требования к студнеобразователю с точки зрения свойств готового продукта специфичны для каждого конкретного типа искусственного продукта и в общем виде не могут быть сформулированы. Достаточно сказать, что речь идет о комплексе свойств, включающем такие характеристики, как прочность, эластичность, твердость, степень и скорость набухания, температура плавления, окраска и т. п. Например, для ряда искусственных продуктов (макаронные изделия, рис и др.) желательно, чтобы студнеобразователи были бесцветны и не имели специфического вкуса и запаха. Как правило, это достигается при соответствующей степени очистки.
Отметим также факторы, связанные с режимом кулинарной обработки. Для получения искусственных пищевых продуктов, применяемых в холодном виде (икра, мясные завтраки, молочные продукты и т. п.), могут быть использованы вещества, образующие сравнительно низкоплавкие студни за счет водородных связей или ван-дер-ваальсовых сил, включая гидрофобные взаимодействия (желатина, агар-агар, агароид, крахмал, высокоэтери-
{'лава вторая
фицированный пектин и др.). С другой стороны, многие продукты применяются в горячем виде и, кроме того, их подвергают относительно жесткой термической (печение или жарение) или гидротермической (варка) обработке. В этом случае студни должны выдерживать нагрев при температуре 140—240° в воздушной или масляной среде или же продолжительное воздействие кипящей воды. Для этого необходимы вещества, образующие студни за счет ковалентных или ионных связей, например, альгинат и пектинат кальция, а также некоторые белки, денатурирующие при нагреве с образованием сетки межмолекулярных дисульфид-ных связей.
В силу важного значения способности искусственных пищевых продуктов выдерживать нагрев в условиях кулинарной обработки, способности к длительному хранению, а также необходимости регулирования консистенции и других органолептиче-ских и потребительских характеристик продукта требуется контролировать условия плавления, термомеханические свойства, ползучесть при постоянной нагрузке, кинетику и равновесную степень набухания студней в различных водных средах и температурных условиях.
Вопрос о биологической ценности студнеобразователей как компонентов искусственных продуктов питания рассмотрен ниже, в гл. III. Отметим лишь, что с этой точки зрения использование высоких концентраций студнеобразователя (10—15% и более) целесообразно лишь для белков, полноценных по составу (белки семян масличных и др.). Необходимо также, чтобы студнеобра-зователи, используемые для создания искусственных пищевых продуктов, не обладали токсическим или аллергическим действием, а также не образовывали подобного рода веществ в процессе получения, хранения искусственного пищевого продукта или при его кулинарной обработке.
В условиях крупнотоннажного производства большое значение приобретают экономические аспекты использования студнеобра-зователей: их ресурсы, стоимость производства и расход при получении той или иной формы искусственной пищи. Очевидно, что при выборе студнеобразователя следует стремиться к тому, чтобы его концентрация в продукте и соответственно расход были минимальными. Это диктуется не только экономическими соображениями, но и тем обстоятельством, что снижение концентрации студнеобразователя может облегчить его совмещение с пищевыми веществами — наполнителями студня. Исключение, естественно, составляют студни полноценных белков, концентрация которых может быть высокой (10—15% и выше).
Расход студнеобразователей при производстве искусственных пищевых продуктов определяется так называемой критической концентрацией студнеобразования, т. е. минимальной концентра-
Физико-химические основы переработки белка в ИПП 75
цией вещества, при которой в объеме системы образуется единая пространственная сетка [133], а также концентрационной зависимостью реологических свойств студня. По этим показателям отдельные студнеобразователи сильно различаются между собой. Например, критическая концентрация студнеобразования желатины при комнатной температуре составляет менее 1 %, однако студни с модулем упругости Ю3—104 н/м1 образуются лишь при концентрации 5—10%. С другой стороны, такие студнеобразователи, как агар-агар, низкоэтерифицированный пектин, альгинат, образуют студни с таким же модулем упругости при концентрации 1% и ниже. В большинстве случаев полисахариды образуют студни при значительно меньших концентрациях, чем белки.
В некоторых случаях экономические факторы могут серьезно ограничивать использование тех или иных студнеобразователей при производстве искусственных продуктов питания. Так, в нашей стране в настоящее время возможности применения таких классических студнеобразователей, как желатина и агар-агар, ограничены в первом случае высокой стоимостью и недостаточными масштабами производства, а во втором — узостью сырьевой базы. В то же время возможности производства и применения альги-ната, пектинов, производных целлюлозы и крахмала весьма велики, однако пока что они реализованы далеко не в полной мере. Особенно перспективны кислые полисахариды, потенциальные ресурсы которых практически не ограничены, а производство
дешево и несложно.
В качестве показателя экономической эффективности использования того или иного студнеобразователя можно было бы принять произведение его концентрации, отвечающей студню с определенным модулем упругости, на цену данного студнеобразователя. На сегодняшний день, однако, когда масштабы производства ряда важнейших студнеобразователей в нашей стране незначительны по отношению к ресурсам этих веществ и потенциальной сфере их использования, принимать в расчет их текущую цену вряд ли оправдано. Можно ожидать, что развитие исследований в области искусственной пищи приведет к расширению масштабов производства и снижению цен на многие студнеобразующие
вещества.
С точки зрения способов получения искусственных продуктов питания и аппаратурного оформления этих процессов первостепенное значение имеют условия перевода смеси структурообразующих и пищевых веществ в студнеобразное состояние. Эта стадия процесса обеспечивает фиксацию формы продукта и в значительной мере определяет качество готового искусственного продукта питания. Опа следует за стадией формования, осуществляемой в жидком состоянии. Перевод в студнеобразное состояние сформованной системы чаще всего производится путем изме-
| Глава вторая |
нения температуры (охлаждение или нагрев) или путем введения (диффузии) в систему ионов металлов и других осадителей. Эти процессы должны быть достаточно «технологичными», т. е. протекать непрерывно, с оптимальной и регулируемой скоростью и не требовать сложного или громоздкого оборудования. Так, диффузия осадителей — ионов металлов в растворы альгината или пектина из-за низкой скорости процесса обычно применима лишь для получения волокон, оболочек гранул [167] и других одно- и двумерных структурных элементов продукта. Этот процесс мало пригоден для получения объемных (трехмерных) продуктов однородной структуры, например искусственного жареного картофеля или макаронных изделий, поскольку для образования однородного студня путем диффузии требуется слишком большое время. В этом случае целесообразнее использовать соли, растворяющиеся при нагреве (глюконат, лактат кальция и т. п.), заменив диффузию через границу раздела двух растворов диффузией ионов из большего числа диспергированных в системе частиц соли (см. гл. IV).
Таким образом, можно сформулировать ряд общих требований к студнеобразователям, используемым для производства искусственной пищи:
1) способность совмещаться с другими компонентами пищи и образовывать студни в присутствии большого числа пищевых веществ, в первую очередь белков, в широком диапазоне условий;
2) способность образовывать студни с комплексом физико-химических свойств, обеспечивающих требуемую консистенцию продукта, пригодность для продолжительного хранения без заметного синерезиса и изменения структуры, пригодность искусственного пищевого продукта для кулинарной обработки и другие потребительские и технологические характеристики;
3) низкая критическая концентрация студнеобразования и сравнительно резкая зависимость реологических свойств студня от концентрации;
4) регулируемая скорость студнеобразования и технологичность перевода жидкой системы в студнеобразное состояние;
5) отсутствие токсического или аллергического действия;
6) низкая стоимость и широта сырьевой базы. Анализ литературных данных (см. гл. IV) и результатов, полученных в ходе исследований в Институте элементоорганиче-ских соединений АН СССР (ИНЭОС), по разработке способов получения искусственных продуктов питания показывает, что известные в настоящее время студнеобразователи в большинстве случаев не способны обеспечить комплекс требований, предъявляемых к тому или иному продукту. Новые возможности открываются при использовании нескольких студнеобразователей [1, 2].
Физико-химические основы переработки белка вИПП 77
При этом оказывается возможным получение студней с характеристиками, принципиально недостижимыми в случае применения отдельных студнеобразователей. Несмотря на очевидную перспективность использования студней, образованных более чем одним студнеобразователем, эти системы до недавнего времени оставались практически неизученными. То же можно сказать и о возможности регулирования состава и биологической ценности пищевых студней путем их наполнения белками и полисахари-дами. Поэтому в ИНЭОС АН СССР в последние годы были систематически исследованы следующие системы [22].
Наполненные студни, в которых один из макромоле-кулярных компонентов выступает в качестве студнеобразователя, а другие играют роль наполнителей. К этой же группе можно отнести студни, наполненные твердыми или жидкими дисперсными частицами пищевых веществ.
Смешанные студни*, в которых существуют две или более пространственные сетки, образованные различными студне-образователями. Необходимым условием для получения смешанных студней является отсутствие специфического взаимодействия между студнеобразователями.
Комплексные студни**, пространственная сетка которых образована продуктами взаимодействия двух или более студнеобразователей. К этой группе могут быть также отнесены наполненные студни с активным наполнителем, т. е. с таким, который взаимодействует со студнеобразователем, принимая участие в организации пространственной сетки студня.
В особую группу следует выделить анизотропные студни различной макроструктуры. Некоторые подходы к получению таких систем рассмотрены выше. Исследования в этом направлении связаны в первую очередь с необходимостью разработки новых способов получения искусственных мясопродуктов, характеризующихся более высокой по сравнению с существующими методами (см. гл. IV) экономической эффективностью и позволяющих перерабатывать белки с пониженными функциональными свойствами.
Характерные свойства перечисленных групп студней будут продемонстрированы ниже преимущественно на примере двух веществ: желатины и альгината натрия, которые образуют студии, резко различные по природе и свойствам, и, кроме того, являются практически интересными студнеобразователями.
* Этот термин был введен впервые в работе [174], посвященной использованию для приготовления заливных блюд студней, образованных комплексами желатины и пектина. На наш взгляд, такие студни правильнее-пазынать комплексными.
** Термин введен Бунгенберг де Йонгом [35, 36] для студной желатины, на-
* полненных дисперсными каплями коацервата желатины и гуммиарабика.
| Глава вторая |
Желатина, как известно, образует студни при понижении температуры, причея процесс студнеобразования сопряжен с кон-формационным переходом клубок—спираль и образованием агрегатов спирализованных макромолекул [143]. Студни желатины плавятся при повышении температуры и вновь возникают при охлаждении, т. е. относятся к группе термообратимых студней.
Альгинат натрия образует студни при взаимодействии с ионами кальция и других поливалентных металлов [150, 154]. Пространственная сетка студней дополнительно стабилизована координационными связями между ионами кальция и гидроксильными группами, преимущественно остатков гулуроновой кислоты [175, 176]. Студни альгината стабильны при нагреве (вплоть до температуры кипения растворителя — воды), но претерпевают обратимый переход в жидкое состояние при изменении ионного состава окружающей среды. Соответственно такие студни можно назвать ионообратимыми.
Взаимодействие желатины и альгината натрия в разбавленных растворах рассмотрено в предыдущем разделе. Полученные результаты позволили определить условия образования смешанных и комплексных студней. Несовместимость студнеобразователя
(сосредоточенного преимущественно в непрерывной фазе системы) с другими пищевыми компонентами может приводить к получению студней, наполненных сферическими или анизодиамет-ричными (деформированными) дисперсными частицами, жидкими или твердыми. Напротив, взаимодействие студнеобразователя с другими компонентами пищи может приводить к получению смешанных, наполненных или комплексных студней. Естественно, что между наполненными, смешанными и комплексными студнями не всегда можно провести резкую границу, особенно в многокомпонентных реальных системах. Изменение состава студнеобра-зующей системы и условий получения студня открывает возможность перехода от одного типа студня к другому. Таким образом, появляется возможность регулирования комплекса физико-химических свойств студня путем изменения структуры и природы его пространственной сетки. Ряд примеров будет приведен ниже.
РЕГУЛИРОВАНИЕ СОСТАВА, СВОЙСТВ И СТРУКТУРЫ СТУДНЕЙ
НАПОЛНЕННЫЕ СТУДНИ
Наиболее подробно влияние наполнителей на свойства студней изучено на примере студней желатины, содержащих белки (сывороточный и яичный альбумины в нативном и денатурированном состоянии, а также казоыи) и полисахариды (декстран),
___Физико-химические основы переработки белкав ЙПЙ 79
а также студней желатины, наполненных каплями раствора декстрана [170, 171 ]. Последние системы можно рассматривать как модели изотропных двухфазных продуктов питания.
Было установлено, что введение белков (нативных и денатурированных) в студни желатины не оказывает существенного влияния на степень набухания (в растворах хлористого натрия), температуру плавления, податливость и скорость релаксационных процессов при условии, что макромолекулы белка могут быть размещены в ячейках пространственной сетки студня. Наблюдаемое в некоторых случаях резкое возрастание степени набухания наполненных студней в воде, например студней желатины, содержащих 5—7% и более казеина, подавляется введением в иммерсионную жидкость электролита (поваренной соли). При высоких концентрациях' наполнителя наблюдается возрастание степени набухания, податливости студней, повышение скорости релаксации деформации, а также снижение температуры плавления
студней.
Образование комплексов между наполнителем и студнеобра-зователем, т. е. переход от наполненных к комплексным студням, приводит к глубоким изменениям физико-химических свойств студней. В результате исследования вязкости растворов смеси желатины и сывороточного альбумина человека было показано [177], что эти белки не взаимодействуют при рН 2—5 и, напротив, взаимодействуют при рН 8—9 с образованием комплексов за счет сил пеэлектростатической природы. В последнем случае перевод системы в студнеобразное состояние приводит к получению студней со свойствами, резко отличающимися от свойств
наполненных студней [170].
К сожалению, в отличие от белок-полисахаридного взаимодействия вопросы взаимодействия белок—белок развиты явно недостаточно для того, чтобы можно было направленно регулировать структуру и свойства белковых студней, содержащих несколько белков. В этом плане, столь важном для рассматриваемой проблемы, их роль отчетливо показана лишь в работах [170, 177]. В отличие от белок-полисахаридного взаимодействия, носящего преимущественно электростатический характер, в случае систем, содержащих несколько белков, помимоих несовместимости (образование наполненных студней) и электростатического взаимодействия белков с различными ИЭТ, возможно также межмолекулярное гидрофобное взаимодействие, образование ковалентных (дисульфидных) и водородных связей. Этот вопрос, следовательно, весьма сложен. Он, однако, имеет большое практическое значение, поскольку перерабатываемое белковое сырье, как отмечалось выше, обычно отличается гетерогенностью и представляет собой смеси белков с различными физико-химическими свойствами. Поэтому здесь можно ожидать получения белковых студней,
80 Глава вторая
наполненных, смешанных или комплексных, с существенно различными свойствами в зависимости от характера взаимодействия макромолекул белков в процессе студнеобразования.
Изменение объемных свойств студней при их наполнении белками было изучено также на примере смешанных альгинат-крах-мальных студней и дало результаты, аналогичные полученным при наполнении белками студиец желатины [169—172 ].
В целом при отсутствии специфического взаимодействия между белком-наполнителем и студиеобразователем изменение объемных свойств студней под действием наполнителей описывается в терминах изменения числа узлов сетки студня. Эти изменения, однако, невелики, и свойства наполненных студней обычно не слишком отличаются от свойств кенаполненных [2, 170, 178].
Более резкие изменения при введении белков претерпевают поверхностные свойства студней. Было обнаружено, что студни желатины характеризуются аномально высокой гидрофобностью. Они очень плохо смачиваются водой и по гидрофобности превосходят все известные материалы [8, 9, 178]. Например, контактный угол воды на поверхности 14%-ного студня желатины составляет 123°, в то время как самое высокое значение контактного угла на углеводородной поверхности, полученное на сколе монокристалла м-гексатриаконтана, составляет 111°. Введение в студни желатины глобулярных белков оказывает различное влияние на смачиваемость студней водой в зависимости от поверхностной активности глобулярного белка, его способности к поверхностной денатурации и других факторов. Так, введение яичного альбумина несколько увеличивает гидрофобность студней, напротив, уже небольшие добавки казеина (0,5%) делают поверхность студня гидрофильной. Контактный угол воды на поверхности студня желатины, содержащего 12,7% казеина, в среде вазелинового или кукурузного масла составляет около 28°, а на поверхности студня желатины, не содержащего казеин, в этих же условиях — около 134°. Такой эффект может иметь практическое значение в различных областях применения желатиновых студней. Он был, в частности, использован при получении искусственной зернистой икры, студнеобразные гранулы которой получают введением капель нагретого раствора желатины (5—8%) содержащего 15% казеина, в охлажденное растительное масло.' Последующая обработка студнеобразных гранул (дубление, окрашивание оболочки и т. д.) (см. гл. IV) требует предварительной отмывки их поверхности от следов масла. Эффективность процесса вытеснения масла водой с поверхности гранул определяется поверхностными свойствами студня, масла и воды. В соответствии с этим гранулы студня желатины, содержащего казеин, в отличие от гранул студня желатины, легко отмываются от масла водой при перемешивании в течение 5—10 мин. Казеин может
Физико-химические основы переработки белка в Hlltl 81
быть при необходимости добавлен к другим белкам приих переработке в искусственную зернистую икру с целью регулирования поверхностных свойств гранул.
При исследовании наполнения студня желатины полисахари-дами, выполненном на системе желатина—декстран—вода, установлено, что зависимость податливости студней желатины от концентрации л лих декстрана описывается кривой с минимумом, отмечающим переходу от однофазных студней, содержащих раствор декстрана, к студням, наполненным каплями раствора декстрана [171]. Положение этого перехода по шкале концентраций декстрана в системе зависит от молекулярного веса послед-пего. Интересно отметить, что в присутствии небольших количеств декстрана, отвечающих однофазному состоянию системы желатина—декстран—вода, резко ускоряются все стадии процесса структурообразования желатины, т. е. конформационный переход, образование фибриллярных агрегатов и формирование пространственной сетки студня. Напротив, студни желатины, наполненные каплями раствора декстрана, имеют более высокую податливость, чем студень желатины, и податливость наполненных студней растет с увеличением объемной доли фазы декстрана. Податливость наполненных студней снижается по мере уменьшения размера капель декстрана при неизменной их объемной доле. Электронно-микроскопическое исследование показало, что r окрестности капель наполнителя сетка студня разорвана и ее фибриллы, примыкающие к капле, ориентированы свободными концами перпендикулярно ее поверхности. Такая ориентация, очевидно, обеспечивает минимизацию контакта фибрилл желатины с макромолекулами декстрана. Наличие разрывов или свободных концов элементов структуры студня снижает число активных фибрилл, участвующих в процессе деформации, и, по-видимому, служит основной причиной увеличения податливости студня желатины при его наполнении каплями раствора полисахарида.
Сопоставление результатов исследования студней желатины, наполненных глобулярными белками и декстраном, показывает, что между наблюдаемыми эффектами имеется много общего. Во всех случаях влияние наполнителей на структуру и свойства студней желатины связаны с изменением эффективного числа узлов пространственной сетки студня, хотя природа этих изменений может быть различной.
Слабое влияние белковых наполнителей на объемные свойства студней указывает на перспективность приема наполнения студней белками в плане регулирования состава искусственных продуктов питания. Это обеспечивает универсальность по белку способов получения различных форм искусственной пищи. Путь наполнения студней белками был использован для получения. искусственной зернистой икры, зерна которой представляют собой
| Глава вторая |
гранулированные студни желатины, наполненные казеином и покрытые одной или двумя оболочками [167, 168, 173, 178]. Наполнение белками смешанных альгинат-крахмальных студней лежит в основе процессов получения искусственных макаронных и картофельных продуктов [169, 172].
СМЕШАННЫЕ СТУДНИ
Смешанные студни желатины и альгината кальция получали путем диффузии уксуснокислого кальция в студень желатины, содержащий альгинат натрия. Для этого водные растворы желатины и альгината натрия смешивали при 40°, охлаждали в форме и затем на поверхность студня желатины, содержащего альгинат натрия, наслаивали раствор уксуснокислого кальция. В полученных таким образом смешанных студнях можно разрушить одну из пространственных сеток без нарушения формы и целостности образца. Для разрушения пространственной сетки желатины достаточно нагреть смешанный студень до 40° на воздухе или в воде, а сетку альгината кальция можно разрушить, обрабатывая смешанный студень разбавленным раствором щелочи или же путем введения в студень хлористого натрия. На рис. 12 показаны термомеханические кривые студней желатины, альгината кальция, а также смешанного студня желатины и альгината кальция. Студни желатины плавятся при температуре около 30°. Для студней альгината кальция область высокоэластического состояния простирается вплоть до температуры кипения растворителя. На рисунке видно, что при введении в смешанный студень 0,5 М хлористого натрия он ведет себя, как студень желатины. Аналогичные результаты получены при исследовании ползучести студней при постоянной нагрузке и различных значениях температуры. В целом эти результаты согласуются с представлением о наличии в смешанном студне двух независимых пространственных сеток желатины и альгината кальция [1, 2, 179—181 ].
Сравнение термомеханических свойств студней желатины, альгината кальция и смешанных студней показывает, что последние отличаются существенно более сложным поведением при нагреве (см. рис. 12). На термомеханических кривых смешанных студней можно выделить три характерных участка. Ниже температуры плавления студня желатины, т. е. ниже 30°, ход термомеханических кривых смешанных студней близок к кривой для студня желатины, а выше 45° — к кривой для студня альгината кальция. В промежуточной области температур (30—45°) наблюдается аномально высокая деформируемость смешанных студней с максимумом податливости при 34—38°. Положение по температурной шкале и интенсивность максимума податливости зависят от состава смешанного студня и скорости нагрева. Явление ано-
Физико-химическив основы переработки белка в ИПП 83
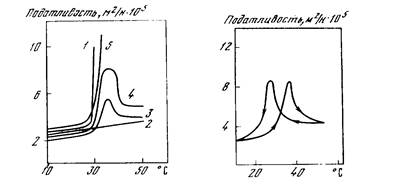
Рис. 12. Термомеханические кривые 10%-ного студня желатины (1), 1%-ного студня альгината кальция (2), смешанных студней: желатина (10%) — альгинат кальция (1%) (кривая 3) и желатина (10%)—альгинат кальция (0,5%) (кривая 4) того же смешанного студня, содержащего 0,5 М хлористого натрия (5)
Скороть нагрева 0,3 граЭ/лшн; напряжение 740 нД*'; продолжительность действия нагрузки 5 сек.
Рис. 13. Термомеханические кривые смешанного студня, содержащего 10% желатины и 0,5% альгината кальция, при нагреве и охлаждении системы
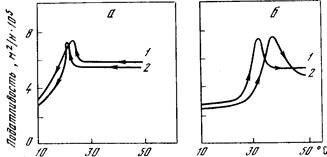
Рис. 14. Термомеханические кривые смешанного студня, содержащего 10% желатины и 0,5% альгината кальция
а—охлаждение системы со скоростью 0,2 град/мин (1) и 0,5 град/мин (2); б—первичный (2) и повторный (J) нагрев. Студень предварительно термостатирован в течение 7 суток при 10° С; повторный нагрев того же образца студня после его охлаждения и термостатирования в течение 2 час. при 10° С
мальной деформируемости хорошо воспроизводится при многократном нагреве и охлаждении системы. Оно весьма чувствительно к скорости нагрева или охлаждения, т. о. носит ярко выраженный кинетический характер. В качестве примера на рис. 13 и 14 приведены термомеханические кривые, полученные при на-
84 Глава вторая
греве и охлаждении системы, а также при первичном и повторном нагреве смешанного студня и при охлаждении системы с двумя различными скоростями.
Явление аномальной деформируемости смешанных студней может быть объяснено ступенчатым характером распада сетки студня желатины, которая, как известно, построена из агрегатов макромолекул. Нагрев смешанного студня до температуры порядка 30° приводит к распаду трехмерной сетки студня желатины на агрегаты макромолекул. В промежуточной области температур (30—45°) система представляет собой студень альгината кальция, дисперсионная среда которого представляет собой раствор агрегатов макромолекул желатины в воде. Такой раствор обладает сравнительно низкой вязкостью. Дальнейшее повышение температуры приводит к распаду агрегатов макромолекул и образованию молекулярно-дисперсного раствора желатины, вязкость которого значительно выше. Возрастание вязкости дисперсионной среды студня альгината кальция проявляется в снижении деформируемости студня'в выбранном режиме испытаний. Выше области температур распада сетки студня желатины равновесная податливость системы отвечает упругости сетки студня альгината кальция. При исследовании термомеханических свойств, однако, измеряется неравновесное значение податливости, отвечающее режиму измерения. Это значение зависит от вязкости дисперсионной среды студня: оно тем ниже, чем выше вязкость. Поэтому в области температур несколько выше температуры разрушения сетки студня желатины при минимальной вязкости дисперсионной среды система обладает максимальной податливостью в режиме термомеханических испытаний.
Дополнительное подтверждение этих представлений получено при исследовании ползучести смешанных студней желатины и альгината кальция в характерных температурных интервалах изменения их податливости при термомеханических испытаниях. На рис. 15 в качестве примера приведены кривые ползучести смешанного студня при 28, 34 и 40°. Видно, что ползучесть студней при 34° выше, чем при 40°. Общий характер явления аномалии податливости систем, содержащих желатину и состоящих из двух относительно независимых пространственных сеток, одна из которых устойчива к нагреву, показан также при исследовании смешанного студня желатины с другим полисахаридом — пектином (рис. 16).
Таким образом, сетка термонеобратимого студня полисахарида может служить своеобразным вискозиметром, позволяющим контролировать изменение вязкости дисперсионной среды термомеханическим методом. В качестве примера приведем термомеханическую кривую студня альгината кальция, содержащего суспензию зерен картофельного крахмала (рис, 17). Клейстеризация
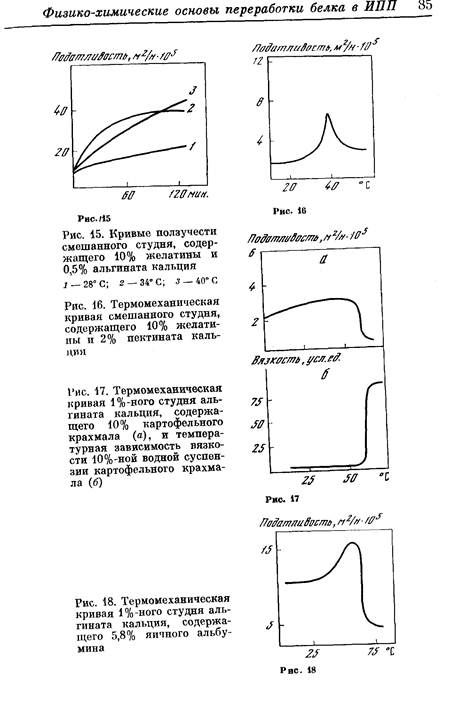
| Глава вторая |
крахмала при температуре около 70° приводит к уменьшению податливости системы. Этот эффект обусловлен возрастанием вязкости дисперсионной среды, о чем свидетельствует приведенная на том же рисунке кривая температурной зависимости вязкости крахмальной дисперсии, полученная с помощью ротационного вискозиметра. Другой пример приведен на рис. 18, где показана термомеханическая кривая студня альгината кальция, содержащего яичный альбумин. Денатурация белка при температуре около 57° также вызывает резкое уменьшение податливости системы с образованием смешанного студня альгинат кальция— яичный альбумин [180].
Таким образом, измерение податливости студней альгината кальция или другого термонеобратимого студня, содержащего белки и полисахариды, представляет собой достаточно простую методику исследования изменений вязкостных свойств растворов и дисперсий этих веществ. Эта методика весьма полезна при решении практических задач переработки белка в искусственные продукты питания, например при получении наполненных и смешанных студней с необходимым составом и консистенцией, т. е. при выборе рецептур искусственных пищевых продуктов.
КОМПЛЕКСНЫЕ СТУДНИ
Наиболее универсальный путь получения комплексных студней основан на явлении образования электростатических комплексов между разноименно заряженными макромолекулами. Образование таких комплексов между белками и кислыми поли-сахаридами рассмотрено выше. К настоящему времени наиболее подробно исследованы свойства комплексных студней желатина— альгинат натрия и желатина—пектин [119, 120, 182, 183], показано также образование комплексных студней желатина—сывороточный альбумин [170] и, по-видимому, также студней крахмал—альгинат кальция [2].
В качестве примера рассмотрим свойства комплексных студней, полученных на основе растворимых и нерастворимых комплексов желатины и альгината натрия [1, 2, 182 ]. Электростатические комплексы желатины и альгината натрия образуются при низкой ионной сило в области рН от 2 до 4,5, где макроионы белка и кислого полисахарида обладают противоположными по знаку зарядами. Изменяя соотношение компонентов при данном значении рН, можно получать как растворимые, так и нерастворимые комплексы.
Нерастворимые комплексы обычно выделяются в виде дисперсных студнеобразных (в случае и жидких) частиц концентрированной фазы (комплексного коацервата). Если концентрированную фазу отделить центрифугированием от равновесной жид-
Физико-химические основы переработки белка вЙПП 87
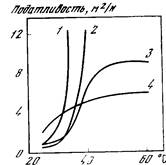
|
Рис. 19. Термомеханическиекривые
l — 20%-ный студеньжелатины;
а — студень концентрированной фазы комплексного коацервата (рН 3,5;
желатина — 20%,альгинат — 5%);
3 — комплексный студень, полученный на основе заряженных комплексен (pit 4,20; желатина—5%, а-чьги-н;|Т—2,5%; время старении 5 суток) ;
4 —то же, что и S, но в 7 М растворе мочевинь/
кости и нагреть выше температуры ее плавления, то возникает макроскопический слой комплексного коацервата в виде вязкой жидкости, охлаждение которой сопровождается переходом в студнеобразное состояние. Полученные таким путем комплексные студни не синерируют и не меняют термомеханических свойств в течение длительного времени. На рис. 19 представлены термомеханические кривые студня концентрированной фазы комплексного коацервата, а также студня желатины. Комплексный студень плавится при несколько более высокой (на 7—10°) температуре
и обладает меньшей податливостью.
Более разительно отличаются по свойствам от студней желатины студни, образованные растворимыми комплексами. Для их получения готовят раствор заряженных комплексов желатина—альгинат, который лиофильно высушивают. Лиофилизирован-ный препарат быстро набухает и растворяется в воде при температуре 40° и выше. При охлаждении до 30° раствор переходит в студнеобразное состояние. Свойства таких комплексных студней, полученных на основе заряженных растворимых комплексов желатина—альгинат, существенно зависят от продолжительности старения (см. рис. 19). Свежеприготовленный комплексный студень имеет термомеханическую кривую, подобную кривой для студня желатины, и плавится при температурах 30—40°. По мере старения (термостатирование образца при 10°) термомеханическая кривая приобретает S-образный характер, т. е. наблюдается переход от термообратимого студня к термонеобратимому. В отличие от студней желатины, в области температур 30—40° обнаруживается лишь скачкообразное возрастание податливости при сохранении упругих свойств. Плавление комплексного студня не наблюдается до 80° и выше. Такое изменение свойств комплексного студня происходит через несколько часов после их получения.
По мере дальнейшего старения наблюдаетсяснижение податливости термонеобратимого студня. Спустя 5 суток термо-
Глава втораЛ
механические свойства такого комплексного студня перестают зависеть от продолжительности старения.
Термомеханические свойства комплексных студней зависят от состава заряженных растворимых комплексов. По мере увеличения доли желатины и соответственно снижения заряда растворимых комплексов податливость студней возрастает, особенно при температурах выше 40°. S-Образный характер термомеханической кривой становится менее выраженным, и она приближается к кривой, характерной для комплексных студней, образованных нейтральными нерастворимыми комплексами. Обнаружено, что в отличие от желатины лиофилизованный препарат растворимых комплексов способен образовывать студни не только в воде, но и в 7 М растворе мочевины. На термомеханических кривых комплексных студней, полученных в концентрированных растворах мочевины, отсутствует скачок деформации в области температур 30—40°. Поскольку в 7 М мочевине существование гидрофобных взаимодействий и водородных связей, по-видимому, исключено, предполагается участие в образовании трехмерной сетки комплексного студня связей электростатической природы. Возрастание деформации в области температур 30—40° для водных комплексных студней может быть объяснено разрушением связей неэлектростатической природы, аналогичных связям, ответственным за образование сетки студня желатины.
Как было показано выше, растворимые заряженные комплексы являются полианионами и содержат желатину в количестве, меньшем эквивалентного. В воде при температуре выше 40° они существуют в растворе как относительно независимые, одноименно заряженные кинетические единицы. Охлаждение сопровождается снижением подвижности комплексов и усилением межли-гандного взаимодействия за счет связей, характерных для межмолекулярного взаимодействия желатины. При этом образуется комплексный студень, близкий по свойствам студню желатины (свежеприготовленный комплексный студень), т. е. термообратимый студень. По мере старения, вследствие флуктуационного характера ионных пар, возможно возникновение новых контактов между комплексами, имеющих уже электростатическую природу. Иными словами, в процессе старения может происходить переход от слабого межлигандного взаимодействия типа желатина—желатина к электростатическому взаимодействию типа желатина— альгинат, т. е. переход от моноядерных комплексов к полиядерным. Комплексный студень становится неплавким и перестает растворяться в растворах мочевины, а введение в студень значительных количеств хлористого натрия резко меняет его термомеханические свойства. Естественно, что чем больше доля желатины в комплексе, т. е. чем выше степень экранирования альгината и ниже отрицательный заряд комплекса, тем меньше возникает
Физико-химические основы переработки белка в ИПП
ионных контактов между комплексами. Поэтому по мере увеличения доли желатины в комплексе термомеханическая кривая комплексного студня приближается к кривой, характерной для студня желатины.
Приведенные примеры показывают, что комплексные студни разительным образом отличаются как от студней отдельных компонентов, так и от смешанных студней. Использование комбинаций студнеобразователей существенно расширяет возможности получения студней, отвечающих по свойствам разнообразным требованиям, которые выдвигает быстро развивающееся производство искусственной пищи.
АНИЗОТРОПНЫЕ СТУДНИ
Получение белковых анизотропных студней волокнистой и пористой макроструктуры получило развитие в связи с производством искусственных мясопродуктов. Они производятся двумя различными методами. Во-первых, путем «мокрого» прядения белковых волокон, их ориентационной вытяжки и последующего склеивания ориентированных волокон пищевым связующим с получением искусственных мясопродуктов в виде студней, наполненных ориентированными волокнами. Во-вторых, механической обработкой грубых водных дисперсий белка при высокой температуре и давлении с последующим резким сбросом давления и охлаждением системы для получения анизотропных студней пористой структуры. Такие студни хорошо имитируют мясопродукты по внешнему виду и консистенции. Оба типа продуктов получают в основном на основе белка соевых бобов, обладающего сравнительно высокими функциональными свойствами. (Методы получения искусственных мясопродуктов будут рассмотрены в гл. IV.),
В последнее время большое внимание уделяется разработке новых методов получения анизотропных белковых продуктов. Необходимость таких исследований диктуется, во-первых, задачей переработки белкового сырья с более низкими функциональными снойствами (более гетерогенного по физико-химическим характеристикам белковых фракций, обладающего пониженной растворимостью и способностью образовывать студни), во-вторых, стремлением к снижению стоимости переработки и, наконец, необходимостью повышения пищевой ценности продукта как за счет более мягких условий процесса, так и благодаря возможности более широкого регулирования химического состава продукта. К числу таких методов относятся «сухое» прядение волокон экструзией нагретых водных концентрированных растворов дрожжевого белка [184, 185], а также методы переработки двухфазных жидких систем [1, 2, 62, 71, 72], подробнее рассматриваемые ниже,
| Глава вторая |
Практически все применяемые до настоящего времени методы придания анизотропии материалам пищевого и технического назначения связаны с ориентацией элементових структуры механическим путем. Однако, помимо механической ориентации, известен метод получения анизотропных студней различной макроструктуры, так называемых ионотропных студней, путем направленной диффузии ионов-осадителей в растворы полиэлектролитов. Этот метод недавно было предложено использовать для получения различных искусственных продуктов питания.
Ниже будут кратко рассмотрены новые приемы получения анизотропных студней, а именно методы переработки двухфазных систем и получения ионотропных студней. (Способы производства искусственных мясопродуктов методом «мокрого» прядения и склеивания белковых волокон, а также путем получения пористых анизотропных студней, уже нашедшие широкое промышленное применение, рассмотрены в гл. IV.)
Получение анизотропных студней путем деформации двухфазных систем и их перевода в студнеобразное состояние
Выше показана принципиальная возможность фиксации формы деформированных в потоке частиц дисперсной фазы двухфазных жидких систем переводом в студнеобразное состояние дисперсной фазы, дисперсионной среды или обеих фаз системы. В связи с этим возникает возможность получения анизотропных материалов трех видов [2]: а) коротких волокон, войлока и нетканых материалов при переводе в студнеобразное состояние дисперсной фазы в потоке; б) анизотропных студней капиллярной структуры, т. е. студней, наполненных жидкими ориентированными анизодиаметричными каплями (жидкими цилиндрами), при переводе в потоке в студнеобразное состояние дисперсионной среды и, наконец, в) анизотропных студней, наполненных ориентированными волокнами, при переводе в студнеобразное состояние обеих фаз системы в потоке (см. рис. 9).
С точки зрения рассматриваемой проблемы наибольший интерес представляет переработка жидких двухфазных систем, содержащих белки. Перевод одной или обеих фаз системы в студнеобразное состояние может быть осуществлен либо в результате изменения температуры (тепловая денатурация белка, студнеоб-разование желатины, а также крахмала и других полисахаридов), солевого состава среды, рН, либо добавлением денатурирующих или сшивающих агентов. Можно также использовать явление денатурации белков па границе раздела фаз. Например, яичпый альбумин легко образует волокна при эмульгировании и переме-
Физико-химические основы переработки белкав ЙПИ У1
шивании его водного раствора в масле или другой органической
жидкости.
Процесс образования и свойства анизотропных студней капиллярной структуры были исследованы на примере системы желатина—декстран—вода [62, 72]. Дисперсная фаза была обогащена декстраном, а дисперсионная среда — желатиной. Частицы
| 1'ис. 20. Зависимость степени асимметрии (Р) дисперсных частиц от скорости сдвига (д) в студнях капиллярной структуры |
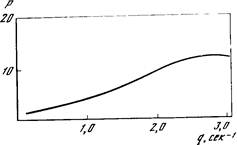
дисперсной фазы имели диаметр около 5-10~3 см, отношение объемов фаз составляло 1:1. Фиксацию формы деформированных в потоке жидких частиц дисперсной фазы (фаза декстрана) осуществляли за счет перевода дисперсионной среды (фаза желатины) в студнеобразное состояние за счет охлаждения системы. В качестве характеристики механических свойств студней использовали величину максимального усилия при пенетрации образца анизодиаметричным индентором, который представлял собой пластинку прямоугольного сечения. Индентор располагали вдоль и поперек направления ориентации частиц дисперсной фазы.
Структура капиллярных студней в значительной мере определялась величиной скорости сдвига. По мере ее возрастания степень асимметрии дисперсных частиц увеличивалась (рис. 20). Деформированные капли уже при малых скоростях сдвига ориентируются по направлению сдвига. Увеличение скорости сдвига, равно как и остановка потока, нарушает стабильность деформированных капель и приводит к их распаду.
Студни капиллярной структуры обладают анизотропией прочности. Прочность студня в поперечном направлении (относительно направления ориентации капилляров) выше, чем в продольном, и повышается с увеличением степени асимметрии частиц (рис. 21). Прочность в продольном направлении при этом падает, что приводит к существенному возрастанию отношения указанных величин, выбранного в качестве характеристики анизотропии прочности студня. На рис. 22 показана зависимость этой величины от степени асимметрии частиц дисперсной фазы. Увеличение прочности студня в поперечном направлении с возрастанием скорости сдвига может быть связано с уменьшением попе-
| Глава вторая |
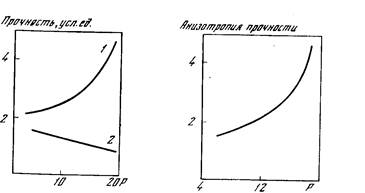
Рис. 21. Зависимость прочности (усилие внедрения индентора) студня капиллярной структуры от степени асимметрии дисперсных частиц
Индентор ориентирован перпендикулярно (J) и параллельно (2) направлению ориентации дисперсных частиц,
Рис. 22. Зависимость анизотропии механических свойств студней капиллярной структуры от степени асимметрии частиц дисперсной фазы
речного размера капель по мере роста степени их асимметрии. Это предположение согласуется с результатами исследования зависимости механических свойств студней желатины от размера наполняющих их сферических капель декстрана [171].
Таким образом, уже при средней степени наполнения (объемная доля дисперсной фазы 50%) анизотропная структура капиллярных студней обеспечивает заметную анизотропию механических свойств, что существенно для получения искусственных мясопродуктов. При более высоких степенях наполнения студня деформированными каплями (жидкими цилиндрами) расположенные между ними элементы непрерывной фазы студня представляют собой макроскопические волокна. Такие студни по внешнему виду и консистенции хорошо имитируют мясопродукты.
Двухфазный характер жидких водных систем, содержащих практически важные белки (см. табл. 9), позволяет перерабатывать их в искусственные мясопродукты по различным вариантам схемы, приведенной на рис. 9 (см. стр. 58).
Так, для получения волокон или же анизотропных студней, наполненных волокнами, могут быть использованы два вида систем, содержащих, например, белки и кислые полисахариды. В первом случае фаза, обогащенная полисахаридом, не образует студня в условиях студнеобразования второй, белковой, фазы. Здесь можно использовать системы, содержащие белок (казеин, белок соевых бобов и др.) и гуммиарабик, так как последний не коагулирует и не образует студни, например в присутствии
Физико-химические основы переработки белка вЙ1Ш^3
солей кальция. Во втором случае, при получении белковых студней, наполненных полисахаридными волокнами, можно использовать, в частности, системы, содержащие те же белки и альги-нат натрия, так как в этом случае обе фазы системы переходят в студнеобразное состояние в присутствии солей кальция, т. е. в одних и тех же условиях. Фазовые диаграммы систем казеин— альгинат натрия—вода и казеин—гуммиарабик—вода приведены па рис. 3, а и б (см. стр. 50).
Для/ получения анизотропного студня на основе казеина используют двухфазную систему казеин—альгинат натрия—вода, которую готовят растворением в 0,1 М растворе NaOH казеина (10%) и альгината натрия (1%). Фазы равновесного состава разделяют центрифугированием, затем повторно смешивают для получения двухфазной системы с дисперсной фазой, обогащенной альгинатом натрия. На рис. 23 показана микрофотография такой двухфазной системы с объемной долей дисперсной фазы 30% и средним размером дисперсных частиц капель 20 мкм', рН 8,0. Дисперсные частицы системы легко деформируются между предметным и покровным стеклами микроскопа при их относительном перемещении, вытягиваясь в тонкие нити (жидкие цилиндры) (рис. 24). После снятия напряжения дисперсные частицы медленно релаксируют, принимая через 20—30 мин. сферическую форму. Если такую двухфазную систему вылить струёй в раствор хлористого кальция, перемешиваемый цилиндрическим ротором в сосуде цилиндрической формы, то струя жидкой системы переходит в студнеобразное состояние в потоке и принимается (наматывается) на ротор. Конечный продукт представляет собой анизотропный студень казеината кальция, наполненный волокнами альгината кальция. Он имеет ярко выраженную волокнистую макроструктуру и при небольшой вытяжке (15—20%) легко расщепляется на макроскопические волокна или пучки волокон (рис. 25). Легкость расщепления студня обусловлена слабой адгезией и заметным различием модулей упругости студней альгината и казеината кальция. По макроструктуре продукт имитирует традиционные мясопродукты. Описанный процесс, очевидно, может быть осуществлен непрерывно и не требует сложного оборудования. Он может быть использован для получения как объемных анизотропных студней, так и пленок, и волокон.
Аналогичным образом можно получить казеиновые волокна, с тем лишь отличием, что для получения двухфазной системы в 0,1 М растворе NaOH растворяют казеин (14%) и гуммиарабик (4%). В качестве коагуляционной ванны используют тот же раствор хлористого кальция. В результате получают короткие тонкие волокна казеина в виде войлока, который может быть пропитан пищевым связующим и переработан в искусственные мясопродукты с помощью известных методов (см. гл. IV).
| Глава вторая |

а^ги^т^р^^Йда^зЙ83^ жидкой системы казеин (10%) -РН 8,0; средний размер капель 20 мкм

Рис_ 24. Микрофотография двухфазной системы казеин - альгинат натрия-вода, деформированной между предметными стеклами микроскопа при их относительном перемещении. 800Х микроскопа
Средняя величина диаметра дисперсных частиц 3—4 мкм
Физико-химические основы переработки белка в ИПП 95

Рис. 25. Микрофотография разрушенного при деформации студня казеина, наполненного волокнами альгината кальция. ЗООХ
Средний диаметр волокон 3мкм.
Естественно, что, не будучи подвергнуты ориентационной вытяжке и интенсивному дублению, такие волокна обладают несравненно более низкими механическими свойствами, чем текстильные белковые волокна. Это, однако, относится к большинству волокон, перерабатываемых в искусственные мясопродукты. Основную роль здесь играют сравнительно высокая степень анизотропии студня и различие в модулях упругости и прочности студня и наполняющих его волокон, что обусловливает легкость расщепления и ощущение неоднородности продукта при его пережевывании, что характерно для мясопродуктов. Описанные методы получения волокон и анизотропных студней более просты, чем обычные методы мокрого прядения волокон и их склеивания (см. гл. IV). Они могут быть также использованы для получения волокон и волокнистых материалов, применяемых в тех областях техники, где требования к механическим свойствам волокон сравнительно невысоки (сорбенты, звуко- и теплоизоляционные материалы и т. п.).
Таким образом, все три варианта переработки белков в виде двухфазных жидких систем, описанные выше (см. рис. 9), могут найти практическое применение при получении искусственных
96 Глава вторая
мясопродуктов. Отметим, что фиксация дисперсных частиц жидких двухфазных систем в потоке возможна при переводе системы не только в студнеобразное, но и в стеклообразное или кристаллическое состояние. Последний вариант имеет большое значение для получения технических материалов переработкой смесей полимеров через растворы или расплавы. В его изучении большого успеха добились Виноградов и сотр. [186—189]. В последние годы переработка смесей полимеров интенсивно исследуется в связи с проблемами получения ударопрочных пластиков, «фиб-риллизующихся» пленок, нетканых материалов ит.п.[186—194].
Ионотропные студни
Растворы многих полиэлектролитов способны образовывать анизотропные студни при диффузии в них ионов поливалентных металлов, точнее, ионов с координационным числом больше единицы. Впервые условия получения, структуру и свойства таких студней исследовал X. Тиле. Поскольку в этом случае переход в студнеобразное состояние вызывается ионами, Тиле предложил называть это явление «ионотропией», а студни «ионотропными».
Ионотропные студни могут быть получены при диффузии противоионов — осадителей в растворы заряженных коллоидных частиц, а также в растворы полиэлектролитов, таких, как поли-акриловая или полиметакриловая кислота, производные целлюлозы с ионогенными группами, другие кислые полисахариды и т. п. [195—203 ]. Основные исследования по ионотропии были выполнены на растворах биополимерных полиэлектролитов, прежде всего альгината натрия. Эти работы были начаты X. Тиле в 1947 г. и их результаты суммированы в монографии [204].
Основное направление исследований Тиле и его сотрудников в области ионотропных студней было связано с моделированием структуры и свойств биологических тканей, прежде всего соединительных тканей, а также внутриклеточных и межклеточных структурных образований [199, 204—210]. Тиле отмечал повышенное содержание полиэлектролитов в молодых и растущих тканях. Он также подчеркивал, что Ионотропные студни образуются в физиологических условиях, при комнатной температуре, могут содержать практически любые полиэлектролиты, обладают двулучепреломлением, способностью к обратимому набуханию и ионному обмену. По мнению Тиле, основной механизм структуро-образования в биологических системах заключается в направленной коагуляции биополимеров под действием ионов.
Исследования по ионотропии имеют и практическое значение. Так, предложены способы получения мембран для ультрафильтрации, стерилизации и ионного обмена на основе ионотропных студней альгината кальция, а также способ получения ультра-
Физико-химические основы переработки белка в ППП 97
тонкой проволоки с использованием ионотропных студней капиллярной структуры [199, 211—213].
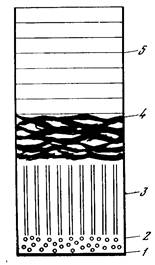
|
Уже в первых работах Тиле показал, что ионотропные студни имеют ориентированную структуру и обладают оптической анизотропией. В ионотропных студнях молекулы полиэлектролита или заряженные коллоидные частицы ориентированы перпендикулярно направлению диффузии [197, 198, 204]. Ориентированную структуру ионотропных студней подтвердили затем Стирлинг, Хайден и Кларе с сотр. [200—203, 214, 215]. О степени ориентации элементов структуры ионотропных студней Тиле судил по величине двулучепреломления образцов. Он считает, что механизм ориентации макромолекул полиэлектролитов при образовании таких студней состоит в том, что заряженные асимметричные частицы ориентируются параллельно границе раздела раствор низкомолекулярного электролита — раствор полиэлектролита в поле диффузионного потенциала. Тиле удалось показать, что степень ориентации макромолекул в ионотропном студне возрастает пропорционально диффузионному потенциалу.
| Рис. 26. Схема расположения структурных зон в ионотропном студне 1 — зона мембран; 2 — зона капельного расслоения; 3 — зона капилляров; 4 — зона линз; 5 — зона полос |
Ионы металла в ионотропном студне могут быть заменены на протоны при выдерживании студня в растворе какой-либо кислоты без изменения его структуры. Протоны, в свою очередь, могут быть заменены на ионы металла, и такая замена может производиться многократно. При этом степень ориентации элементов структуры студня возрастает. Этот процесс Тиле назвал ионными волнами [216]. Объем ионотропного студня после 10 ионных волн может быть уменьшен на 25%. Если подобной операции подвергнуть образец ионотропного студня в форме куба, то наблюдают анизотропную контракцию. Ионотропные студни набухают и могут быть растворены в растворах солей щелочноземельных металлов, а также набухают и могут быть растворены в разбавленных растворах NaOH [204].
Интересные результаты получены при исследовании макроструктуры ионотропных студней (на уровне оптического микроскопа) . При диффузии противоионов в раствор полиэлектролита
4 В. Б. Толстогузов
98 Глава вторая
в направлении снизу—вверх наблюдается образование пяти последовательно расположенных структурных зон (рис. 26) [199, 204].
Плотная первичная мембрана состоит из макромолекул» ориентированных перпендикулярно направлению диффузии. Ее толщина составляет около 1 мкм (для системы альгинат натрия— нитрат меди). Мембрана имеет поры диаметром порядка 5 нм.
За двулучепреломляющей мембраной следует зона капельного расслоения толщиной 3—5 мкм. (для указанной выше системы). В этой зоне студня видны мелкие капли водной фазы, образованные в результате дегидратации полиэлектролита. В конце зоны наблюдаются более крупные капли, возникшие за счет коалес-ценции мелких капель благодаря снижению скорости диффузии противоионов через слой образовавшегося студня.
Дальнейшее снижение скорости диффузии противоионов, согласно Типе, приводит к тому, что капли новой фазы имеют возможность коалесцировать в направлении диффузии и образовывать капилляры. Поэтому следом за зоной капельного расслоения в ионотропном студне расположена зона капилляров. Последние представляют собой однородные по диаметру трубки, расположенные параллельно направлению диффузии и расширяющиеся в этом направлении. Они заполнены раствором электролита. Доля объема, занятого полостями капилляров, может достигать 0,996-Диаметр капилляров составляет от 8 до 350 мкм, длина — от нескольких миллиметров до десятков сантиметров, в зависимости от состава системы и условий получения ионотропного студня. Показано, что диаметр капилляров тем больше, аих число на единицу площади поперечного сечения студня тем меньше, чем слабее противоион связывается с полиэлектролитом. Если для получения ионотропного студня используют смесь солей, то его структура определяется тем ионом, который сам по себе обеспечивает образование капилляров большего диаметра, например ионом кальция в присутствии иона меди. Это явление объяснено различием скоростей диффузии противоионов, в разной мере связываемых полиэлектролитом: ионы меди, сильнее взаимодействующие с альгинатом, движутся медленнее ионов кальция, задающих структуру ионотропного студня, затем, однако, ионы кальция вытесняются ионами меди в результате ионного обмена.
Ряды противоионов, отвечающие увеличению диаметра капилляров, приведены в работах [204, 217, 218]. При снижении концентрации низкомолекулярного электролита существенную роль начинает играть и природа аниона. Влияние природы соли на параметры капилляров сильно зависит от условий эксперимента;
возможно, что поэтому сведения о влиянии природы катионов и анионов весьма противоречивы.
Физико-химические основы переработки белка вЙПП 99
При увеличении концентрации полиэлектролита диаметр капилляров снижается, и в случае альгината натрия последние не образуются при концентрации выше 5%. Добавление в раствор полиэлектролита неэлектролитов, а также поверхностно-активных веществ не сказывается заметным образом на структуре капилляров [217].
Поскольку при получении ионотропных студней наблюдается заметная контракция, тем большая, чем ниже исходная Концентрация полиэлектролита, Типе [218] объяснил наблюдаемое расширение капилляров в направлении диффузии разбавлением раствора полиэлектролита по мере его перехода в студнеобразное состояние за счет воды дегидратации.
Установлено, что длина образца ионотропного студня пропорциональна корню квадратному из продолжительности диффузии. Показано также, что при восходящей диффузии противоионов в раствор полиэлектролита капилляры обрываются на определенной высоте, тогда как при нисходящей диффузии они пронизывают весь образец студня. Это различие объяснено тем, что в последнем случае на диффузионной границе за счет конвекции поддерживается постоянная и достаточно высокая концентрация противоионов. Очевидно, что это условие может выполняться только в том случае, если плотность раствора низкомолекулярного электролита выше плотности раствора полиэлектролита, что имело место в экспериментах Типе.
Обрыв зоны капилляров при восходящей диффузии ионов Типе связывал с замедлением диффузии ионов до определенной величины в результате утолщения слоя студня. Капли дегидра-тационной воды могут при этом коалесцировать и достигать большего размера. Крупные капли раствора электролита образуют «линзы», чередующиеся с пучками волокон. Ионотропный студень приобретает пористую структуру. Эту структурную зону Типе назвал зоной линз. Дальнейшее замедление диффузии ионов приводит к тому, что капли раствора электролита сливаются в слои. Ионотропный студень приобретает «полосатую» структуру (см. рис. 26).
Условия образования зоны линз и полос в ионотропных студнях были исследованы на примере студней альгината кальция, полученных диффузией уксуснокислого кальция в раствор альгината натрия [219—221 ]. В этих условиях, как показали Типе и Халих, зона линз и полос занимает большую часть образца. Методика получения студней весьма проста. Оптическую кювету (с плоскопараллельными или цилиндрическими стенками) доверху заполняли водным раствором альгината натрия, накладывали на поверхность раствора фильтровальную бумагу, смоченную водным раствором уксуснокислого кальция (10%), и быстро погружали кювету открытым концом вниз в стакан с тем же
А*
| Глава вторая |

|
Рис. 27. Микрофотография студня альгината кальция в скрещенных николях. Образцы получены путем диффузии 10%-пого раствора уксуснокислого кальция в 2%-ный раствор альгината натрия в направлении снизу вверх
о — структура типа «полос»;
б — структура типа «линз»
раствором соли кальция. При наложении фильтровальной бумаги происходило мгновенное образование пленки студня на поверхности раствора альгината натрия, что обеспечивало в дальнейшем хорошее качество диффузионной границы. Диффузия длилась 10—15 час. Длина возникающего при этом студня составляла 14—18 мм.
Полученные студни обладали значительным двулучепрсломле-нием по всей длине образца. Для микроскопической картины характерна поперечная исчерченность, проявляющаяся либо в наличии перпендикулярных направлению диффузии эквидистантных полос толщиной порядка 10 мкм, либо большого числа искривленных более тонких полос, преимущественно ориентированных под небольшими углами к фронту диффузии (рис. 27). Поперечная исчерченность наблюдалась не по всей длине образца студня. Она начиналась на расстоянии 1—3 мм от диффузионной границы. Начальная зона студня (1—3 мм) состояла из зон мембраны, капельного расслоения и капилляров. Длина зоны студня с поперечной исчерченностью составляла 7—9 мм. Конечная зона (5—6 мм) представляла собой однородный студень. Характер микроскопической картины (полосы, линзы или же отсутствие обоих видов поперечной исчерченности) меняется от одного образца к другому в зависимости от ряда параметров. Среди них хорошо воспроизводимыми оказались зависимости от размеров кюветы, начальной концентрации альгината натрия и направления диффузионного потока относительно поля тяготения.
Слои с четкой «полосатой» структурой образуются лишь в кюветах диаметром (толщиной) не более 2,2 мм, при начальной
Физико-химические основы переработки белкав ИПП 101
концентрации альгината 1,0—2,5%. В указанных условиях период идентичности элементов структуры студня составляет от 0,04 до 0,10 мм (рис. 27, а), причем можно отметить тенденцию к уменьшению периода идентичности при возрастании диаметра кюветы. При дальнейшем увеличение диаметра кюветы и начальной концентрации альгината наблюдалось все возрастающее искривление полос (см. рис. 27, б). Иопотропные студни с более или менее совершенной поперечной исчсрчеппостыо образуются в кюветах, расположенных под углами от 0 до 8° относительно вертикали при направлении диффузия снизу вверх. При большем отклонении от вертикали возникают студни, лишенные поперечной псчерченности, с преобладающей капиллярной структурой. Полученные данные по влиянию направления диффузионного потока на структуру ионотропных студней подтверждают представления Тиле об отрицательной роли конвективного смешения при получении студней с преобладающей поперечной исчерчен-постыо.
В процессе образования ионотропного студня с поперечной исчерченностью отчетливо наблюдается концентрирование студне-образователя в зоне поперечной исчерченности, тогда как для последующей зоны макроскопически однородного образца студня характерно понижение концентрации студнеобразователя. Очевидно, что возникновение слоистых структур в студне сопряжено с процессами синерезиса. При диффузии соли кальция в направлении сверху вниз, т. е. при образовании студня с преимущественно капиллярной структурой, сохраняется практически равномерное распределение студнеобразователя по высоте студня.
Установлено также, что студни альгината кальция, полученные при диффузии кальция снизу вверх, претерпевают резкие изменения в результате медленного замораживания. После оттаивания, сопровождающегося отделением жидкости, прежде макроскопически однородный студень приобретает ярко выраженную слоистую структуру. Он представляет собой стопку тонких (0,1— 0,5 мм), местами сросшихся слоев студня, расположенных перпендикулярно направлению диффузии. Эти слои могут быть легко отделены друг от друга. Следует отметить, что резкое охлаждение, например в жидком азоте, не приводит к такому результату. Можно полагать, что способность студней к расслаиванию обусловлена их слоистой структурой, а замораживание играет роль проявителя этой структуры. Причиной расслаивания является расширение при замораживании зон с повышенным содержанием воды, расположенных между слоями альгината кальция. Поэтому стеклование этих зон при резком охлаждении студня в жидком азоте не приводит к расслаиванию студня.
Исследование ползучести ионотропного студня альгината кальция слоистой структуры показало, что податливость студней в
102 Глава вторая
| Риг,. 28. Ползучесть О^ч/о-ного студня альгината кальция в направлении, параллельном (1) и перпендикулярном (2) направлению диф-фу.чип ионов кальция |
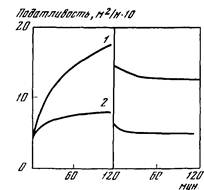
направлении диффузии намного выше, чем в перпендикулярном направлении (рис. 28). В обоих случаях модуль упругости сгуд-ней пропорционален концентрации альгината [222]. Анизотропия механических свойств студней альгината кальция, очевидно, обусловлена анизотропией его макроструктуры. Слоистая структура студня с макроскопическими слоями, ориентированными перпендикулярно направлению движения ионов кальция и разъединенными зонами с высоким содержанием воды, приводит к тому, что их деформация оказывается частично необратимой. Развитию остаточной деформации при одноосном сжатии в направлении, параллельном диффузии ионов кальция, т. е. перпендикулярном плоскости слоев, способствует перемещение слабосвязанных элементов структуры и макрослоев студня, сопровождаемое выдавливанием воды. Это, естественно, проявляется в анизотропии пластичности студня. Отметим, что после замораживания и оттаивания слоистого студня альгината кальция, как показано выше, происходит распад сплошного образца студня на стопку слоев с отделением водной фазы под действием собственного веса образца. При этом наблюдается сокращение размера образца в том же направлении, что и при исследовании его ползучести, а именно, в направлении диффузии ионов кальция при получении первоначального образца иопотропного студня.
Таким образом, ионотропные студни альгината кальция слоистой структуры обладают анизотропией механических свойств и образуются в условиях, исключающих конвекционное смешение раствора соли кальция с раствором альгината натрия, т. е. при диффузии ионов кальция в направлении снизу вверх. Образование слоистых студней сопровождается концентрированием полиэлектролита в направлении диффузионной границы. Замораживание и оттаивание таких студней приводит ких расслоению.
Смешанные студни желатины и альгината кальция, получаемые диффузией ионов кальция в студни желатины, содержащие
Физико-химические основы переработки белка в ИПП 103
альгинат натрия, также обладают анизотропией механических свойств [180]. Однако в отличие от студней альгината кальция смешанные студни проявляют большую податливость в направлении, перпендикулярном диффузии ионов кальция. Приведенные па рис. 12—15 термомеханические кривые и кривые ползучести характеризуют свойства смешанных студней в направлении, параллельном диффузии ионов кальция. В отличттс от студией аль-гипата-.калт.ция студни пектината кальция, т. о. полиэлектролита с меньшей плотностью заряда, не обнаруживают заметной ани-яотропии механических свойств [223].
Несмотря на успехи, достигнутые в изучении условий образования и структуры ионотропных студней, даже в феноменологии этого явления многое остается неясным, не говоря уже об отсутствии ясного понимания природы явления. Образование слоистой структуры студней, по-видимому, можно рассматривать как результат некоего периодического процесса, ведущего к фазовому расслоению и нарушению градиента концентрации диффундирую-щего катиона. Высказывалось мнение [220] о связи этого явления с явлением образования колец Лизеганга, против чего возражает Типе [204]. Электронно-микроскопическое исследование различных структурных зон в ионотропных студнях альгината кальция [224, 225] не обнаружило ориентации макромолекул альгината в направлении, перпендикулярном направлению диффузии. Этот результат не согласуется с более ранними данными [226, 227] и требует внимательного рассмотрения.
Мало изучен также вопрос о связи между молекулярными характеристиками полиэлектролитов и структурой ионотропных студней. Согласно Тиле [204], степень ориентации макроионов в ионотропных студнях снижается при уменьшении заряда макроиона. Степень ориентации уменьшается также по мере снижения молекулярного веса полиэлектролита, и ниже некоторого порогового значения молекулярного веса ионотропные студни вообще не образуются. Отмечается, что для получения воспроизводимых результатов необходимо использовать один и тот же образец альгината [217].
Интересные данные о зависимости структуры иопотропных студией альгипата цинка от источника полисахарида получены Паардсетом [228]. Оказалось, что количество и форма капилляров зависят от вида и возраста водоросли, а также части растения, из которой выделен альгинат, и могут служить характеристическими признаками альгинатов, полученных из различных источников.
Одним из важных факторов, определяющих структуру ионо-троппьтх студней, является сополимерпый состав альгинатов. Исследования Хауга, Смидсреда, Кона и др. [229—231] показали, что остатки гулуроновой кислоты в макромолекуле альгината име-
| Глава вторая |
ют большее сродство к ионам кальция, меди и ряда других металлов, чем остатки маннуроновой кислоты. Согласно [232—235], образование трехмерной сетки студня альгината кальция включает кооперативное межмолекулярное связывание ионов кальция блоками остатков гулуроновой кислоты. Сополимерный состав в значительной мере определяет способность альгинатов к студне-образованию [230, 236, 237 ], а также механические и физико-химические свойства студней альгината кальция [238]. При исследовании влияния сополиморного состава альгинатов на структуру ионотропных студней было показано [22], что по мере снижения содержания гулуроновой кислоты диаметр капилляров в студнях альгината меди и альгината кальция возрастает, а их количество уменьшается. В этом же направлении ухудшается качество слоистой структуры студней [22]. В то же время различия в структуре наблюдаются и для образцов, имеющих одинаковый Сополимерный состав. Это свидетельствует о том, что последний не является единственным фактором, определяющим характер ио-нотропной структуры. В~качестве других молекулярных характеристик, возможно играющих роль в формировании структуры ионотропных студней, можно указать распределение остатков маннуроновой и гулуроновой кислот по структурным блокам, распределение блоков по размерам, а также молекулярный вес и мо-лекулярно-весовое распределение альгинатов.
С точки зрения проблемы переработки белка ионотропные студни слоистой структуры представляют определенный практический интерес при получении различных форм искусственной пищи [1, 2]. Поверхность слоев, получаемых в результате замораживания и оттаивания таких студней, имеет волокнистую макроструктуру, представляющую собой отпечатки анизодиамет-ричных кристалликов льда. Пропитка таких слоев связующим, содержащим белки, денатурирующие при нагреве, и последующий нагрев системы приводят к получению продуктов, имитирующих мясные изделия. Белки и другие пищевые вещества могут быть введены не только в состав связующего, но и в состав слоистых элементов структуры. Например, белки могут быть использованы для получения слоев в виде заряженных комплексов с кислыми полисахаридами. Процесс диффузии ионов кальция при получении объемных студней слоистой структуры можно ускорит!, с помощью электрического поля. Поскольку требования к механическим свойствам связующего значительно ниже при склеивании слоев — двумерных структурных элементов, чем при склеивании волокон как одномерных элементов структуры, такой прием получения искусственных мясопродуктов отличается большей «универсальностью по белку». Существенно также то обстоятельство, что студни альгината кальция устойчивы к нагреву. Это расширяет возможность использования приема склеивания тон-
Физико-химические основы переработки белка вИПП 105
ких слоев волокнистой макроструктуры при получении искусственных мясопродуктов, подвергаемых различным видам кулинарной обработки.
О ЗНАЧЕНИИ ИССЛЕДОВАНИЙ ПРОЦЕССОВ ПЕРЕРАБОТКИ БЕЛКА В ИСКУССТВЕННЫЕ ПРОДУКТЫ ПИТАНИЯ
В предыдущих разделах рассмотрены результаты физико-химических исследований жидких и студнеобразных многокомпонентных водных систем, содержащих белки, выполненных с целью развития общего подхода к проблеме переработки белка в искусственные продукты питания. Эти исследования позволили выявить особенности поведения белков при их переработке в искусственные пищевые продукты, а также наметить ряд путей получения новых форм пищи. При этом показано, что решающее значение для проблемы переработки белка в искусственные продукты имеет изучение взаимодействия и совместимости белков и полисаха-ридов в водных средах, а также условий получения и свойств наполненных, смешанных, комплексных и анизотропных студней. Г)то положение продемонстрировано на примерах регулирования состава и свойств белоксодержащих систем и переработки белка в искусственную зернистую икру, искусственные макаронные изделия, мясопродукты и т. д. [1, 2, 120, 167, 168, 172, 173].
Здесь необходимо отметить, что исследования в области физико-химических аспектов получения искусственных продуктов питания имеют также существенное значение для ряда других областей науки и техники. Результаты этих исследований позволяют, в частности, наметить пути совершенствования традиционных процессов пищевой технологии и комплексной переработки различных видов пищевого сырья. Известно, например, что условия формования традиционных пищевых систем существенно влияют на макроструктуру и свойства конечных изделий. Учет этого обстоятельства особенно важен, поскольку перерабатываемое пищевое сырье обычно имеет многокомпонентный и гетерофазный характер. В связи с этим важное прикладное значение имеет изучение жидких и студнеобразных пищевых систем, моделирующих традиционные пищевые системы по структуре и составу. Например, изучение поведения в потоке двухфазных жидких систем имеет прямое отношение к процессам образования волокнистой структуры таких традиционных продуктов, как, в частности, халва, карамель и др.
С другой стороны, принимая во внимание тот факт, что традиционные продукты обычно невоспроизводимы по составу и структуре, причем их состав с трудом поддается регулированию,
106 Глава вторая
представляется весьма перспективным исследование модельных искусственных продуктов питания с заданным и хорошо воспроизводимым составом. Здесь возникает возможность получения более достоверных сведений о поведении отдельных компонентов пищи при переработке, хранении и кулинарной обработке, их атакуемости ферментами желудочно-кишечного тракта, роли ферментных и иммунных систем в процессах изменения состава, свойств и качества пищи при ее хранении, переработке и т. д.
Можно привести множество других возможных примеров применения результатов исследования в области переработки белков для совершенствования традиционной пищевой технологии. Ограничимся лишь несколькими. Так, обнаруженный эффект регулирования растворимости глобулинов и глютелинов за счет получения их комплексов с кислыми полисахаридами, а также возможность модифицирования физико-химических свойств растворов и студней, содержащих эти белки, позволяют использовать указанные комплексы для извлечения и переработки белков в мягких условиях, а также для обогащения и регулирования свойств традиционных пищевых продуктов. Например, образование комплексов кислых полисахаридов с клейковиной пшеницы открывает возможность регулирования реологических свойств изделий из теста [123, 172 ]. Отметим также, что процессы взаимодействия белок—кислый полисахарид, лежащие в основе комплексной коацервации, с недавнего времени нашли применение для микроинкапсулирования ароматических, вкусовых, пищевых и других веществ. Этот же процесс может быть использован для иммобилизации ферментов [118, 126].
Исследование взаимодействия природных макромолекул с образованием комплексов в жидком и студнеобразном состояниях имеет также непосредственное отношение к изучению сложных биологических систем. Взаимодействие белков и кислых полисахаридов и комплексная коацервация широко исследуются в связи с моделированием ряда биологических процессов и предполагаемой ролью коацерватов в абиогенезе [80—83]. Исследование студнеобразного состояния, в свою очередь, представляет собой одну из центральных проблем физико-химии полимеров и физико-химической биологии [34, 38]. Результаты этих исследований могут найти применение и для решения ряда задач медицины.
В свою очередь, возможность переработки двухфазных систем в волокна, анизотропные студни капиллярной структуры и студни, наполненные или армированные волокнами, представляет интерес для ряда областей техники, прежде всего для производства волокон, нетканых и армированных материалов, сорбентов и т. д.
Таким образом, изучение многокомпонентных водных систем, содержащих белки и полисахариды, имеет, с одной стороны, самостоятельный научный и практический интерес, в частности для
Физико-химические основы переработки белка в ИПП 107
решения ряда задач физической химии растворов полимеров, пи-шовых и биологических систем, а с другой — открывает возможность использования белков из нетрадиционных источников для питания путем их переработки в искусственные продукты. Эта область физико-химических исследований находится в стадии становления и в основном ограничена феноменологическим уровнем. Она, однако, будет играть все возрастающую роль в развитии производства искусственных продуктов питания — нового вида крупнотоннажного производства.
ЛИТЕРАТУРА
1. W. В. ГоЫоувхо ю.—Nahrung,18, N 5, 523 (1974).
2. W. B. Tolstogasow, E. E. Braado, E. S. Wainerman.— Nahrung,19, N 9/10, 973 (1975).
3. А. А. Покровский— ЖВХО,10, № 3, 247 (1965).
4. Б. А. Николаев. Измерение структурно-механических свойств пищевых продуктов. М., «Экономика», 1964.
5. С. А. Матц. Структура и консистенция пищевых продуктов. М., «Пищевая промышленность», 1972.
6. E. E. Braado, D. B. Isjumow, W. B. Tolstogusow.—fiahruag,17, N 8, 773 (1973).
7. E. E. Braado, D. B. Isjumow, W. B. Tolstogasow, E. S. Wainerman.—Nahrung, 18, N 1, 1 (1974).
8. E. E. Braado, E. A. Nikitina, W. B. Tolstogasow.— Z. phys. Chem.,253,N 5/6, 300 (1973); E. E. Браудо. В. Б. Толстогуаов, E. А. Никитина.— Коллоидн. ж., 36, № 2, 208 (1974).
9. E. E. Braudo, E. N. Michailow, W. B. Tolstogasow.—Z. phys. Chem.,253,N5/6,369 (1973).
10. В. Б. Толстогузов, E. С. Вайнерман.— Nahrung,19, N 2, 111 (1975).
11. E. E. Браудо, Д. Б. Изюмое, В. Б. Толстогузов, Д. П. Радкевич. Новые методы исследования физико-химических свойств и оценка качества желатины. М., ЦНИИТЭИ. Клеевая и желатиновая промышленность, 1972.
12. E. E. Браудо, И. Г. Плащина, Н. С. Кузьмина, В. Б. Толстогузов.— Коллоидн. ж., 36, Я» 1, 136 (1974).
13. Г. Л. Слонимский, В. Ф. Алексеев, В. Я. Гринберг и др.— Высокомол. соед., НА, №2, 460 (1969).
14. E. E. Браудо, В. Б. Толстогузов.— Высокомол. соед., 12А, № 2, 474 (1970).
15. E. П. Козьмина, В. Б. Толстогузов, Э. С. Бондарева.— Хранение и переработка зерна, ЦИНТИГоскомзаг. СССР, № 7, 23 (1968).
16. E. П. Козьмина, Ю. И. Чимиров, Д. Б. Изюмое, В. Б. Толстогузов.— Хлебопек. и кондитерск. пром., № 8, 20 (1973).
17. О. Г. Бровко, Д. Б. Изюмое, В. С. Грюнер, В.. Б. Толстогузов.— Труды Донецкого ин-та сов. торг., № 2, 30 (1972).
18. В. Б. Толстогузов, E. С. Вайнерман, Ж. Я. Чумак.— Изв. вузов. Пищевая технология, № 3, 170 (1975).
19. В. Б. Толстогузов, E. С. Вайнерман.— Изв. АН СССР. Серия хим., № 1, 198 (1973).
20. E. F. Titova, E. М. Belavtseva, E. E. Braudo, V. B. Tolstogazou.— Colloid and Polym. Sci„252, N 7, 497 (1974).
V. E. М. Велавцева, E. Ф. Титова, E. E. Браудо, В. Б. Толстогузов.—Биофизика, 18, № 5, 929 (1973);19, № 1, 19 (1974).
Глава вторая
22. В. Б. Толстогузов. Докт. дисс. М„ ИНЭОС АН СССР, 1975.
23. К. Ossima.— J. Agric. Chem. Soc., 7, 328 (1931).
24. К. Voit, H. Fridrich—Klin. Wochenschr.,14, 1792 (1935); С. А.,30, 3030 (1936).
25. Л. Hesp, B. Ramsbottom— Nature, 208, 1941 (1965).
26. A. Satton— Nature,216, 1005 (1967).
27. 3. В. Дубровина, М. Ю. Долматова, П. М. Малкин и др.— Гигиена и санитария,34, № 5, 105 (1969).
28. О. Д. Лившиц.— Вопросы питания, 28, № 4, 76 (1969).
29. М. Ю. Долматова, 3. В. Дубровина.— Гигиена и санитария, 35, № 3, 105 (1970).
30. Ч. Тенфорд. физическая химия полимеров. М., «Химия», 1965.
31. Р. Моравец. Макромолекулы в растворе. М., «Мир», 1967.
32. В. А. Каргин, Г. Л. Слонимский. Краткие очерки по физике-химии полимеров. М., «Химия», 1967.
33. А. Б. Зезин, В. Б. Рогачева.— В сб. «Успехи химии и физики полимеров». Под ред. 3. А. Роговина. М., «Химия», 1970.
34. С. П. Папков. физико-химические основы переработки растворов полимеров. М., «Химия», 1971.
35. H. G. Bungenherg de Jong. La coacervation, les coacervates et leur importance en biologic, I. Generalites et coacervates complex, II. Coacervates autocomplex. Paris, Hermann et Cie., 1936.
36. H. G. Bungenberg de Jong.—Koll.-Z., 79, 223 (1937);80, 221, 350 (1938).
37. С. П. Панков. Докт. дисс. М., НИФХИ им. Л. Я. Карпова, 1966.
38. С. П. Папков. Студнеобразное состояние полимеров. М., «Химия», 1974.
39. Р. J. Flory. Printiples of polymer chemistry, ch. 13. Ithaca. N. Y., Cornell Univ. Press, 1953.
40. G. L. Slonimskii—7. Polym. Sci.,30, 625 (1958).
41. D. J. Buchley.— Trans. N. Y. Acad. Sci.,29, N 6, 735 (1967).
42. L. Bohn— Rubber Chem. and Technol.,41, N 2, 495 (1968).
43. М. W. Beijerinck— Centrabl. BakterioL, Abt. 2, 2, 627, 698 (1896); Koll.-Z., 7, 16 (1910).
44. 0. Butschli.— Untersuch. Strukturen, 1898, 251.
45. Wo. Ostwald, R. H. Hertel— Koll.-Z., 47, 258, 357 (1929).
46. К. Doi— Biochim. et biophys. acta,94, 257 (1965).
47. В. Б. Толстогузов, В. Я. Гринберг, Л. И. Федотова.— Изв. АН СССР. Серия хим., № 12, 2839 (1969).
48. В. Б. Толстогузов, В. Я. Гринберг.— Изв. АН СССР. Серия хим., W 6, 1423 (1970).
49. В. Я. Гринберг, В. Б. Толстогузов, Г. Л. Слонимский.— Высокомол. соед 12А, 1593 (1970).
50. В. Я. Гринберг, К.-Д. Швенке, В. Б. Толстогузов.— Изв. АН СССР. Серия хим., № 6, 1430 (1970).
51. V. Ya. Grinberg, V. В. Tolstogasov.— Carbohydr. Res.,25, 313 (1972).
52. Ю. А. Антонов, В. Я. Гринберг, В. Б. Толстогузов.— Высокомол. соед., 18Б, № 8, 566 (1976).
53. Yu. Antonov, V. Ya. Grinberg, W. B. Tolslogusow.— Starke,27, N 12, 424 (1975).
54. Ya. A. Antonov, V. Ya. Grinberg, V. B. Tolstogasov.— Koll.-Z. und Z. Po-lym., 255, N 10, 937 (1977).
55. S. A. Rice, М. Nagasawa. Polyelectrolyte solutions. New York—London, Acad. Press, 1961, p. 178.
56. G. Ehrlich, P. Doty— J. Am. Chem. Soc., 76, 3764 (1954).
57. A. Veis.—]. Polym. Sci.,25, 113 (1957).
58. 0. Smithsred. Some physical propertis of alginates in solution and in the gel state. Rept 34. Norwegian Inst. Seaweed, 1973.
Физико-химические основы переработки белка в ИПП 109
59. /. N. Bemiller— In: «Industrial Gums». R. L. Whistler (Ed.). New York-London, Acad. Press, 1959, p. 643.
60. F. A. Bettelheim.— In: «Biological polyelectrolytes», v. 3. A. Veis, М. Dek-ker (Eds). N.Y., 1970, p. 143.
61. J. N. Bemiller— In: «Industrial gums». R. L. Whistler (Ed.). New York-London, Acad. Press, 1959, p. 214.
62. V. B. Tolstoguzov, A. I. Mzhel'sky, V. Ya. Gulov.— Colloid and Polym. Sci., 252,124 (1974).
63. G. }. Taylor.— Proc. Roy. Soc. London, A138, 47 (1932);A146, 501 (1934). R4. Эмульсии. Под ред. Ф. Шерман. Л., «Химия», 1972.
65. Л. Сег^, H. A. Scheraga— Chem. Rev.,51, 185 (1952).
66. W. Kuhn— Koll.-Z.,132, N 1—3, 84 (1953).
67. A. Silberberg, W. Kuhn.—l. Polym. Sci.,13, N 68, 21 (1954).
68. F. Rusheidt, S. G. Mason— J. Coll. Sci., 16, 238 (1961).
69. H. L. Doppert, W. S. Overdiep— Adv. Chem. Ser.,99, 53 (1971).
70. S. Tomotika— Proc. Roy. Soc. London, A150, 322, (1935); A153, 302 (1936.)
71. В. Я. Гулов. Канд. дисс. М., ИНЭОС АН СССР, 1974.
72. В. Б. Толстогузов, А. И. Мжелъский, В. Я. Гулов.— Высокомол. соед., 15Б,№ 11,824 (1973).
73. В. Б. Толстогузов, А. И. Мжелъский, В. Я. Гулов.— Зав. лаб.,39, № 7, 829 (1973).
74. H. Erbring.— Kolloidchem.-Beih.,44, 171 (1936).
75. W. Paali, F. Rona— Hofmeisters Beitr., 2, 1 (1902).
76. F. W. Tiebackx—Koll.-Z., 8, 198 (1910);9, 61 (1911).
77. K. Spiro.— Hofmeisters Beitr., 4, 300 (1904).
78. H. G. Bangenberg de Jong.— In: «Colloid science», v. 2, ch. 8—9. H. R. Kruyt (Ed.). New York — Amsterdam, Elsevier, 1949.
79. H. L. Booij, H. G. Bungenberg de Jong. Biocolloids and their interactions. Protoplasmologia. Wien, Springer Verl., 1956.
80. А. И. Опарин,— Природа, № 4, 3 (1952).
81. А. И. Опарин. Жизнь, ее природа, происхождение и развитие. М., Изд-во АН СССР, 1960.
82. Т. H. Евреинова. Концентрирование веществ и действие ферментов в коацерватах.М., «Наука», 1956.
83. К. Б. Серебровская. Коацерваты и протоплазма. М., «Наука», 1971.
84. /. Th. G. Overbeek, М. I. Voorn.— J. Cell. and Compar. Physiol., 49, Siippl. 1,1,7 (1957).
85. М. I. Voorn— Rec. trav. chim.,75, 317, 405, 427, 925, 1021 (1956).
86. A. Veis.—In: «Biological polyelectrolytes», A. Veis (Ed.). Now York— Amsterdam, Elsevier, 1970, p. 211.
87. A. Veis, C. Aranyi.— J. Phys. Chem., 64, 1203 (1960).
88. A. Veis.—i. Phys. Chem., 65, 1798 (1961); 67, 1960 (1963).
89. A. Veis, E. Bodor.— In: «Structure and function of connective and skeletal tussue». London, S. Fitton-Jackson, 1965, p. 228.
90. H. I. Bixler, A. S. Michaels.— In: «Encyclopedia of polymer science and t.rchnology», v. 10. New York—London—Sydney. Intersci. Publ. a division of J. Willey and Sons, 196ft, p. 765.
ill. H. Rufiak.— Bull. Soc. chim. biol,,32, 703 (1950).
92. J. G. Bungenberg de Jong, W. A. L. Dekker.— Kolloidchem.-Beih., 43, 143, 213 (1935).
93. V. Zitko, I. Rosik, J. Vasatko— Chem. zvest.,16, 175 (1962).
94. E. A. McMallan, F. R. Eirich.— J. Coll. Sci., 18, 526 (1963).
95. Я. R. Kruyt, A. H. de Villingen.— Proc. Kon. ned. Acad. vetensk., B,34,
1271 (1931). %. R. V. Rice, М. A. Stahmann, R. A. Alberty— J. Biol Chem209 105
(ИЫ). 97. D. G. Deruichian, C. Magnat— Bull. Soc. chim. biol., 29, 655, 660 (1947).
| но |
| Глава вторая |
98. Я. Nagashi.— Biochim. et biophys. acta,22, 459 (1956).
99. А. Б. Кульман. Физическая и коллоидная химия. М., Пищепромиздат, 1963, с. 378.
100. F. Л. Eirich, S. Tabarin, J. Hatcher, G. Tomas.— Polym. Prep^11, 775. (1970).
101. H. G. Bungenberg de long, Ong Sian Gwan.— Biochem. Z., 221, 182 (Д930)-
102. V. floss.—Arch. Biochem. and Biophys.,50, 34 (1954).
103. Л. F. Steiner— Arch. Biochem. and Biophys., 47, 56 (1954).
104. М. Shubert, E. С. Franclin— J. Am. Chem. Soc.,83, 2920 (1961)..
105. A. I. Andersen— Biochem. J., 88, 460 (1963).
106. У. Tseng, Т. E. Thompson.—•S. Phys. Chem., 69, 4242 (1965).
107. Л. /. Doyle, Tze-Jou-Kan.—VV.BS Lett,20, 1 (1972).
108. /. Steinhardt, J. A. Reynolds. Multiple equilibriain proteins. N. Y., Acad. Press, 1969.
109. P. С. Spensley, H. J. Rogers—Nature,173, 1190 (1954).
110. S. E. Kornguth, М. A. Stahmann.—Arch. Biochem. and Biophys.,91, 32 (1960). •
111. В. H. Т. Hofstee— Biochim. et biophys. acta,50, 440 (1962).
112. М. Nakagaki, Y. Sano.— Bull. Chem. Soc. Japan,45, 1011 (1972).
113. /. К. ATirat.—FEBS Lett.,36, 53 (1973).
114. L. A. Day.— Biochemistry, 12, 5329 (1973).
115. С. В. Кольцова, М. В. Гликина, Г. В. Самсонов.— Изв. АН СССР. Серия хим., №8, 1895 (1970).
116. С. В. Кольцова, М. В. Гликина, H. Г. Илларионова, Г. В, Самсонов.— Молек. биол., 5, 225 (1971).
117. В. И. Воробьев.—В сб. «Клеточное ядро». М., «Наука», 1972, с. 42—58
118. 3. А. Стрельцова. Канд. дисс. М., ИНЭОС АН СССР, 1975.
119. E. С. Вайнерман. Канд. дисс. М., ИНЭОС АН СССР, 1973.
120. Ж. Я. Чумак. Канд. дисс. М., МИНХ им. Г. В. Плеханова, 1977.
121. E. S. Wajnermann, W. la. Grinberg, W. B. Tolstogusow— Koll-Z u Z Polym., 250, 945 (1972).
122. E. S. Wajnermann, W. Ja. Grinberg, W. B. Tolstogusow— Koll.-Z., u Z Polym., 252, 234 (1974).
123. A. N. Garov, E. S. Wajnerman, W. B. Tolstogusov.— Starke 26 N 5 172 (1974); 29, N6, 186 (1977).
124. W. B. Tolstogusow, E. S. Wajnerman, S. W. Rogoshin e.a.—Nahrune' 18 N4,355(1974). °' '
125. W. B. Tolstogusow, E. S. Wajnerman.— Nahrung,19, N 1, 45 (1975).
126. Z. A. Streltsowa, W. B. Tolstogusow— Koll.-Z. u. Z. Polym.,255 1054 (1977).
127. E. С. Вайнерман, В. Я. Гринберг, В. В. Толстогузов.— Высокомол. соед 16А,№2,252 (1974).
128. E. E. Браудо, С. E. Калисанов, E. С. Вайнерман, В. Б. Тоястогузов.— Прикл. биохимия и микробиол.,11, № 2, 300 (1975).
129. 3. А. Стрельцова, Е. Е. Браудо, В. Б. Толстогузов.— Биоорг. химия 1 №2,267(1975).
130. 3. А. Стрельцова, В. К. Швядас, А. В. Максименко и др.— Биоорг химия, 1,№ 10, 1464 (1975).
131. E. E. Braudo, S. A. Strelzowa, W. B. Tolstogusow.— Nahrung,19, 9/10 903 (1975). '
132. E. Heymann. The sol-gel transformation. Paris, Hermann, 1936
133. 7. D. Ferry.— Adv. Protein Chem., 4, 1 (1948).
134. P. H. Hermans.—In: «Colloid science», v. 2. H. R. Kruyt (Ed) New York — Amsterdam, Elsevier, 1949, p. 483.
135. H. R. Kruyt, I. Th. Ouerbeek. Initiation a la chimio physique ch XI Paris, Masson, 1961.
136. W, F. Harrington, P. Ц. van Hippel,— Adv. Protein Cbcm., 16, 1 (1961).
Физико-химические основы Переработки белка в ИНН 111
137. Г. Р. Кроит.— Успехи химии,9, 682 (1940).
138. С. М. Липатов. Физико-хнмия коллоидов. М.— Л., Госхимиздат, 1948.
139. П. И. Зубов. Докт. дисс. М., НИФХИ им. Л. Я. Карпова, 1948.
140. Г. В. Виноградов.— Успехи химии, 21, 533 (1951).
141.К>. С. Липатов, H. Ф. Прошлякова.— Успехи химии,30, 517 (1961).
142. Дж. Ферри. Вязкоупругие свойства полимеров. М., ИЛ, 1963, гл. 17.
143. А. Вейс. Макромолекулярная химия желатина. М., Пищепромиздат, 1971.
144.В. }{. Измайлова. Докт. дисс. МГУ, 1971.
145. В. II. Измайлова, П. А. Ребиндер. Структурообразование в белковых системах. М., «Наука», 1974.
146. Л. 3. Воговина, Г. Л. Слонимский.—Успехи химии, 43, 1102 (1974).
147. М. Gitcksman— Adv. Food Res.,11, 109 (1962); 12, 283 (1963).
148. Industrial gums. New York — London, Acad. Press, 1959.
149. Z. J. Kertesz. The peotic substances. New York — London, Intersci. PubL, 1951.
150. E. Percival, R. H. McDowell. Chemistry and enzymology of marine algal polysaccharides. New York — London, Acad. Press, 1967.
151. М. G. J. Worth—Chem. Rev., 67, N 4, 465 (1967).
152. Е. П. Козъмина, Г. Л. Слонимский, В. Б. Толстогузов, Э. С. Бондарева.— Труды МИНХ им. Г. В. Плеханова, 58, 118 (1968).
153. Б. Йиргенсонс. Природные органические макромолекулы. М., «Мир», 1965, гл. 3.
154. В. С. Баранов. Докт. дисс. МИНХим. Г. В. Плеханова, 1973.
155. H. S. Owens, H. A. Swenson, T. H. Schulz.-Ad.-v. Chem. Ser.,11, 10 (1954).
156. Я. Я. Зубов, 3. Я. Журкина, В. А. Каргин.—1'Коллоцца. ж.,9, № 1, 109 (1947).
157. С. А. Гликман.— В кн. «Процессы гелеобразования». Изд. Саратовского гос. ун-та, 1968, с. 3.
158. В. H. Измайлова, Л. И. Хом у то в.— Высокомол. соед.,12А, 2377 (1970).
159. С. И. Меерсон.— Тезисы докладов на конференции «Природа студнеобразного состояния полимеров». Саратов, 1972.
160. С. П. Папков, М. И. Иовлева.— Высокомол. соед., 16А, № 3, 534 (1974).
161. М. L. Anson.— In: «Processed plant protein foodstuffs», ch. 11. A. М. Alt-schul (Ed.). N.Y., Acad. Press, 1958, p. 282.
162. М. Arason.—Arch. Biochem. and Biophys., 68, 1 (1962).
163. /. F. McGowan— Food Technol.,20, 55 (1966).
164. Г. Л. Слонимский, В. Б. Толстогузов.—В сб. «Успехи химии и физики полимеров». М., «Химия», 1970, с. 308.
165. Технология кондитерского производства. М., Пищепромиздат, 1959.
166. В. С. Грюнер. Товароведение крахмала, сахара и кондитерских товаров. М., Госторгиздат, 1959.
167. В. А. Ершова, В. Б. Толстогузов, Е. Е. Браудо и др.— Труды МИНХ им. Г. В. Плеханова, 58, 125 (1968).
168. В. Б. Толстогузов, В. А. Ершова, Е. Е. Браудо.—Ж. прикл.химии, 46,№ 11,2534 (1973).
169. Ю. И. Чимиров, Д. Б. Изюмов, В. Б. Толстогузов.— Труды МИНХ им. Г. В. Плеханова, № 2, 83 (1974).
170. E. R. Braudo, W. B. Tolstogusow— Nahrung, 18, N 2, 173 (1974).
171. V. B. Tolstogiisou, V. P. Belkina, V. Ja. Gulou e. a— Starkp, 26 N 4 130 (1974).
W. B. Tolstogusow, Ju. [. Tschimlrow, E. E. Braudo e a — Nahrung19N 1, 33 (1975).
173. S. W. Rogoshin, W. B. Tolstogusow.—Ibid., p. 5.
174. W. Bock, D. Lange, E. Pfeiffer.— Lebensmittel Ind.,11 337 (1962)
175. Л. G. Schweiger.—]. Oig. Chem., 27, 1789 (1962).
| Глава вторая |
176. V. Anthonsen, В. Larsen, 0. Smidsred.— Acta chem. scand., 26, 2988 (1972).
| 177, |
177. Е. Е. Браудо, Р. Б. Толстогузов.— Прикл. биохимия и микробиол., 10, № 2, 232 (1974).
178. Е. Е. Браудо. Канд. дисс. М., ИНЭОС АН СССР, 1971.
| 179. 180. |
179. Г. Л. Слонимский, В. Б. Толстогузов, Д. Б. Изюмов.— Высокомол. ооед., 12Б,№2,160 (1970).
180. Б. Б. Толстогузов, Д. Б. Ияюмов.— Высокомол. соед.,12А, № 8, 1972 (1470).
181. Д. Б. Изюмов. Канд. дис. М., ИНУОС АН СССР, 1971.
182. М. A. Muchin, Е. S. Wajnermann, W. В. Tolstogusow.— Nahriing,20, N 3, 313 (1976).
183. G. Ja. Tschumak, Е. S. Wajnermann, W. B. Tolstogusow.— Ibid., p. 231.
184. С. G. Heden, N. Molin, U. Olsson, A. Rapprecht— Biotechnol. Bioong.,13,147 (1971).
185. F. Haang, Cho Kyun Rha— Biotechnol. Bioeng.,14, 1047 (1972).
186. М. V. Tsebrenko, М. Jakob, М. Yu. Kuchinka e. a.— Int. J. Polym. Mater., 3, 99 (1974).
187. Т. I. Ablazoua, М. В. Tsebrenko, A. B. V. Yudin e.a.—J. Appl. Polym. Sci.,19, 1781 (1975).
188. G. V. Vinogradov, В. V. Yarlykov, М. V. Tsebrenko e. a.—Polymer,16,609 (1975).
189. М. В. Цебренко, А. В. Юдин, М. Ю. Кучинка и др.— Высокомол. соед., 15Б,566 (1973).
190. J. L. White, R. C. U fjord, K. R. Dharod, R. C. Price— J. Appl. Polym. Sci., 16, 1313 (1972).
191. Z. К. Walczak.—y. Appl. Polym. Sci., 17, 169 (1973).
192. C. D. Han, Y. W. Kim.—J. Appl.Polym. Sci.,19, 2831 (1975).
193. W. Berger, I. Mellentin— Faserforsch. und Textiltechn.,21, 288 (1970).
194. В. Бергер, X. В. Каммер.— Тезисы докладов. Международный симпозиум по химическим волокнам. Калинин, 1974, с. 153—159.
195. Н. Thiele— Naturwis.,34, 123 (1947).
196. Н. Thiele— Z. Naturforsch.,3b, 7 (1948).
197. Н. Thiele, H. Luck— Ibid., p. 393.
198. Н. Thiele— Universitas,5, 1081 (1950).
199. H. Thiele— Protoplasma, 58, 318 (1964).
200. Я. Klare, H. Grobe, B. Philipp— Chemiofaser, 7, 502 (1965).
201. A. Grobe, H.-J. Purz, R. Maron— J. Polym. Sci., C16, 3047 (1967).
202. H.-J. Parz, A. Grobe.— Faserforsch. und Textiltechn.,19, 460 (1968); 20 219 (1969).
203. H.-J. Purs— Faserforsch. und Textiltechn.,24, 312 (1973).
204. H. Thiele. Histolyse und Histogenese; Gewebe und ionotrope Gele. Prin-zip einer Strukturbildung. Frankfurt a. М., Acad. Verl., 1967.
205. H. Thiele, G. A ndersen.— Naturwis.,40, 366 (1953).
206. H. Thiele, G. Reese— Z. Naturforsch.,17b, 469 (1962).
207. Я. Thiele— Umschau,63, 117 (1963).
208. H. Thiele, A. Wollmer.— Klin. Monatsh. Angenheilk.,146, 900 (1965).
209. H. Thiele— Naturwis. Rdsch.,20, 51 (1967).
210. Ch. Clausen— Koll.-Z. u. Z. Polym.,224, 1 (1968).
211. Я. Thiele, G. Schyma— Naturwis.,40, 583 (1953).
212. Я. Thiele. Патент ФРГ 1011853 (1957); 1108665 (1961).
213. Я. Thiele, B. Braun. Патент США 3491760 (1970).
214. С. Sterling— Biochim. et biophys. acta,26, 294 (1957).
215. W. T. Higdon.—]. Phys. Chem.,62, 1277 (1957).
216. Я. Thiele, A. Avad— Bioreology,3, 63 (1966).
217. Я. Thiele, K. Hallich— Koll.-Z.,151, 1 (1957).
218. Я. Thiele, K. Hallich—г. Naturforsch.,13b, 580 (1958).
Физико-химические основы переработки белка вЙПП 113
2Щ В. Б. Толстогузов, А. И. Мжельский, Н. В. Гринберг и др.— Высокомол,
соед.,15А, № 12, 2703 (1973).
220. Б. Б. Толстогузов, Д. В. Изюмов, А. И. Мжельский.— Конференция пп Природе студнеобразного состояния. Саратов, 1972. Изд. Саратовского
^ос. ун-та, 1972, с. 25.
221. V. В. Tolstoguzov—Colloid and Polym. Sci., 253, N 2, 109 (1975).
222. Г, Л. Слонимский, В. В. Толстогузов, Д. Б. Изюмов.— Высокомол. соед.,
12Б,№6,408 (1970).
223. Д. Б. Изюмов, В. Б. Толстогуяов, В. И. Бугаева.— Изв. АН СССР. Серия
хим., № 3, 711 (1970). 22'i. /','. С. Оболонкова., Е. М. Белавцева, R. Е. Браудо, В. Б. Толстогузов.—
Биофизика,19, № 3, 447 (1974).
?.25. Е. S. Obolonkova, E. М. Belavtseua, E. E. Braudo, V. B. Tolstogusov— Colloid and Polym. Sci.,252, N 7, 526 (1974).
226. Я. Thiele, H. Lack— Z. Naturforsch.,3b, 393 (1948).
227. E. М. Белавцева, В. Б. Толстогузов, Д. Б. Изюмов, М. М. Генина.— Биофизика,17, Ni 5, 744 (1972).
228. E. Baardseth. Proceedings 5th. International seawead symposium. Halifax,
1965, p. 19.
229. A. Haug.—Acta chem. scand.,13, 1250 (1959).
230. A. Haug, 0. Smidsred.— Acta chem. scand.,19, 341 (1965).
231. Д. Kohn, J. Furda, A. Hang, 0. Smidsred.—Acta chflm. scand.,22, 3098
(1968).
232. 0. Smidsred, A. Haug— Acta chem. scand., 26, 2063 (1972).
233. 0. Smidsred, A. Haug, S. G. Whittington,— Ibid., p. 2563.
234. E. R. Moris, D. A. Rees, D. Thorn.— Chem. Communs, 1973, 245.
235. G. T. Grant, E. R. Moris, D. A. Rees e. a.— FEBS Lett, 32, 195 (1973).
236. A. Hang, 0. Smidsred.— Actachem. seand., 19, 329 (1965).
237. A. Haug, S. Myklestad, B. Larsen, 0. Smidsred— Acta chem. scand.,21,
768 (1967).
238. 0. Smidsred, A. Haag.— Acta chem. scand., 26, 79 (1972).
ГЛАВА ТРЕТЬЯ
БЕЛОК КАК СЫРЬЕ ДЛЯ ПОЛУЧЕНИЯ ИСКУССТВЕННЫХ ПРОДУКТОВ ПИТАНИЯ
ПОНЯТИЕ О ФУНКЦИОНАЛЬНЫХ СВОЙСТВАХ БЕЛКА
Оценка ресурсов пищевого белка зачастую страдает существенным недостатком, поскольку учитывает лишь продуктивность тех или иных источников белка, биологическую ценность последнего и в лучшем случае стоимость его производства. Однако, как показано в гл. I, белок не является пищей, а служит лишь ее компонентом, и поэтому биологическая ценность белка и его стоимость не являются достаточными аргументами для потребления белка человеком. Ориентация на максимальную биологическую ценность и минимальную стоимость даже для новых продуктов питания (комбинированных и обогащенных) обычно не приводит к успеху при их сбыте. Этого тем более недостаточно, когда речь идет о белке. Узловой момент проблемы пищевого белка заключается в его переработке в искусственные продукты питания, и поэтому оценка реальных ресурсов белка должна учитывать возможность и стоимость такой переработки. Следовательно, методы выделения белка из того или иного источника, экономическая целесообразность и масштабы производства белка и его использования для питания не могут быть оценены без учета возможностей и стоимости переработки этого белкового сырья в искусственные продукты питания.
Возможность и стоимость переработки данного вида белкового сырья в искусственные продукты питания определяются сложным комплексом физико-химических характеристик этого сырья, охватываемых понятием «функциональные свойства». Таким образом, основное требование к белку как к исходному сырью для получения искусственных продуктов питания заключается в наличии необходимых для его переработки функциональных свойств.
Наряду с функциональными свойствами, а также стандартностью, важнейшими критериями качества белкового сырья для получения искусственных продуктов являются его стоимость и биологическая ценность. Как правило, по мере повышения степени очистки белка его функциональные свойства и стандартность повышаются, биологическая ценность снижается, а стоимость растет. Повышенная стоимость белка с высокими функциональными
Белок как сырье для полученияИПП И5
свойствами компенсируется, однако, увеличением продолжительности и удешевлением хранения белка, а главное, возможностью его переработки, и притом с меньшими затратами, в более широкий ассортимент искусственных продуктов питания, в том числе в искусственные продукты, имитирующие наиболее дорогостоящие традиционные продукты массового потребления, например в искусственные мясопродукты. В свою очередь, снижение биологической ценности белка при его выделении и очистке обычно может быть скомпенсировано добавлением незаменимых аминокислот или же путем его переработки в виде смеси с другими белками со взаимодополняющим аминокислотным составом, т. е. путем использования принципов обогащения или комбинирования. Таким образом, с точки зрения переработки и использования в виде искусственных продуктов питания цена и биологическая ценность белка как критерии его качества имеют относительно меньшее значение, чем функциональные свойства.
Понятие о функциональных свойствах было кратко рассмотрено в гл. II при обсуждении физико-химических задач, возникающих при переработке многокомпонентных систем, содержащих белки. Там же рассмотрены некоторые приемы регулирования функциональных свойств белков и полисахаридов в жидких и студнеобразных системах. Это понятие требует, однако, более подробного рассмотрения.
Под функциональными свойствами обычно понимают характеристики белка, определяющие его поведение при переработке и хранении. К ним относятся растворимость в воде, в солевых, щелочных и кислых средах, гетерогенность, совместимость с другими компонентами пищи, способность стабилизировать суспензии, эмульсии, пены, образовывать студни при нагреве растворов и дисперсий, адгезионные свойства и другие характеристики, а также обусловленные примесями цвет, вкус и запах продукта. Высокими функциональными свойствами характеризуются белки, хорошо растворимые в водных средах, способные образовывать высококонцентрированные, вязкие растворы и прочные студни, обычно возникающие при нагреве растворов, эффективно стабилизирующие пены, эмульсии и суспензии других пищевых веществ в водных средах, лишенные специфического запаха, вкуса, окраски, практически не содержащие липидов и не изменяющие своих свойств при продолжительном хранении в обычных условиях. Напротив, белки с низкими функциональными свойствами, как правило, нерастворимы или частично растворимы в водных средах, не образуют прочных студней при нагреве растворов или дисперсий, окрашены, обладают специфическим запахом и вкусом в сухом состоянии, в водных средах или же приобретаютихпри нагреве, имеют нестандартные характеристики, изменяющиеся при хранении. Белки с низкими функциональными свойствами
| Глава третья |
обычно не используют в производстве искусственных продуктов питания, а применяют для получения белковых гидролизатов, а
также в качестве обогащающих пищевых или кормовых добавок.
Функциональные свойства белка чаще всего оценивают по растворимости в стандартных условиях и характеризуют коэффициентом растворимости азота или коэффициентом диспергируемо-сти белка (КДБ). В первом случае определяют количество; азота, во втором — количество белка, перешедшего в раствор. Так контролируют, в частности, изменение свойств белка в процессе выделения, очистки и хранения.
Реологические свойства белков исследуют в различных водных средах и температурных режимах, в разных условиях деформирования жидких и студнеобразных систем. Важными показателями служат прядомость растворов белка, условия образования и реологические свойства белковых студней. Способность белков стабилизировать пены обычно определяют встряхиванием или перемешиванием водных растворов или дисперсий белка в строго стандартизованных условиях (объем, концентрация, рН раствора белка, температура, размеры и форма сосуда, мешалки, продолжительность и режим перемешивания или встряхивания). Измеряют объем образовавшейся пены, а также ее объем после хранения в определенных условиях; в последнем случае оценивают стабильность пены. Аналогичным образом определяют эмульги-рующую способность белка интенсивным перемешиванием смеси раствора белка и масла в строго стандартизованных условиях с последующим центрифугированием полученной системы в стандартных условиях и измерением объема неэмульгированного масла. Результаты обычно выражают в виде количества эмульгиро-ванного масла на грамм белка. Здесь упомянуты, однако, лишь простейшие методы оценки функциональных свойств белков, так как это понятие носит существенно более широкий характер и включает различные физические и физико-химические характеристики растворов, дисперсий и студней белков и т. д. [1—20].
В связи с необходимостью производить белки с требуемыми функциональными свойствами, возможно более низкой стоимостью и высокой биологической ценностью важное значение приобретает разработка экономически эффективных способов выделения белка из различных источников, исключающих значительную денатурацию и деструкцию и обеспечивающих определенный фракционный состав и комплекс физико-химических свойств белка, а также разработка методов очистки белка от липидов, нуклеиновых кислот, токсических веществ, аллергенов, а также веществ, обусловливающих вкус, запах и окраску. Белок, естественно, должен быть очищен от примесей, нежелательных с медико-биологической точки зрения, В этом отношении среди многочисленных ви-
Белок как сырье для полученияИПП 117
дов белкового сырья выделяются казеин и другие белки молока, не требующие очистки. Поэтому, несмотря на сравнительно невысокие функциональные свойства, казеин представляет большой практический интерес.
Требования к очистке белка с позиций функциональных свойств очень различны. Очистка белка должна обеспечивать необходимую продолжительность хранения. В этом отношении важно удалить реакционноспособные и легкоокисляемые компоненты, прежде всего липиды. В ряде случаев требуется отделить минеральные и другие примеси, препятствующие получению многокомпонентных систем необходимого состава и фазового состояния, например удалить ионы поливалентных металлов, осаждающие кислые полисахариды. Макро- и микроэлементы, липиды и другие компоненты, важные с биологической точки зрения, могут быть затем вновь введены в продукт на последующих стадиях его получения. В других случаях оказывается необходимым полностью удалить нерастворимые примеси, например целлюлозные волокна при производстве изолятов соевого белка, предназначенных для получения белковых волокон методом мокрого прядения. В противном случае возможно засорение фильер и обрыв волокон.
Основные научно-технические задачи в области выделения и очистки белков заключаются в выборе режимов этих процессов, обеспечивающих необходимые функциональные свойства белка как важнейший критерий его качества. Эти задачи весьма сложны и разносторонни по характеру, особенно если учесть сложность структуры и многокомпонентную природу систем, из которых выделяют белок, а также широкий диапазон требований к его функциональным свойствам. Последние определяют выбор стратегии при переработке белка и имеют, следовательно, решающее значение для его потребления. Действительно, если выбор приемов переработки материалов технического назначения возможен при учете сравнительно небольшого числа параметров, например для полимеров при наличии сведений о растворимости и поведения при нагреве (термопластичные и термореактивные материалы), то белки обычно перерабатываются в искусственные продукты питания в составе многокомпонентных систем. Наряду со сведениями о растворимости и поведении белка в растворе при изменении температуры, ионного состава и рН системы, необходимы сведения о его сорастворимости с другими компонентами пищи, способности стабилизировать суспензии, эмульсии, пены, окрашиваться и ароматизироваться и т. д. Сложность задач, возникающих при выделении и очистке белка, обусловлена, таким образом, разнообразием требований к белку как исходному сырью для получения пищи. Она может быть в известной мере снижет» в результате разработки приемов регулирования функциональных
118 Глава третья
свойств белка, а также способов получения искусственных продуктов питания, достаточно универсальных по белку (см. гл. II).
Белки, как правило, производят в виде трех основных типов продуктов, различающихся по содержанию белка и степени его очистки. Так, белки семян масличных культур выпускают в форме обезжиренной муки семян (содержит около 50% белка), концентрата и изолята белка (содержат соответственно 70—75 и 90— 99% белка). Аналогичные виды продуктов производят и из других источников, например из малоценных пород рыбы (рыбная мука, концентраты и изоляты рыбного белка), дрожжей и других одноклеточных (дезинтеграт дрожжевой биомассы, концентраты и изоляты дрожжевого белка) и т. д. Наиболее стандартный вид белкового сырья, с наилучшими функциональными свойствами, — изоляты белков. Их производство растет наиболее быстро, и они практически полностью используются для питания.
Белковые продукты всех трех основных типов выпускаются в виде многочисленных модификаций, различающихся фракционным составом, степенью денатурации и очистки белка. Каждая из этих модификаций характеризуется определенными функциональными свойствами и специально предназначена для производства тех или иных искусственных продуктов питания. Регулирование функциональных свойств белка обычно достигается изменением технологии и режимов его выделения.
Высокие функциональные свойства белков, извлекаемых из соевых бобов, наряду с научно-техническим уровнем, достигнутым в области производства различных модификаций этого белка, сыграли важную роль в быстром развитии производства искусственных пищевых продуктов на их основе. Ниже будут рассмотрены методы получения и характеристики этого вида белкового сырья, а также, более кратко, другие перспективные, но менее изученные в отношении функциональных свойств и способов переработки виды белков. Ресурсы белков и возможности их использования для питания обсуждаются в большом числе научных сообщений и монографий [21—37].
БЕЛОК СОЕВЫХ БОБОВ
Производство искусственных продуктов питания начиная с периода его организации в США и до настоящего времени базируется почти исключительно на переработке белка соевых бобов. Это обусловлено рядом причин. Соевые бобы содержат большое количество белка (около 40% от сухого веса), который отличается высоким содержанием незаменимых аминокислот (за исключением метионина) и, следовательно, высокой в сравнении с другими растительными белками биологической ценностью. Данные
Белок как сырье для полученияИПП
о среднем составе соевых бобов [3] приведены ниже (% на су-
vnu VOf.) •
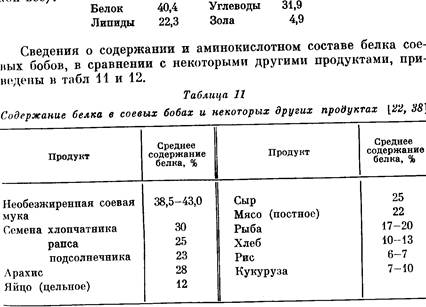
Соевые бобы содержат также около 20% высококачественного масла, одновременное получение и использование которого снижает стоимость белка приблизительно в два раза. При исключительно широких масштабах производства соевых бобов в США они являются мощным источником наиболее дешевого белка. В табл. 13 приведены сведения о масштабах производства соевых бобов в США, а в табл. 14 — данные о стоимости белков.
Помимо низкой стоимости и высокой пищевой ценности, близкой к белкам животного происхождения, белок сои обладает высокими функциональными свойствами, что существенно облегчает и удешевляет его переработку в различные формы искусственных пищевых продуктов. Другим важным обстоятельством, способствовавшим развитию производства искусственных пищевых продуктов на основе белка сои, послужила широкая апробация соевых бобов в питании на многих поколениях людей. Искусство превращать соевые бобы в пищевые блюда было развито уже около 4 тыс. лет назад и прочно вошло в кулинарную практику народов Юго-Восточной Азии [3, 38, 43—45]. В настоящее время соевые бобы составляют заметную часть белкового рациона населения этих стран. Так, в 1967 г. в Японии доля белка соевых бобов в белковом рационе составила 12—15% [10, 46, 47].
120 Глава третья
Таблица 12
Содержание незаменимых аминокислот (г/16 г азота) в белках семян масличных культур и некоторых пищевых продуктах [17, 39]
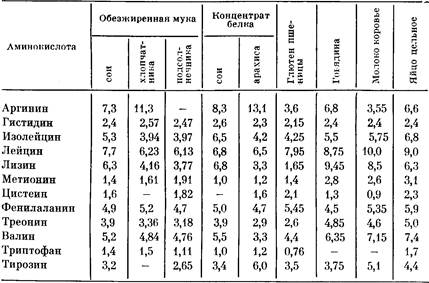
В США сою начали культивировать в начале прошлого века, однако на протяжении более ста лет она оставалась сельскохозяйственным курьезом. Толчком для развития производства бобов сои в США и Японии послужила разработка в 1920-х годах в Германии процессов и аппаратуры для непрерывной экстракции соевого масла органическими растворителями. В Германии же было впервые организовано производство обезжиренной соевой муки и соевого масла методом непрерывной экстракции. Первый завод такого рода в США (мощность 100 т бобов в день) был пущен в 1934 г. в Чикаго фирмой «Арчер даниельс мидланд ко.». Начиная с 1930-х годов в США наблюдался быстрый рост производства бобов сои и их переработки на обезжиренную соевую муку и соевое масло методом непрерывной экстракции гексаном. За последние 50 лет объем производства соевых бобов возрос в США приблизительно в 300 раз и ныне составляет более 70% от мирового производства. В 1973 г. в США было произведено 43 млн. т соевых бобов, и в настоящее время в этой стране под сою занята шестая часть обрабатываемых земель. При этом около 65% урожая перерабатывается в муку и масло [3, 28, 38— 40, 43, 45—49]. Соевое масло содержит много полиненасыщен-
Белок как сырье для полученияИПП.
ных жирных кислот (незаменимый фактор питания) и более чем на 90% используется для пищевых целей в виде салатных масел, в производстве маргарина и т. д. Объем его производства составляет более 85% от общего производства растительных масел
Таблица 13
Производство соевых бобов [3, 39, 40]
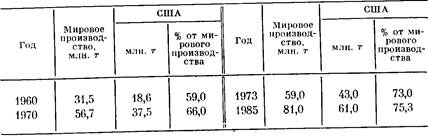
Таблица 14
Стоимость белка в различных пищевых продуктах. США, 1966-1971 гг. [28, 29, 35, 41, 42]
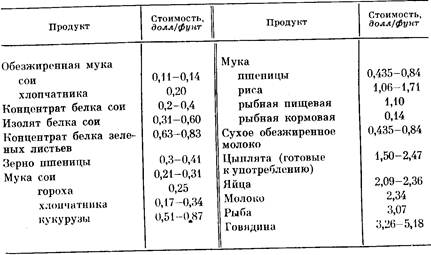
в США [49]. Соевая мука более чем на 80% используется в виде кормов и лишь около 3% ее (около 400—500 тыс. г) идет в настоящее время непосредственно для питания человека [3, 43].
При столь больших масштабах производства и дешевизне полноценного белка соевых бобов в США на его основе было организовано производство практически всех известных форм искусст-
122 Глава третья
венной пищи. Проблема получения искусственных продуктов питания в США почти полностью свелась поэтому к развитию способов переработки белка сои в пищевые продукты. Аналогичный характер имеет проблема получения искусственных продуктов питания в странах Западной Европы (Голландия, Англия, ФРГ) и в Японии. В США и Японии нашли также развитие методы переработки белка пшеницы (отход производства крахмала).
Таблица 15
Типичный состав обезжиренной соевой муки (ОМ), концентрата (КБ) и изолята (ИБ) белка бобов сои [3, 11}
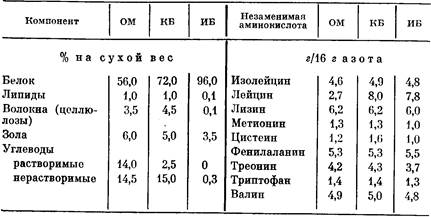
Производство и переработка белков семян других масличных (хлопчатник, арахис, подсолнечник, рапс) и зерновых (кукуруза) культур играет пока существенно меньшую роль, хотя, как будет показано ниже, в этом направлении предпринимаются большие усилия.
Стремление улучшить функциональные свойства белка сои привело к организации производства концентратов и изолятов соевого белка. Производство белковых изолятов было впервые организовано и США в 1960—1961 гг. [11] и затем в 1965—1967 гг. в Японии [10]. В настоящее время белок соевых бобов используют для производства искусственных продуктов питания в виде трех основных продуктов: обезжиренной соевой муки, концентрата и изолята соевоего белка, типичный состав которых показан в табл. 15. Каждый из этих основных продуктов имеет большое число модификаций (см. табл. 16—20) с различными функциональными свойствами [3, 8, 9, 12—16] и биологической ценностью [9, 16, 50, 51]. Кратко рассмотрим принципиальные схемы производства этих продуктов.
Белок как сырье для получения ИНН 12.3
Схема I
ПРОИЗВОДСТВО ОБЕЗЖИРЕННОЙ СОЕВОЙ МУКИ МЕТОДОМ НЕПРЕРЫВНОЙ ЭКСТРАКЦИИ ГЕКСАНОМ [3, 52]
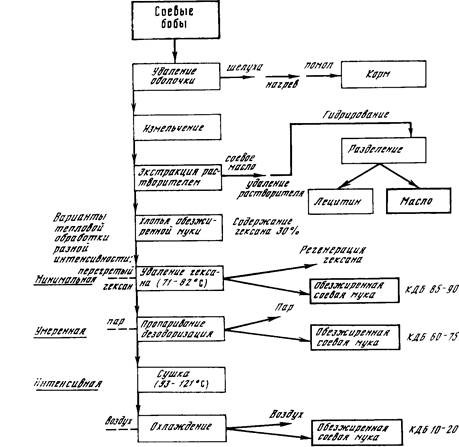
Для получения обезжиренной муки соевые бобы освобождают от оболочек и обезжиривают экстракцией гексаном. Основные этапы процесса показаны на схеме I. Существенную роль играет режим тепловой обработки обезжиренной соевой муки при удалении из нее растворителя, от чего зависят как функциональные свойства, так и биологическая ценность продукта. В табл. 16 приведены сведения о некоторых функциональных свойствах (КДБ, вкус) и биологической ценности (КЭБ) белка обезжиренной соевой муки, получаемой при различной интенсивности тепловой об-

работки. Промышленность выпускает обезжиренную муку в виде ряда продуктов, различающихся режимом тепловой обработки, функциональными свойствами и назначением (табл. 17).
Концентраты белка соевых бобов производят тремя основными методами. Все они сводятся к удалению из обезжиренной муки углеводов, минеральных солей и других водорастворимых веществ | (схема II). В первом случае обезжиренную соевую муку обраба- | тывают разбавленным раствором кислоты при рН 4,5—4,6 (ИЭТ | глобулинов сои), затем белок промывают, нейтрализуют и сушат. | Высокая растворимость белка достигается лишь в случае его тща- 1
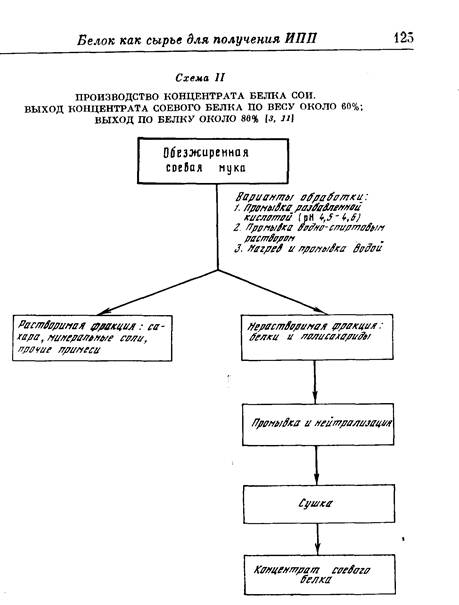
тельной нейтрализации перед сушкой. Во втором случае обезжиренную соевую муку обрабатывают 60—80%-ным водным раствором спирта. Так получают концентрат сои с низкой растворимостью белка вследствие его денатурации под действием спирта. Третий способ заключается в предварительном нагреве обезжиренной муки для денатурации белка и последующем экстрагировании водорастворимых примесей. В последнее время предложен еще один метод получения концентрата белка, который заключа-
126 Глава третья
ется в нагреве обезжиренной муки в водном растворе хлористо кальция и последующей промывке коагулята белка водой [45 Все виды концентрата соевого белка, естественно, имеют разли ные функциональные свойства при приблизительно одинаковом с держании белка (табл. 18).

Для получения белкового изолята обезжиренную соевую муку обрабатывают водным раствором щелочи для растворения белка (схема III). Раствор фильтруют и осаждают белок при ИЭТ (рН 4,5—4,6) добавлением кислоты. Коагулят белка промывают водой и сушат. В результате получают так называемый изоэлект-рический изолят белка, характеризующийся низкой растворимостью в воде. Растворимый в воде продукт, или изолят белка — протеинат, получают нейтрализацией коагулята белка щелочью (до рН 7,0) перед его сушкой. В промышленных масштабах в настоящее время производится широкий набор модификаций концентратов и изолятов соевого белка различного назначения. В табл. 19 в качестве примера приведены данные о составе и функциональных свойствах ряда модификаций изолятов соевого белка, выпускаемых фирмой «Ральстон пьюрина ко.».
В последнее время предложен ряд новых способов производства изолята соевого белка. Так, по методу компании Юнилевер [53] белок бобов сои растворяют в подкисленном растворе соли (рН 5; 0,5 М NaCI), а затем осаждают, разбавляя водой. В этом случае получают изолят белка повышенной биологической ценности, поскольку процесс его производства не сопровождается разрушением части аминокислот, как это происходит в щелочных растворах белка при обычных способах производства изолята. Кроме того, как показано в [54, 55], обработка белка соевых бобов щелочью, по-видимому, сопровождается образованием ток
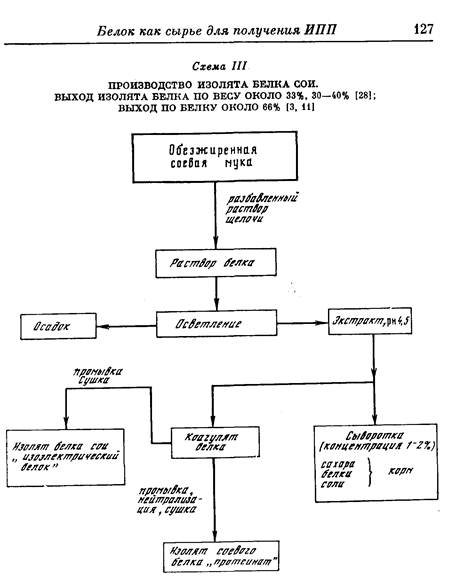
сичного продукта лизиноаланина. Тем не менее щелочные растворы используют не только для выделения белка в виде концентратов и изолятов, но и при его переработке, например, в пищевые волокна (см. гл. IV). Большое значение имеет поэтому разработка методов выделения белка без использования щелочей, равно как и методов регулирования функциональных свойств белков (см. гл. II). В настоящее время функциональные свойства белка соевых бобов регулируют в основном, варьируя режим их выделения, величину рП при промывке и нейтрализа-
Таблица 19 Белковые продукты фирмы «Ралъетон пьюрина ко.» *'
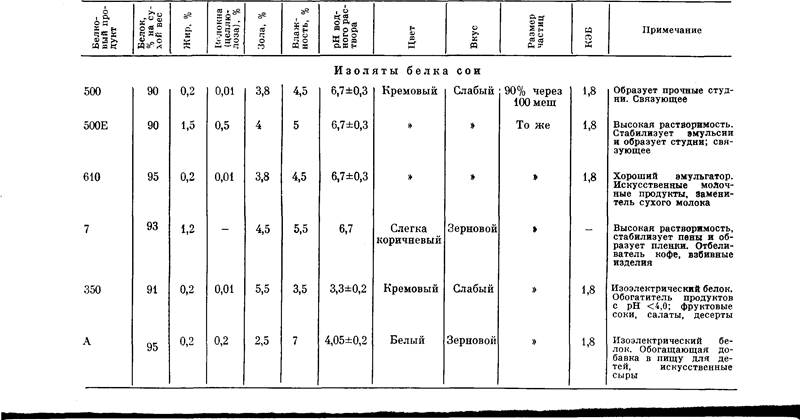
Таблица 19 (окончание)
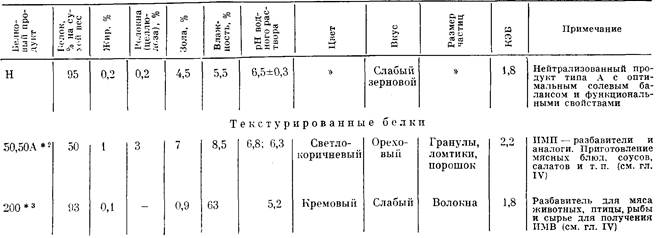
*•>' См. гл. IV, [245].
*2 Продукты получены методом экструзии (см. гл. IV).
*3 Продукт получен ме годом мокрого прядения изолята белка бобов сои.
130 Глава третья
ции, режимы тепловой обработки и сушки. Биологическая ценность белка бобов сои в изолятах, концентратах и обезжиренной муке обычно тем ниже, чем выше его функциональные свойства и содержание в продукте (табл. 20).
Производство концентратов и изолятов соевого белка имеет целью расширить возможности переработки белка соевых бобов в искусственные продукты питания, а также использовать эти белки с целью совершенствования технологии и повышения содержания белка в традиционных пищевых продуктах. Дополнительные
Таблица 20
Биологическая ценность белков сои в виде обезжиренной соевой муки, концентрата и изолята белка [8, 9, 50, 52]

затраты на получение концентратов и изолятов компенсируются относительно высокой стоимостью искусственных пищевых продуктов, особенно тех, которые имитируют мясопродукты. Концентраты белка сои с высокой растворимостью белка используют в качестве связующего при получении искусственных мясопродуктов и изделий из рубленого мяса, а концентраты с низкой растворимостью — is качестве белковых обогатителей п при производство напитков с повышенной биологической ценностью. Изоляты белка применяют более широко. Они имеют нейтральный вкус, запах л цвет (белый, кремовый), хорошо растворяются в воде (протеппаты), солевых п щелочных растворах, при нагрево растворов и копцептрпроваппых суспензий образуют прочные песиперпрующпе студни с высоким содержанием воды (йто последнее свойство характеризуют термином «водосвязы-пающая способность»), обладают волокнообразующнмн свойствами, хорошо стабилизуют эмульсии жиров в воде, непы и суспензии белков и крахмала. Их используют для стабилизации эмульсий при получении сосисок и других изделий из рубленого
Белок как сырье для получения ИПП 131
мяса, в производстве искусственных молочных продуктов и напитков, при получении белковых волокон для искусственных мясопродуктов и т. д. [8—16, 33—39].
Производство белка сои в США в последние 5—7 лет резко возросло, и только обезжиренная соевая мука производится на 125 заводах.
13 табл. 21 приведены сведения об объеме пронзнодстпа и пенах в США на три основных тина соевых белковых продуктов
Таблица 21
Производство белков сон для пищевых целей (ИНН и обогащающие добиики}. ('111 Л
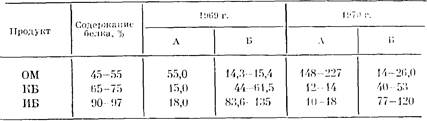

Примечание. Л — объем производства (ЮПИ т); I; цгна (1(''"г/к?).
f3, 11, 12, 15, Hi, 2<S, 5(i, 57].15 области нронзнодства и переработки белка соеных бобов работает более дкадц.гги крупных фирм СШЛ. Аналогичный процесс происходит и и других иро-мышленно развитых странах [.'-i, 39, W. •)8—61].
Производство белка соевых бобов, его состаи, функционал],пые снойства п биологическая ценность рассмотрены в ряде обзоров и монографий [0. 9, 12—16, 2/l, 62].
ДРУГИЕ РАСТПТЕ/П.НЫ!': Г,ЕЛ1>11
li первой rnai;e была отмечена высокая .•ффгктнтюсть растительных культур li проп.-яюдстве белка (см. табл. 3) н ведущая po.'n, зерновых культур в обеспечении белком населения планеты (см. табл. 7). Мы говорили также и о том, что болге половины
5*
132 Глава третья
производимых растительных белков используется для питания животных, а кроме того, значительная часть ценных белковых отходов сельскохозяйственного производства и пищевой промышленности используется не только в виде кормов, но также в качестве удобрений и для технических целей. Отсюда, естественно,
Таблица 22
Мировое производство важнейших видов растительной пищи [46]
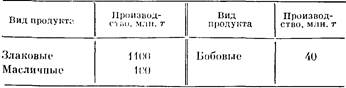
следуют огромные потенциальные ресурсы пищевого белка, который можно было бы использовать для питания человека при условии его выделения из растительного сырья в виде препаратов с необходимыми функциональными свойствами и переработки в искусственные продукты питания. Решение этой задачи — путь к интенсификации сельскохозяйственного и пищевого производства, существо которого заключается в комплексной переработке растительного сырья и прямом использовании белка для питания человека. Учитывая, что в ближайший период времени первостепенная роль в решении проблемы дефицита белка несомненно будет принадлежать сельскохозяйственному производству, и 'прежде всего земледелию, становится ясной чрезвычайная актуальность задачи разработки методов выделения растительных белков и методов их переработки в искусственные продукты питания массового потребления. Важно также то обстоятельство, что к настоящему времени накоплен большой положительный опыт широкого использования для питания человека рационов, содержащих исключительно растительные продукты [43, 63, 64], а также в области получения продуктов с повышенной биологической ценностью (принципы комбинирования и обогащения). Поэтому как вкусовые качества, так и биологическая ценность таких рационов могут быть существенно улучшены в результате использования новой технологии, позволяющей перерабатывать растительные белки в искусственные пищевые продукты.
Среди растительных культур ведущее место по объему производства занимают зерновые. Сведения о масштабах производства основных растительных культур, зерновых культур и белка зерновых приведены п табл. 22 и 23. Обращает на себя внимание огромное количество бглка, производимого в виде зерновых куль
Белок как сырье для полученияИПП 133
тур. Прямое использование для питания даже части этого белка позволило бы полностью ликвидировать дефицит белка в рационе питания мирового населения, при условии обогащения получаемых на их основе искусственных продуктов питания недостающими незаменимыми аминокислотами.
Таблица 23
Мировое производство зерновых и белка зерновых (по данным ООН) [Д5]
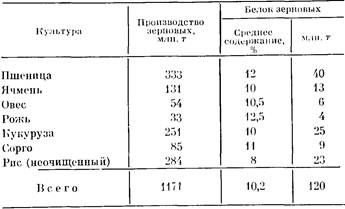
В результате переработки зерновых культур, например пшеницы, кукурузы, риса, на крахмал в виде отходов получают значительные количества дешевого белка. Однако поскольку производство ориентировано на выработку крахмала, то белки зерновых обычно обладают низкими функциональными свойствами и используются для получения белковых гидролпзатов, а также как обогащающие пищевые добавки или же как корм скоту.
Тем не менее в последнее время в ряде стран организовано промышленное производство белков зерновых с высокими функциональными свойствами, получаемых наряду с крахмалом. Наибольшее развитие получило производство и переработка в искусственные пищевые продукты пшеничной клейковины. Это производство организовано в США и Японии. Интересно отметить, что в Японии масштабы переработки в пищу белка соевых бобов и пшеницы вполне сопоставимы, но производство и переработка последних растет несколько быстрее (табл. 24).
Большой интерес представляют выделение н переработка белка картофеля как отхода производства крахмала. Учитывая значительные масштабы производства картофельного крахмала и высокую биологическую ценность этого белка, несмотря на низкое
134 Глава третья
содержание его в картофеле (около 2%), он может стать одним из весьма перспективных дополнительных источников белка для питания. Производство картофельного белка налажено в Голландии.
Наиболее перспективными видами сырья для производства искусственных продуктов питания считают белки семян масличных культур. Это наиболее дешевое на сегодня белковое сырье, к тому
Таблица 24
Производство искусственных продуктов питания (в тоннах) на основе растительных белков. Япония [45]
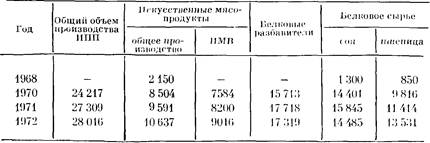
же отличающееся сравнительно высокой биологической ценностью. К масличным культурам относятся соя, хлопчатник, подсолнечник, арахис, рапс, копра, конопля, леп, кунжут, горчица и др. Среди них наибольшее значение приобрели соя, хлопчатник, подсолнечник, арахис и рапс. Фракционный, химический состав и функциональные свойства белков некоторых из указанных культур сравнительно хорошо изучены [13—17, 37, 62, 66—70].
В настоящее время подавляющую часть урожая семян масличных используют для производства растительных масел, а получаемые при этом белковые отходы в виде жмыхов и шротов идут главным образом на корм скоту, а также па удобрения и для технических нужд. Данные о производстве растительных масел из семян масличных культур в различных странах и районах мира приведены в табл. 25 и 26. В 1967—1969 гг. для питания было использовано не более 11 млн. т семян масличных, преимущественно в странах Азии. Около 90 млн. г, что эквивалентно приблизительно 30 млн. г белка, не используется в пищу. При этом около 63 млн. т семян масличных идет на корм и удобрения [11, 23]. Потенциальные ресурсы белка масличных культур, следовательно, весьма велики. Однако, если методы получения белка бобов сои с необходимыми функциональными свойствами и методы переработки этих белков в искусственные пищевые продукты сравнительно хорошо изучены, то этого нельзя
Белок как сырье для получения ИПП 135
сказать о белках других масличных культур, производство которых только осваивается. Жмыхи, получаемые при производстве растительных масел, хотя и содержат много белка (табл. 27), но последний обладает относительно низкими функциональными свойствами и поэтому непригоден для производства искусственных продуктов питания. Несомненно, более прогрессивна технология, ориентированная на одновременное выделение белка и масел, позволяющая получать белки с высокими функциональными снойствами. Как было показано выше, такой подход был реализован при переработке соевых бобов; в последнее время аналогичные методы разрабатываются и для переработки других масличных культур.
Недавно в США начато производство обезжиренной муки, концентрата и изолята белка семян хлопчатника. Необходимой предпосылкой явилась разработка методов удаления токсичного
Таблица 25 Основные страны - производители растительных масел [28]
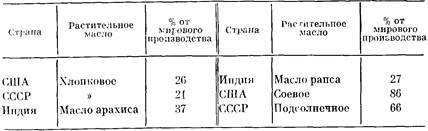
Таблица 26 Мировое производство масличных в J967—1969 гг. [37,46]
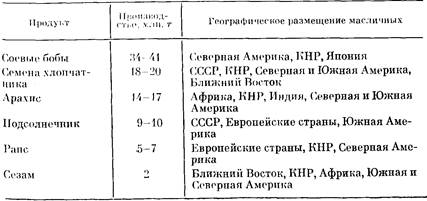
136 Глава третья
пигмента госсипола [И, 71—73], а также методов переработки белка. В США, кроме того, выведены сорта хлопчатника, свободные от госсипола, дающие нетоксичный изолят белка. К 1980 г. они, как предполагается, должны полностью заменить обычные сорта [23, 74].
Все большее внимание привлекает белок подсолнечника. Он может быть получен с хорошими функциональными свойствами, с относительно высоким содержанием незаменимых аминокислот и со стоимостью ниже, чем для белков сои (в 1971 г. обезжиренная мука подсолнечника стоила 85 долл/т, обезжиренная мука соевых бобов—110 долл/т). По-видимому, это наиболее дешевый вид белкового сырья.
Другим перспективным источником растительного белка могут стать семена бобовых культур (помимо сои): гороха, фасоли, бобов, которые содержат в среднем 20—35% белка. Эти белки отличаются хорошей сбалансированностью по содержанию пезаме-
Таблица 27 Содержание белка в жмыхах масличных культур [33]

Таблица 28
Источники пищевого белка для получения искусственных продуктов питания и пищевых добавок. Англия. Прогноз на 1981 г. [31]
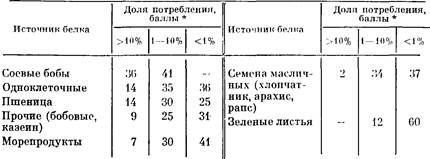
* Статистическая обработка мнения экспертов.
Белок как сырье для полученияИПП 137
пнмых аминокислот и высоким содержанием водорастворимых фракций, однако их функциональные свойства остаются неисследованными.
Наконец, еще одним чрезвычайно интересным источником растительного белка для питания являются листья и зеленая масса растений. Ресурсы белка здесь практически неограничены. Они включают не только белки трав и других быстрорастущих растений, но также отходы земледелия, например при выращи-нанин овощей и фруктов, отходы плодо- и овощеперерабатывающей промышленности и т. д. Эффективность производства белка при выращивании трав обычно значительно выше, чем в других отраслях земледелия, особенно, если учесть возможность собирать несколько урожаев в год. Как было отмечено выше, при выращивании, например, люцерны производительность 1 га культивируемой земли приблизительно в 5 раз выше, чем для бобов сои (см. табл. 3). При этом белок люцерны обладает сравнительно высокой биологической ценностью (КЭБ—2,2 [37]).
Листья и зеленая масса растений содержат белок в форме, удобной для извлечения. Их измельчают, отжимают сок, белок осаждают подкисленном или нагревом и подвергают очистке. Ряд технологических трудностей связан с низким содержанием в соке белка и высоким содержанием целлюлозы, пигментов и других примесей, которые необходимо удалять [23, 39, 75—82]. Хотя способ получения концентрата белка листьев был впервые описан более двухсот лет назад, его изучение проводится в ограниченных масштабах лишь в течение последних 30 лет и еще не достигло такого уровня, как для белков семян масличных культур, что позволило бы широко использовать этот вид белка для питания человека. Тем не менее, в этом направлении достигнуты определенные успехи. Начато производство и переработка белка золеных листьев и растений в ряд форм искусственной пищи, прежде всего в искусственные молочные продукты [75, 81]. Было сообщено [82] о пуске опытного завода, производящего пищевой коиноптрат белка из свежей люцерны («Вилпро»). Этот продукт белого цвета, содержит около 90% белка и менее чем по 0,5% жиров, целлюлозы и минеральных солей. Средний выход продукта составляет 1,9—2,2% от веса люцерны, 8,7% от общего содержания белка и 26,1% от растворимого белка.
В заключение отметим, что перспективность того или иного источника определяется прежде всего экономической рентабельностью производства па его основе белков с необходимыми и варьируемыми (для различных форм пищи) функциональными свойствами, а также переработки этого белкового сырья в искусственные продукты питания. Она, естественно, зависит в первую очередь от ресурсов данного источника белка, а также от научно-технического уровня, достигнутого в области выделения и пере-
138 Глава третья
работки этого вида белка. Поэтому перспективность различных источников нетрадиционного белка для питания различается для отдельных стран. Так, в США белок бобов сои в настоящее время является наиболее перспективным, в Японии он перерабатывается приблизительно в тех же количествах, что и белок пшеницы. В Англии [31] как наиболее перспективные рассматриваются белки сои, за ними следуют белки одноклеточных и пшеницы, далее — белки бобов, казеин, концентраты белка рыб и, наконец, белки других масличных культур и зеленых листьев (табл. 28). В нашей стране, по всей видимости, наиболее перспективно производство и переработка в искусственные продукты питания белков подсолнечника и хлопчатника, принимая во внимание масштабы производства этих культур (см. табл. 25 и 26). Другим перспективным видом белкового сырья может стать белок соевых бобов, если учесть планируемое на десятую пятилетку резкое увеличение производства сои, а также клейковина пшеницы, белки зеленых листьев и, наконец, белки картофеля, а также гороха и других бобовых культур.
БЕЛКИ ЖИВОТНОГО ПРОИСХОЖДЕНИЯ
Среди источников пищевого белка животного происхождения наибольший интерес представляют молоко, отходы молочной промышленности (производства сливочного масла, сыров и т. д.), отходы мясной промышленности, а также малоценные поропы рыбы и другие морепродукты. Хотя по объему потенциальных ресурсов эти источники белка многократно уступают растительным, они, однако, превосходят последние по биологической ценности, а при совместной с растительными белками переработке позволяют повысить биологическую ценность продуктов питания (принцип комбинирования белков) и потому представляют большой интерес с точки зрения производства и переработки в искусственные пищевые продукты.
В первой главе была отмечена относительно высокая степень конверсии белка растительных кормов в животные при производстве молока. Этим обусловлено то обстоятельство, что белки молока — один из самых дешевых белков животного происхождения.Их производство дополнительно удешевляется одновременным получением сливочного масла, сыров и других продуктов. Среднее содержание белка в молоке составляет 2,6—3,7% и зависит от породы скота, условий кормления, периода лактации и ряда других факторов. На основной белок молока — казеин приходится до 80% молочных белков, на сывороточные белки — около 12—17%, остальные азотсодержащие вещества молока (до 10%) представляют собой пептиды и аминокислоты.
Белок как сырье для полученияИПП
Казеин производят осаждением из обезжиренного молока. Чаще всего для этой цели используют коагуляцию казеина при рН 4,6—4,7 за счет добавления какой-либо кислоты, например соляной или уксусной, или же под действием молочной кислоты, образующейся в процессе молочнокислого брожения. Казеин получают также путем сычужной коагуляции (основной процесс при производстве сыров) или осаждения солями кальция. Наибольшее развитие получило производство кислотного казеина, так как этот процесс может быть осуществлен непрерывно и легче поддается автоматизации. Производство молочнокислого казеина требует большего времени для коагуляции белка. Кислотный казеин, осажденный в изоэлектрических условиях, естественно, нерастворим в воде. Его растворяют в слабых растворах щелочей. Высушивание таких растворов позволяет получать водорастворимый препарат казеина — казеинат.
Белки сыворотки, получаемой после осаждения казеина или при производстве сыров, могут быть отделены от лактозы и минеральных солей методом ультрафильтрации и электродиализа и выделены термическим осаждением или же путем распылительной сушки. В состав сывороточных белков в основном входят альбумины и глобулины, которые после тепловой денатурации (предварительный нагрев молока) осаждаются кислотой при рН 4,6—4,7. Наряду с казеином, казеинатом, сывороточными белками, производят также так называемые копреципитаты белков молока. Они представляют собой продукты соосаждения казеина и белков сыворотки. Копреципитаты получают осаждением белков молока после предварительного нагрева или же в присутствии ионов кальция. Для получения водорастворимых препаратов копреципитаты перед сушкой растворяют при перемешивании в растворе полифосфата. Вопросы производства молочных белков, их функциональные свойства и переработка рассмотрены в работах [83-84-93].
Казеин — один из наиболее биологически полноцепных и дешевых животных белков. Пищевой кислотный казеин обычно содержит 90—95% белка, 1—2% липидов, около 1% лактозы; пищевые казеинаты — около 85—88% белка, около 2% липидов и 0,5% лактозы. Кроме того, пищевой кислотный казеин, выпускаемый промышленностью, как правило, содержит значительные количества витаминов, минеральных солей и других ценных пищевых веществ. Биологическая ценность казеина обусловлена высоким и сбалансированным содержанием незаменимых аминокислот и сравнительно легкой атакуемостью ферментами желудочно-кишечного тракта. Тем не менее, казеин используется для питания приблизительно лишь на 30%. Он представляет собой один из наиболее ценных отходов пищевого производства [94—98]. То же относится и к другим белкам молока,
140 Глава третья
Казеин и казеинаты применяются в пищевой промышленности в качестве обогатителей, эмульгаторов и стабилизаторов пен при производстве диетических продуктов, колбасо-сосисочных и мучных кондитерских изделий. Белки сыворотки вводят в состав сыров, используют для обогащения продуктов детского питания, хлебобулочных изделий, напитков, а также в кондитерской промышленности, при производстве мороженого, кремов и т. д. Мировое производство казеина непрерывно растет (86 тыс. г в 1948— 1952 гг., 145,5 тыс. т в 1963 г.). Объем производства молочной сыворотки достиг в 1973 г. 74 млн. г, в том числе 3 млн. т при производстве казеина, однако до сих пор в большинстве стран теряется до 50% производимой сыворотки [85, 92].
Основное количество казеина находит применение не в пищевой промышленности, а в различных отраслях техники, прежде всего в бумажной промышленности (более половины мирового производства казеина [85]) для проклеивания и мелования бумаги, в качестве клеев, в фармацевтических и косметических производствах и при производстве пластмасс. Отметим, что и суммарный белок молока, мировое производство которого составляет около 6 млн. т (в виде обезжиренного молока, ил них 2 млн. т сухого молока), используется преимущественно для кормления животных (до 5 млн. т), так что для питания человека остается несколько больше 1 млн. т [23].
Основная причина, ограничивающая применение казеина и других белков молока для питания, заключается в их относительно невысоких функциональных свойствах. Они обладают низкой студнеобразующей способностью, имеют специфический запах и вкус, изменяют свойства при хранении и т. д. Поэтому в последнее время значительные усилия были направлены на решение вопросов регулирования функциональных свойств молочных белков, получения студней на основе казеина и разработку приемов его переработки в искусственные продукты питания. Учитывая высокие коэффициенты конверсии кормов при производстве молока (в 2—3 раза выше, чем при производстве мяса), переработка казеина, например, в искусственные мясопродукты позволяет в 2—3 раза увеличить потребление высококачественных животных белков.
Другим перспективным источником животного белка являются малоценные породы рыбы и другие морепродукты. Для хранения рыбы, которая портится быстрее других животных продуктов, помимо посола, копчения, охлаждения, очень широко используют сушку, особенно при переработке малоценных пород. Высушенную измельченную рыбу в виде рыбной муки используют в качестве кормов и даже удобрений. На эти цели в некоторых странах идет до 40—50% улова. Понятно поэтому, что большой интерес представляет производство белка из рыб малоцен-
Белок как сырье для полученияИПП
ных пород и некондиционной продукции, не находящей спроса. Производство изолятов и концентратов белка рыбы для пищевых целей получило развитие, в частности, в Скандинавских странах, США, Канаде, Англии, Индии, Перу и ПНР. С этой целью обычно измельчают филе или мороженную рыбу, обрабатывают растворителем для удаления липидов, после чего белок переводят в раствор и очищают переосаждениом. В качестве растворителей для удаления липидов используют изопропанол, гексан, хлорированные углеводороды. Применяют также поверхностно-активные вещества или же осуществляют промывку большими количествами воды, водными растворами солей или щелочей. Концентрат белка рыбы имеет высокую биологическую ценность. Возможность его хранения и переработки в пищу определяется в основном полнотой удаления липидов и компонентов запаха. Концентраты белка, лишенные запаха, стоят пока что, по крайней мере, в два раза дороже белков семян масличных. Они используются в ограниченных масштабах (порядка сотен тыс. г) для получения искусственных молочных и мясных продуктов, обогащения хлеба, макарон, мучных кондитерских и крупяных изделий.
Учитывая важность сокращения пищевых цепей океана, большой практический интерес представляют белки океанического рачка — криля и водорослей, в разработке процессов выделения которых получены интересные результаты [22, 23, 65, 71, 99—
107].
БЕЛКИ ДРОЖЖЕЙ, ВОДОРОСЛЕЙ И ДРУГИХ ОДНОКЛЕТОЧНЫХ
Микроорганизмы с древних времен используются для переработки пищевого сырья, например, при получении хлеба, кисломолочных продуктов, сыров, пива, вин, соусов и т. д. Их потребляют в пищу вместо с указанными продуктами в значительных количествах. 13 виде отдельных белковых продуктов применение дрожжей для питания и лечебных целей начато лишь в нашем веке [34—36, 108]. Оно получило развитие в европейских странах в период мировых войн и в послевоенное время. Дрожжи используют в качестве белково-витаминных и вкусовых добавок к пищевым продуктам (хлеб, котлеты, соусы и т. д.) и заменителей мясных экстрактов, обычно в виде гидролизатов.
Дрожжи, бактерии, одноклеточные водоросли и другие микроорганизмы в последнее время привлекают все возрастающее внимание в качестве практически неограниченного потенциального источника дешевого пищевого белка [21—23, 26, 27, 34—36, 65, 108—117]. Этот интерес вызван прежде всего тем, что скорость
| Глава третья |
биосинтеза белка у одноклеточных приблизительно в 1000 раз больше, чем у высших организмов. Ниже приведено время удвоения биомассы некоторых организмов из статистических данных [34,35]:
Бактерии, дрожжи, одноклеточные водоросли 1—6 час. Высшие растения: пшеница, стручковые, злаковые 1—4 недели Птица, цыплята 1 мес. Свиньи 2-4 » Коровы (производство молока) 2-4 » Крупный рогатый скот мясных пород до 5 лет
Явное преимущество одноклеточных в скорости биосинтеза белка связано, однако, с некоторым непринципиальным недостатком—высоким (до 15%) содержанием нуклеиновых кислот, от которых белок необходимо очищать.
Другое преимущество гетеротрофных микроорганизмов в сравнении с высшими растениями и животными заключается в том, что для их выращивания в качестве источника углерода и энергии пригодны разнообразные виды дешевого непищевого сырья, например, углеводы, спирты, углеводороды в виде газа, жидких парафинов, сырой нефти и т. д. Углеводороды при этом — более выгодный субстрат в качестве источника как энергии, так и углерода. В качестве сред для выращивания дрожжей большой интерес представляют отходы сельскохозяйственного и пищевых производств, а также сок зеленых листьев, травы и других растений (см. выше). Это обусловлено тем, что указанные виды сырья чрезвычайно разнообразны и невоспроизводимы по составу и содержанию белка. Поэтому их использование в качестве дешевых субстратов для выращивания дрожжей позволяет с одной стороны получать более однородное по составу и характеристикам белковое сырье в виде дрожжей, а с другой — более полноценный в пищевом отношении белок в удобной для извлечения и более концентрированной форме.
Важное значение имеет и то обстоятельство, что биомасса дрожжей и других микроорганизмов отличается высоким содержанием полноценного белка, 40—80% (табл. 29). Это выше, чем даже в семенах масличных культур, и в несколько раз выше, чем в мышечной ткани животных. Аминокислотный состав белка дрожжей и бактерий сходен и близок аминокислотному составу животных белков (см. табл. 29). Белок дрожжей обычно беден метионином, но богат лизином и треонином. Отсюда очевидна целесообразность его переработки вместе с белками зерновых культур. Добавление метионина повышает биологическую ценность белка дрожжей до уровня животных белков [34, 119].
Белок как сырье для полученияИПП
Наконец отметим, что производство биомассы микроорганизмов носит индустриальный характер со всеми его преимуществами (.см. гл. 1). Расчеты показывают [22, 26, 116], что переработка 50 млн. т нефти (около 2% ежегодной мировой добычи) позволяет произвести до 25 млн. т белка, количество, достаточное для питания 2 млрд. человек в течение года. Ресурсы производства белка здесь, следовательно, огромны. Для сравнения укажем, что максимально возможный уровень мирового улова рыбы 100 млн. т отвечает производству около 15 млн. т
белка.
Сведения о развитии микроорганизмов на углеводородах нефти и газа были получены ужо сравнительно давно [120], но практические работы в этом направлении развиваются с начала 60-х годов, на первом этапе в сиязи с проблемой донарафипи-зации нефти [26], а затем, и все более интенсивно, с целью получения кормового и пищевого белка [21—23, 26, 27, 65, 110—
119].
Широкие токсикологические и медико-биологические исследования на большом числе различных видов животных и людях
Таблица 29
Состав дрожжей и бактерий, выращенных на нормальных парафинах, и одноклеточной водоросли спируллины (вес.°/дна сухой вес) [34, 35J
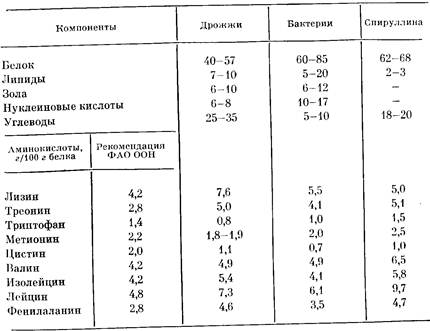
| Глава третья |
до сих пор не выявили каких-либо токсических эффектов при использовании очищенных белков (изолягов белка) дрожжей, выращенных на углеводородах [34, 65, Ml—ИЗ]. Более того, показано, что биологическая ценность изолятов белка дрожжей после добавления основной лимитирующей аминокислоты — метио-нипа заметно выпге, чем у казеина [119]. Производство дрожжей на углеводородах быстро осваивается промышленностью ряда стран [36, 71, 114] и уже сейчас превосходит по масштабам (многие сотни тысяч тонн) производство обычных пекарских дрожжей (150 тыс. т в 1965 г.). Их используют в виде кормов, но стоимость производства остается пока несколько более высокой, чем для обезжиренной соевой муки [23, 114].
Выделение пищевого белка связано с необходимостью разрушения оболочек дрожжевых клеток. Для этого предложены механические методы, например кавитационная мельница, работающая в среде органического растворителя, что позволяет одновременно с разрушением клеток экстрагировать липиды и ряд нежелательных примесей [110, 117, 121]; обработка дрожжей в нагретом пищевом масле [122], что приводит к вскипанию воды, разрушению клеток, удалению примесей перегонкой с нодяпым паром и растворением в масло; метод кратковременной обработки биомассы дрожжей нагретой соляной кислотой [123] и др. До сих пор, однако, не налажено производство дешевого и пригодного для переработки в искусственные продукты питания изо-лята белка дрожжей. Это обусловлено недостаточным научно-техническим уровнем развития экономичных и эффективных методов разрушения клеточных оболочек, отделения нуклеиновых кислот, очистки и выделения белков с необходимыми функциональными свойствами. Переработку дрожжевых белков в искусственные продукты питания затрудняет также их высокая гетерогенность как преимущественно функциональных белков клетки, т. е. выполнявших функции ферментного катализа, структурную и др. Однако эти вопросы, очевидно, могут быть решены в ближайшее время, учитывая огромное значение дрожжевых белков как источника пищевого белка и растущий в связи с этим интерес к изучению их функциональных свойств и методов переработки.
Так, в последние годы были начаты исследования прядомости растворов дрожжевых белков [124] и других функциональных
свойств [19], а также показана принципиальная возможностьихрегулирования [125].
Другим интересным источником белка служат одноклеточные и многоклеточные водоросли, производство которых для кормовых и пищевых целей приобретает и последнее время все возрастающее значение [35, 36, 111, 112]. К ним относятся прежде всего синезеленые (спируллина) и зеленые (хлорелла, сцепедес-
Белок как сырье для получения111111
мус и др.) водоросли. При этом обращают внимание па относительно высокое содержание белка в водорослях, обычно до 50%
на сухой вес и выше.
Однако основная причина интереса к водорослям заключается
в том, что эти фотосинтезирующие организмы трансформируют солнечную энергию в пищу с эффективностью, на два порядка более высокий, чем наземные растения (см. стр. 142). Этот источник белка интересен поэтому и с экологической точки зрения, так как культивирование водорослей на площади 1 м2 дает столько же пищи, сколько ее производится традиционными методами приблизительно на 0,5 га культивируемой земли. Поэтому культивирование водорослей в естественных и искусственных водоемах открывает большие возможности для производства белка и других пищевых веществ. В первой главе была также показана чрезвычайно высокая продуктивность океана относительно первичной растительной продукции. Интересна также возможность одновременного с белком получения из водорослей кислых поли-сахаридов — важного компонента искусственных продуктов питания, обеспечивающего переработку многих белков (см. гл. II). В последнем случаи интерес, по-видимому, также представляют
бурые и красные водоросли.
Хотя некоторые водоросли (например, хлорелла) производятся для кормовых целей, их практическое использование как мощнейшего источника дешевого пищевого белка тормозится явно недостаточной изученностью методов выделения из водорослей белка с необходимыми функциональными свойствами и его переработки. Исследования здесь едва лишь начаты, но уже теперь совершенно очевидна чрезвычайная перспективность этого направления. Работы в этой области ограничены пока что определением запасов, изучением продуктивности водорослей, технологией культивирования и медико-биологическим исследованием их применения для питания. Они, кроме того, распространяются прежде всего на изучение хлореллы, сценедесмуса и спируллины среди чрезвычайно большого разнообразия водорослей.
Интересна, в частности, водоросль спируллина, произрастающая в озере Чад и некоторых других водоемах Африки. Она с глубокой древности потребляется в пищу племенами, живущими по берегам этих водоемов, в количестве (в расчете на белок) до 40 и в день на человека. Спируллину собирают, сушат на солнце и применяют для получения лепешек, которые используют в пищу. Эта синезеленая водоросль имеет вид волокон спиральной формы, длиной 0,3—0,5 мм. По размерам она превосходит хлореллу и сцонсдесмус легко отделяется от культуральной жидкости центрифугированием, но уступает по продуктивности сценедесмусу. С 1 л(2 поверхности бассейна можно получать 10—15 з в день сухих водорослей. Спируллииа легко отфильт-
146 Глава третья
ровывается и высушивается. Продукт представляет собой порошок темно-зеленого цвета, содержащий около 65% белка и большое количество витаминов (кроме D). Белок спируллины дефицитен по метионину. Он тем не менее имеет высокую биологическую ценность (КЭБ более 90% от казеина) и хорошо усваивается организмом. Он может быть использован для питания в больших количествах. В 1972 г. было начато производство спируллины вблизи Мехико (оз. Текскоко, 1 г в день). Ее используют в пищу в виде бисквитов. Большим преимуществом этой культуры, очень существенным для ее культивирования в открытых водоемах, является то, что она растет в солевых и щелочных средах (оптимум рН 8,5—11). Эти условия, с одной стороны, препятствуют бактериальному заражению водоемов, где выращивается спируллина, а с другой — благоприятны для полного использования СОа, который может вводиться в виде карбонатов или бикарбонатов. Азот может поставляться в виде аммонийных солей. Это, таким образом, чрезвычайно перспективная культура для производства белка индустриальным методом.
АМИНОКИСЛОТЫ
Выше было показано, что один из методов получения искусственных продуктов питания высокой биологической ценности при переработке нетрадиционных видов белков, особенно растительных, заключается в обогащении продуктов недостающими незаменимыми аминокислотами. Это особенно важно при производстве искусственных продуктов, имитирующих продукты животного происхождения, так как позволяет доводить их биологическую ценность до уровня натуральных аналогов и резко увеличить объем производства полноценной белковой пищи. Отметим, что помимо обогащения белкового сырья и искусственных пищевых продуктов отдельными незаменимыми аминокислотами, последние используются для питания также и в виде смесей. Смеси аминокислот могут быть добавлены к продукту для повышения биологической ценности как за счет корректировки аминокислотного состава, так и для повышения общего содержания аминокислот, а кроме того, и для улучшения вкусовых свойств. Смеси аминокислот находят также применение в качестве синтетических диет различного назначения, например для пар-энтерального питания, в тех случаях, когда прием и усвоение традиционной пищи нормальным путем невозможны. В качестве вкусовых добавок, помимо смесей аминокислот и композиций на основе реакции Майара, используют также и отдельные аминокислоты и пептиды. Наиболее широкое применение получила глютаминовая кислота в виде натриевой соли — глютамината нат-вия.
Белок как сырье для полученияИПП
При обогащении продуктов питания аминокислоты обычно добавляют в количествах от долей процента до 1—1,5%. В результате стоимость продукта увеличивается незначительно, биологическая же ценность может при этом возрастать в 1,5—3 раза.
Таким образом, в связи с проблемой переработки нетрадиционных белков в полноценные искусственные продукты питания еще более возрастает значение задачи производства значительных количеств незаменимых аминокислот, смесей аминокислот, а также вкусовых и ароматизирующих композиций на их основе.
Таблица 30 Мировое производство аминокислот[130}
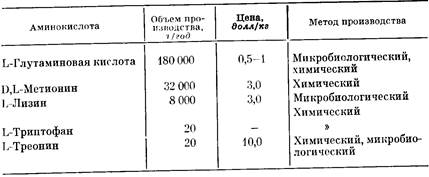
Смеси аминокислот могут быть получены кислотным гидролизом белков, прежде всего белковых отходов пищевой промышленности, а также ферментативным гидролизом, в частности автолизом дрожжей. Они могут быть очищены от посторонних примесей и выделены методом ионообменной хроматографии. Состав таких смесей можно корректировать добавлением отдельных
аминокислот.
Индивидуальные аминокислоты обычно получают микробиологическим и химическим синтезом или их комбинацией. Метод химического синтеза, по-видимому, наиболее универсален и наиболее рентабелен экономически при больших масштабах производства. Вопросы разделения рацематов аминокислот, получаемых в результате их химического синтеза, рассмотрены в работах [110, 126 ]. Сведения о масштабах и методах производства отдельных аминокислот, а также их стоимости приведены в табл. 30.
Проблема производства аминокислот в промышленно развитых странах считается практически решенной, и объем их выпуска ограничен лишь спросом. Основные направления исследований в этой области связаны, с одной стороны, с разработкой более эффективных, экономически выгодных процессов их полу-
148 Глава третья
чения, очистки и выделения, с другой — с изысканием приемов использования аминокислот и их смесей. Эти вопросы подробно анализируются в работах [21, 127—134].
В заключение необходимо еще раз подчеркнуть, что накопленный к настоящему времени опыт использования нетрадиционных видов белка для питания человека со всей определенностью свидетельствует о том, что решающим звеном в цепи возникающих при этом проблем является получение на основе этих белков пищевых продуктов, привлекательных для потребителя. Функциональные свойства, стандартность и стоимость должны, следовательно, обеспечивать возможность переработки белка в искусственные продукты питания экономически эффективными методами. При этом необходимо учитывать, что речь идет о про -дуктах массового потребления, а также тот факт, что именно сопоставление стоимости искусственных и традиционных продуктов в решающей мере определяет целесообразность производства искусственной пищи. Функциональные свойства белкового сырья определяют при этом возможность, стоимость, а следовательно, и целесообразность его переработки в различные формы искусственной пищи и, в конечном счете, масштабы производства и потребления белка. Это положение можно дополнительно продемонстрировать на примере казеина — одного из наиболее полноценных белков, пригодность и целесообразность использования ь пищу которого не вызывает никаких сомнений. Этот белок к тому же относительно дешев, и тем не менее его используют для питания лишь в очень малой степени. Причина заключается в том, что функциональные свойства казеина весьма невысоки. В то же время пищевая желатина — продукт с минимальной пищевой ценностью и в несколько рая более дорогой, чем казеин, производится во все возрастающих количествах, так как обладает высокими функциональными свойствами и обеспечивает переработку и потребление многих пищевых веществ и продуктов в виде желейных кондитерских изделий, заливных блюд и т. д. То же относится и ко всем другим белкам. Например, как было показано выше, стоимость белков масличных в виде изолятов выше, а биологическая ценность всегда существенно ниже, чем в составе обезжиренной муки. Тем не менее изоляты белков масличных, в отличие от обезжиренной муки, полностью потребляются в пищу.
Современный дефицит пищевого белка обусловлен не недостатком ресурсов белка, которые, как было показано выше, практически безграничны, а прежде всего недостаточным на сегодня научно-техническим уровнем в области выделения и переработки белков из нетрадиционных источников в искусственные продукты питания.
Белок как сырье для получения ИПП
ЛИТЕРАТУРА
1. К. F. Mattil.—J. Am. Oil Chem. Soc., 48, N 9, 477 (1971).
2. D. W. Johnson— J. Am. Oil Chem. Soc., 47, N 7, 402 (1970).
3. F. E. Horan— J. Am. Oil Chem. Soc,51, N 1, 67 (1974).
4. Л. C. Eldridge, Р. К. Hall, W. J. Wolf—Food Technol., 17, 120 (1963).
5. N. Catsimpoolas, E. W. Meyer— Cereal Chem,, 47, 559 (1970).
6. /. /. Kelley, R. Pressey— Cereal Chem.,43, 195 (1966).
7. A. M. Pearson, M. E. Spooner, G. R. Hegarty, L. I. Bratzler.— Food Technol.,19, 1841 (1965).
8. /. Rakosky, Jr— J. Agr. Food Chem., 18, N 6, 1005 (1970).
9. /. Rakosky, Jr— J. Am. Oil Chem. Soc.,51, N 1, 123 (1974).
10. S. Kakuchi— Ibid., p. 189.
11. E. W. Meyer.— J. Am. Oil Chem. Soc., 48, N 9, 484 (1971).
12. W. J. Wolf— J. Agr. Food Chem., 18, N 6, 969 (1970).
13. W. J. Wolf, J. C. Cowan. Soybeans as a food source. Ohio, CRC Press., 1971.
14. W. J. Wolf, A. K. Smith— Food Technol.,15, N 5, 4, 12 (1961).
15. S. J. Circle, А. К. Smith.—In: «Seed proteins». G. E. Inglett (Ed.). West-port, Connecticut, AVI Publ. Сотр., 1972, ch. 17, p. 242—254.
16. А. К. Smith, S. J. Circle.— In: «Soybeans: Chemistry and Technology», v. 1. Proteins. A. K. Smith, S. J. Circle (Eds). Westport, Connecticut, AVI
Publ. Co., 1972, ch. 9, 10, p. 327-346.
17. E. E. Burns, L. J. Talley, B. J. Brammett— Cereal Sci. Today,17, N 9,
287 (1972).
18. P. S. La, J. E. Kinsella—J. Food Sci.,37, 94 (1П74).
19. P. Vananuvat, J. E. Kinsella.— J. Agr. Food Chem., 23, N 4, 613 (1975).
20. L. D. Satterlee, M. Bemhers, J. G. Kendrick— J. Food Sci.,40, N 1, 81
(1975).
21. А. Н. Несмеянов, В. M. Целиков, С. В. Рогожин и др.—Вестник АН ^
СССР,№ 1,29 (1969).
22. A. Uzzan.— Chim. ot Ind., 94, N 4, 306 (1965).
23. International action to avert the impending protein crisis. E/4343/Rev. 1.
New York, United Nations, 1968. '-M. Processed plant protein foodstuffs. A. M. Allschnl. (Ed.). N. Y., Acad.
Press, 1958.
25. Л. M. Allfchnl.— In: «Now protein foods», v. 1. A. M. Altschul (Ed.). Technology. New York — London, Acad. Press, ch. 1, 1074, p. 1—40.
26. A. Champagnat, C. Vernet, В. Laine, J. Filosa.— Nature,197, 13 (1963).
27. A. T. McPherson— Chem. Eng. Progr.,61, N 10, 101 (1965).
28. D. В. Walker, F. E. Horan, R. E. Burket— Food Technol.,25, N 8, 55 (1971).
29. A. S. Claasi— Ibid., p. 63.
30. Я. fflosterm.ei/er.—Milchwissonschafl, 26, N 8, 465 (1971).
31. B. J. F. Hudson—Chem. Ind., 6, 251 (1972).
32. /. Dasek.— Chem. Rnndsch., 27, N 40, 19 (1974).
33. /. Bombal, L. N'Diaye, F. Fenardji, R. Ferrando.— Rev. Med. vet.125, N 4.
469 (1974).
34. /. Maaron— J. Int. Vitaminol., 39, N 2, 212 (1969).
35. /. Maiiron.— Bibl. Nutr. Diet,16, 169 (1971).
36. /. Mauron—ВШ. Nutr. Diet.,21, 147 (1975).
37. T. Siaron— Rev. Ital. sost. grasse,51, N 7, 225 (1974).
38. Textured vegetable protein. Miles Laboratories. Elkhart, Indiana, 1973.
39. /. Lefebvre.—Cah. nntr. diet,4, N 4, 45 (1969);5, N 4, 46 (1971).
40. R. W. Fischer.— J. Am. Oil Chom. Soc.,51, N 1, 178 (1974).
41. R. L. Kellor.—^. Am. Oil Chem. Soc., 48, N 9, 481 (1971).
42. M. D. Wilding—Ibid., ]). 489.
43. A. K. Smith, S. J. Circle.— In: «Soybeans: Chemistry and Technology»,
Глава третья
v. I, ch. 1. Historical background. А. К. Smith, S. J. Circle (Eds). West-port, Connecticut, AVI Publ. со., 1972, p. 1—27.
44. Т. Watanabe, H. Ebrine, M. Okada— In: «Now protein foods». A. M. Alt-schul (Ed.). New York—London, Acad. Press, 1974, ch. i», p. 415—450.
45. Т. Watanabe— 1. Am. Oil Chem. Soc.,51, N 1, 111 (1974).
46. Д. /. Dimler— J. Am. Oil Chein. Soc., 48, N 8, 400 (1971).
47. /. Coppock— J. Am. Oil Chem. Soc.,51, N 1, 59 (1974).
48. /. Baltes.— Ibid., p. 52.
49. W. Pringle— Ibid., p. 74.
50. К. F. Mattil.— Ibid., p. 81.
51. /. /. Rackis— Ibid., p. 161.
52. Л. L. Kellor— Ibid., p. 77.
53. E. H. M. Greuell— Ibid., p. 98.
54. Л С. Wodard— Fed. Proc.,31, 695 (1972).
55. /. С. Wodard, D. D. Short— J. Nutr.,103, N 4, 569 (1973).
56. E. L. Butz— J. Am. Oil Chem. Soc.,51, N 1, 57 (1974).
57. M. D. Wilding— Ibid., p. 128.
58. W. W. Thulin, S. Kuramoto— Food Technol.,21, N 2, 64 (1967).
59. Meat menagement, aug., 1970, 24.
60. Л. F. Robinson—Food Technol.,26, N 5, 59 (1972).
61. F. E. Horan.—ln: «New protein foods», v. 1, ch. 8. A. M. Altschul (Ed.). New York—London, Acad. Press, 1974, p. 367—411.
62. И. А. Вайнтрауб. Докт. дисс. АН МолдССР. Кишинев, 1970.
63. N. G. Hardinge, И. Croks.—l.Am. Diet. Ass.,43, N 6, 545, 550 (1963);45,N6,537 (1964).
64. S. D. Koury, R. E. Hodges—L Am. Diet. Ass.,52, N 6, 480 (1968).
65. The biological efficiency of protein production, ed. J. G. W. Jones, Cambridge. Univ. Press, 1973, p. 84, 303—363, 358.
66. К. D. Schwenke, В. Raab— Nahrung,17, N 3, 373 (1973).
67. К. D. Schwenke, B. Ender, В. Raab.— Ibid., p. 579.
68. К. D. Schwenke, В. Raab, J. Uhlig e. a.— Nahrung,17, N 8, 791 (1973).
69. К. D. Schwenke, M. Schultz e. a— Nahrung, 18, N 6-7, 709 (1974).
70. К. D. Schwenke— Nahrung,19, N 1, 69 (1975).
71. E. V. Andersen— Chem. Eng. News,49, N 10, 19 (1971).
72. Food Technol., 27, N 8, 66 (1973).
73. Bai-Xuan-Nhuan— Oleagineux,26, N 11, 713 (1971).
74. A. M. Altschul— Chem. Eng. News, 47, N 49, 68 (1969).
75. Chem. Rundsch., N 7, 207 (1965).
76. /. Hallo— Austral. Chem. Eng.,10, N 2, 9 (1966).
77. N. W. Pirie.—Chem. Eng., N 26, 864 (1968).
78. N. W. Pirie. Leaf Protein: Its agronomy, preparation, quality and use, 1BP Handbook N 20. Oxford and Edinburgh, Blackwell Sci., 1971.
79. С. В. Coulson— Chem. Ind., N 31, 1015 (1970).
80. 7. E. Kinsella— Chem. Ind., N 17, 550 (1970).
81. D. B. Arkcoll, M. N. J. Davys— Chem. Eng.,251, 261 (1971).
82. Д. Я. Edwards, E. R. Miller, D. de Fremery e. a.— J. Agr. Food Chem.23N4,620 (1975).
83-84. П. Ф. Дьяченко. Труды ВНИМИ, № 19, M., Пишепромиздат, 1959
85. Dairy Ind.,30, N 12, 929 (1965).
86. /. A. MacAlpine.—J. Soc. Dairy Technol.,24, N 4, 142 (1971).
87. E. J. Mann— Dairy Ind.,36, N 8, 470 (1971).
88. E. 1. Mann— J. Soc. Dairy Technol., 24, N 4, 145 (1971).
89. J.-C. Jacquemet— Ind. Alim. Agr., 89, N 9-10, 1301 (1972).
90. Л Guerin, Ch. Alais.— Ind. Alim. Agr.,91, N 4, 343 (1974).
91. P. Devos— Rev. lait franc., N 328, 131, 133 (1975).
92. Dairy Ind.,39, N 12, 466 (1974).
93. G. W. Smith.— Milk. Ind., 76, N 2, 25 (1975).
Белок как сырье для голучения ИПП
94. H. Яременко.— Молочная пром., № 3, 25 (1963).
95. Р. Давидов. Молочные продукты в отходах.— Правда, 22.2.1965.
96. А. Кац. Белковые резервы (об использовании обезжиренного молока для производства пищевых продуктов).— Известия, 1.10.1968.
97. С. Антонов. Критерий — спрос.— Правда, 5.3.1968.
98. M. Т. Денщиков. Отходы пищевой промышленности и их использование. M., Ппщепромиздат, 1963, с. 553—560.
99. С. С. Школьникова. Производство и использование рыбного белкового концентрата. M., ВНИРО, 197).
100. D. Sen— J. Food Sci. Technol., 3, N 4, 142 (1966).
101. G. Snyder.— Food Technol., 21, N 8, 56, N 9, 70 (1967).
102. D. Swendsen.—Chem. Eng.,74, N 18, 186 (1967).
103. M. Moorjani, N. Lahirg.— Fcod Technol.,24, N 1, 56 (1970).
104. M. Caiozzi.— Food Technol., 22, N 6, 100 (1968).
105. /. Connell— Food Technol.,23, N 2, 72 (1969).
106. W. Chapman— Food Technol., 20, N 7, 110 (1966).
107. H. V. Semling, Jr— Canner/Packer,135, N 1, 56 (1966).
108. Я. Gounelle, S. So f man.— Ann. Nutr. Alim.,10, N 5-6, 253 (1956).
109. N. Lyall.— Food. Eng. Food Ind. News, 4, N 3, 3 (1966).
110. С. В. Рогожин. Докт. дисс. M., ИОХ АН СССР, 1971.
111. Медико-биологические исследования углеводородных дрожжей. Под " ред. А. А. Покровского. M., «Наука», 1972, с. 9—58.
112. Single-cell protein. R. J. Mateles, S. R. Tannenbaum (Eds). Cambridge, Mass., MIT Press, 1968.
113. S. R. Tannenbaum—•Food TechnoL,25, N 9, 98, 103 (1971).
114. R. Crahmer.—Wws. und Fortschr.,22, N 8, 368 (1972).
115. M. Cepede.— Coop. techn., N 56-57, 35 (1969).
116. Л. Champagnat.—In: «Food». San Francisco, W. H. Freeman со., 1973,
p. 254.
117. S. W. Rogosin, W. A. Sergejew, A. M. Mamzis, D. G. Walkowski— Nah-rung,19, N 1, 23 (1975),19, N 9-10, 961 (1975).
118. S. G. Kharatyan, T. W. Antonowa, A. I. Wolnova, W. M. Belikow— Nah-rung,19, N 1,61 (1975).
119. Б. П. Суханов. Канд. дисс. I Московский медицинский ин-т, 1974
120. Э. Бирштехер. Введение в микробиологию нефтяной промышленности Л., Гостоптехиздат, 1957.
121. С. В. Рогожин, А. M. Мамцис, Д. Г. Вальковский.— Прикл. биохимия и i микробиол., 6, № 6, 638 (1970);10, № 6, 841 (1974).
122. D. G. I. (Danish Fermentation Ind). Copenhagen. Inform. Sheet Pl-4, 1967.
123. H. Samejima, H. Teranishi, T. Kogawa (Kyowa Fermentation Ind. со.). Пат. Японии 7328 (1973).
124. F. Haang.Cho Kyan Rha.— Biotechnol. Bioeng.,14, 1047 (1972).
125. W. B. Tolstogusow, E. S. Wainerman, S. W. Rogoshin e. a.—Nahrung, 18, N 4, 355 (1974).
126. В. А. Даванков. Докт. дисс. M., ИНЭОС АН СССР, 1975.
127. А. H. Несмеянов, В. M. Беликов. Проблемы синтеза пищи. M., «Наука»,
1965.
128. Д. M. Великое, Т. Л. Бабаян— Успехи химии,40, № 5, 828 (1971).
129. Э. Н. Сафонова, В. M. Беликов.—У cue-in химии, 36, 913 (1967);43, № 9, 1575 (1974).
130. В. М. Беликов.— Вестник АН СССР, № 8, 33 (1973).
131. В. М. Беликов.— Мир науки, 18, № 3, 17 (1974).
132. В. М. Беликов, В. К. Лотов, В. А. Циряпкин, В. А. Сергеев.— Микробиол. пром., № 3, 1 (1976).
133. G. Л. Jansen.— In: «New protein foods», v. 1, ch. II. A. M. Altschu! (Ed.). New York — London, Acad. Press, 1974, p. 40—121.
134. H. Milsnda, K. Ynsamolo.— Ibid., ch. Ill, p. 121—156.
ГЛЛВЛ ЧЕТВЕРТАЯ
СПОСОБЫ ПОЛУЧЕНИЯ ИСКУССТВЕННЫХ ПРОДУКТОВ ПИТАНИЯ
Новое направление производства пищи, как показано, выше, может иметь успех только в том случае, если искусственные продукты питания станут продуктами массового потребления, т. е. дешевыми, привлекательными для потребителя и удобными в использовании. Важно также, чтобы их состав отвечал представлениям о рациональном питании.
Исследования в области переработки белков в искусственные продукты питания получили быстрое развитие за последние 7— 10 лет во многих странах, прежде всего ввиду очевидной экономической целесообразности промышленного производства пищи на основе растительного и несельскохозяйственного белкового сырья, недостатка полноценной белковой пищи, а также в связи с растущей потребностью в продуктах для детского, диетического и профилактического питания. В результате этих исследований разработаны методы получения и организовано промышленное производство ряда искусственных продуктов питания массового потребления, таких, как искусственные мясные, молочные изделия, крупы и ряд других.
Необходимо отметить, что развитие научно-технических исследований по проблеме получения искусственных продуктов питания отличалось известным своеобразием. Прежде всего до недавнего времени эта проблема решалась как проблема переработки белка соевых бобов, и лишь в последнее время начинают вырисовываться общие способы переработки белка. Отметим также, что подавляющее большинство результатов исследований п области получения искусственных продуктов питания ввиду ее исключительного экономического значения изложено в патентных публикациях. Последние защищают главным образом общие принципы, а не режимы отдельных стадий процессов, что характерно для начального этапа практического развития какой-либо новой области техники. В последнее время основное внимание было обращено на разработку способов получения наиболее дорогостоящих белковых продуктов — искусственных мясопродуктов, а также искусственной зернистой икры. В этих направлениях, наряду с производством искусственных молочных продуктов, до-
Способы полученияИПП 153
стигнут наибольший успех. Несмотря, однако, на успехи в производстве различных форм искусственной пищи, методы регулирования качества новых продуктов питания разработаны еще явно недостаточно. Исследования в этом направлении только начинают развиваться (см. гл. II). То же относится к способам регулирования функциональных свойств белка и к методам получения искусственных продуктов с достаточной универсальностью по белку.
Способы получения различных форм искусственной пищи различаются как приемами формования пищевых систем (получение волокон, слоев, гранул и т. д.), так и по способам структурирования, позволяющим фиксировать форму искусственного продукта питания. При анализе процессов получения искусственных продуктов питания представляется, однако, целесообразным классифицировать их по типу конечного продукта, поскольку для каждой из новых форм пищи характерны определенные требования к функциональным свойствам белка, составу перерабатываемых жидких систем, а также специфические режимы их формования и структурирования. Рассмотрим поэтому раздельно способы получения искусственных молочных, крупяно-макаронных, мясных и других изделий.
ИСКУССТВЕННОЕ МОЛОКО И МОЛОЧНЫЕ ПРОДУКТЫ
Как было показано в первой главе, степень конверсии растительных и других белков через посредство животного в белки молока в 2—3 раза выше, чем в белки мяса. Естественно поэтому, что производство искусственных молочных продуктов на основе белков различного происхождения способно в значительно меньшей мере расширить общие ресурсы белка для питания, чем, например, производство искусственного мяса. Кроме того, натуральное молоко ввиду его низкой себестоимости и высоких пищевых качеств будет, по-видимому, медленнее заменяться искусственным, нежели другие пищевые продукты массового потребления. С другой стороны, производство молока, так же как и других жидких продуктов, легче поддается автоматизации, чему благоприятствует большая стандартность и простота обработки. Наконец, производство и переработка молока ориентированы на получение масла, в результате чего значительная часть молока, как показано выше, не используется для питания. В этой связи отметим также, что заменитель сливочного масла — маргарин по существу представляет собой один из первых искусственных продуктов питания, производимый промышленностью во все возрастающих масштабах,
154 Глава четвертая
Производство искусственного молока и других молочных продуктов в промышленно развитых странах организуется в целях детского, диетического и лечебного питания, а также питания населения с низким уровнем дохода, при использовании критериев состава и стоимости. Лишь в развивающихся странах производство искусственных молочных продуктов способно внести заметный вклад в решение проблемы белкового дефицита.
Методы получения пищевых эмульсий типа «масло в воде» с использованием низкомолекулярных поверхностно-активных веществ, а также белков и полисахаридов в качестве эмульгаторов сравнительно хорошо разработаны [1—б]. Основные научные проблемы в этой области связаны скорее с получением дезодорированных белков масличных с необходимыми функциональными свойствами. Поэтому, несмотря на то, что масштабы производства этой формы искусственных продуктов питания весьма значительны, ограничимся кратким рассмотрением назначения основных видов искусственных молочных продуктов и несколько подробнее рассмотрим способы производства искусственного молока на основе растительных белков.
Можно выделить три основные категории искусственных молочных продуктов:
1. Продукты, в которых полностью или частично заменены энергетические компоненты (липиды, углеводы).
2. Продукты, в которых полностью или частично заменены белковые компоненты.
3. Продукты, не содержащие компонентов натурального молока.
В первом случае существенны два момента. С одной стороны, значительная часть взрослого населения не усваивает молочный сахар — лактозу и поэтому не может потреблять натуральное молоко в значительных количествах. В некоторых районах мира (Африка, Азия и Америка) это относится к большинству населения [7, 8]. Отсюда возникает необходимость удаления из молока лактозы или же выделения белков для их повторного использования в виде искусственного молока. Это можно осуществить, например, методом ультрафильтрации [9]. С другой стороны, биологическая ценность липидов в значительной мере обусловлена содержанием в них полиненасыщснных жирных кислот (линолевой, линоленовой, арахидоновой), которые относятся к числу незаменимых факторов питания. Главный их источник — растительные масла. Последние содержат также много фосфатидов и токоферолов — важных компонентов питания [ 10— 13]. Поэтому в диетических целях и для получения продуктов с пониженной калорийностью (молоко, сливки, пасты, кремы, мороженое, сыры) заменяют молочный жир растительными маслами [3, 14—17].
Способы полученияИПП
Второй тип продуктов предназначен в основном для детского питания. Здесь тоже имеется два рода проблем. Использование коровьего молока для питания грудных младенцев и детей, страдающих желудочными заболеваниями, затруднено тем, что повышенное содержание в нем ионов кальция приводит к образованию в желудке ребенка плотного, трудноперевариваемого коагулята белка. Для полной или частичной замены ионов кальция на ионы натрия или калия молоко, цельное или обезжиренное, пропускают через колонки с ионообменными смолами. Используют также щелочные растворы казеина (коровьего молока), к которым после декальцификации на катионите добавляют лецитин и затем эмульгируют растительные масла. При створажи-вании такое молоко дает нежные, хорошо перевариваемые коагуляты. Обычно все виды ионитного молока обогащают витаминами и сахарами.
Второй аспект проблемы связан с тем, что ряд белков молока может быть аллергенами для детей и взрослых. С целью устранения аллергических свойств этих белков предложено денатурировать их в обезжиренном молоке путем нагрева или же заменять па белок сои [18, 19].
При получении искусственного молока и молочных продуктов первых двух типов в качестве растительных масел (для замены молочного жира) обычно используют соевое, кукурузное, хлопковое, кокосовое или подсолнечное, в качестве белков — кислотный казеин, казеинаты натрия, калия или кальция, сумму белков молока или же растительные белки. Эмульгаторами обычно служат белки, пектины, альгинат, лецитин и т. д.
В последнее время для расширения сбыта искусственного и натурального молока большое распространение получило производство на их основе кондитерских желейных изделий и десертов. В качестве студнеобразователей используют желатину, а также пектины, каррагенипы, альгинат и другие кислые полисахариды. Заменители молока широко используются и для производства мороженого. В США диетический заменитель сливочного мороженого «меллорин» готовят на основе молочных продуктов, в которых молочный жир заменен растительным. В штатах Техас и Калифорния потребление меллорина составляет соответственно более 40% и более 15% от общего потребления мороженого
[20, 21].
Наиболее интересен третий тип искусственных молочных продуктов как в плане современной проблемы белкового питания, так и в историческом отношении. Эти белковые искусственные пищевые продукты были, видимо, первыми из всех известных и используемых для питания. В настоящее время они производятся во все возрастающих масштабах на основе растительных белков, преимущественно белка сои.
156 Глава четвертая
Выше отмечено, что белок сои применяют в питании уже несколько тысячелетий. Способ получения молока и творога на основе сои был открыт более 2000 лот назад китайским философом Ван Нан-цзе [22—29]. Соевые бобы вымачивают и затем диспергируют в воде. Полученную дисперсию фильтруют, и приготовленное таким образом соевое молоко кипятят, охлаждают и коагулируют хлористым магнием. Отжатый на полотне коагулят
Таблица 37 Состав (в %) соевого творога тофу и натурального мяса [22]
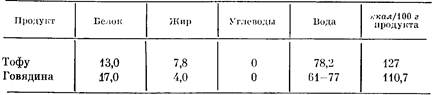
соевого белка, белого или голубовато-серого цвета, называют соевым творогом теофу (в Китае), тофу (в Японии), данфу (в Индокитае). Соевый творог иногда называют растительным мясом [22]. Данные о его составе приведены в табл. 31. Соевый творог используют непосредственно в пищу, а также для приготовления различных блюд, добавляют в супы или же жарят в масле. Состав и свойства тофу сильно зависят от состава исходных бобов сои, условий экстракции и коагуляции белка, которая теперь чаще производится с помощью солей кальция. В Японии этот процесс в настоящее время стандартизован [27, 28]. Помимо тофу в Японии производят ряд других национальных продуктов на основе сои (табл. 32). Замораживанием, оттаиванием, дегидратацией и сушкой соевого творога тофу получают кори-тофу, очень интересный продукт пористой структуры. Исследование процесса получения этого традиционного для Японии продукта позволило недавно разработать оригинальные методы получения изолята белка сои, искусственных молочных и мясных продуктов. Было показано, что при замораживании водной дисперсии соевого белка он теряет растворимость. Подбор концентрации раствора белка и режима замораживания — оттаивания позволяет регулировать структуру и физические свойства образующихся белковых губок [27]. Промывка губки водой позволяет очистить белок от углеводов и специфических вкусовых компонентов соевых бобов с получением концентратов или изолятов белка соевых бобов. Последующая дезинтеграция белковой губки в воде с добавлением поваренной соли, глюкопата кальция, сульфата железа и витаминов Л, С и D позволяет получать искусственное молоко
Способы получения ИПП
с высокими пищевыми и вкусовыми свойствами [30]. Получение аналогичным путем заменителей мяса рассмотрено ниже.
Процесс получения соевого молока в послевоенное время был освоен в США, Англии и Канаде [23]. Основные технологические операции показаны на рис. 29. Поело удаления оболочек соевые бобы измельчают в воде, центрифугируют суспензию для удаления крупных частиц — остатков соевых бобов, после чего нагревают для инактивации ингибиторов ферментов. Для улучшения
Таблица 3'2
Производство (в 1000 т} традиционных пищевых продуктов на основе соевых бобов и обезжиренной соевой муки. Япония [27]
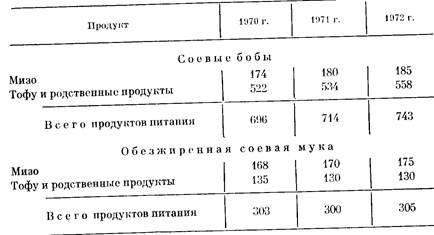
вкуса и биологической ценности продукта добавляют сахар, ме-тионин, соли кальция, железа и ароматизаторы. Готовый напиток разбавляют до нужной консистенции и стерилизуют в бутылках.
Выпускают также сухое соевое молоко.
В последующий период развитие производства искусственных молочных продуктов протекало различными путями в разных странах. Основные направления совершенствования процесса относятся к аппаратурному оформлению и режимам экстракции белка бобов сои, его дезодорировапию, регулированию функциональных свойств, прежде всего способности эмульгировать растительные масла. По мере развития производства обезжиренной муки, концентратов и изолятов белка соевых бобов они становятся основными видами белкового сырья для производства как искусственных молочных, так и традиционных пищевых изделий, таких, как тофу, которые до войны изготавливали лишь из бобов сои. Их преимущество перед соевыми бобами заключается в
158 Глава четвертая
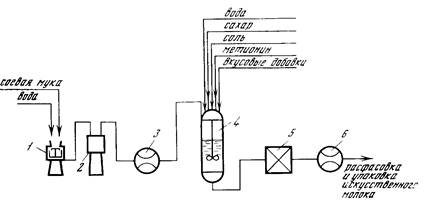
Рис. 29. Схема производства искусственного молока 1— аппарат для измельчения к водной среде; 2 — аппарат для отделения грубьк дисперсных частиц; 3 — аппарат для тепловой обработки; 4 — аппарат для смешения "чмпонептов; 5 гомогенизатор; в -- стерилизатор
большей стандартности и лучших функциональных свойствах. Концентраты и изоляты белка соевых бобов, используемые для получения искусственных молочных продуктов, как правило, обладают высокой диспергируемостыо, не окрашены, лишены постороннего запаха и вкуса. Обычно 1 вес. % изолята белка способен эмульгировать около 12 вес. % растительного масла. Другим важным функциональным свойством изолятов белка соевых бобов является их способность стабилизовать цепы. Поэтому они широко используются для получения взбивных изделий [26, 31— 33 ]. Наряду с работами в области улучшения функциональных свойств белкового сырья, большое внимание уделяется получению сухого молока, творога, паст, сыров, процессам ферментации соевого молока и творога (получение продуктов типа йогурта и т. п.), а также производству сладких молочных желе и различных диетических продуктов. Эти работы особенно интенсивно развивались в СШЛ и Японии [23, 24, 26—28].
В США производство различных искусственных молочных продуктов на базе концентратов и изолятов белка сои получило быстрое развитие начиная с 60-х годов. Эти продукты широко используются на внутреннем рынке, прежде всего для детского питания. Широкое распространение получили также диетические искусственные молочные продукты. It ним можно отнести продукты с пониженной калорийностью, высоким содержанием по-линенасыщепных жирных кислот и повышенным содержанием белка. К этой категории продуктов относятся искусственные сливки, отбеливатели кофе, кремы, другие взбивные изделия, легко приготавливаемые десерты, салатные заправки, сыры и ряд дру
Способы полученияИПП
гих [34—42]. Для получения искусственного молока, а также в качестве отбеливателя кофе используют, например, изолят белка сои (супро 610), выпускаемый в США фирмой «Ральстон пьюри-на ко.». Продукт имеет белый цвет, нейтральный вкус, хорошо растворим в воде и обладает высокой эмульгирующей способностью [38]. Его аминокислотный состав показан в табл. 33. Отметим, что уже теперь более 65% взбитых сливок и 35% отбе-ливателей кофе на рынке США являются искусственными продуктами питания, не содержащими животных жиров [41]. Для
Таблица 33
Аминокислотный состав (г/16 г азота) белка, искусственного молока на основе изолята белка бобов сои (супро 610) и арахиса (милтон) [3843}

Таблица 34
Состав (в % на сухой продукт) некоторых искусственных молочных -.--- --.. 1л,,„„л лЛпптии.гтпн Лпдя инк.».США) [39
| Состав (в "/о на сулии, ii.puuyn.ii ,.^,.и, ..у».-. -- .„-продуктов на основе сои (фирма «Вортингтон фудз инк.», США) [39] |

целей белкового питания в США производят на основе сои ряд «фруктовых» и освежающих напитков. Так, фирма «Вортингтон фудз» производит несколько вариантов сухого бананового напитка моментального приготовления — «соя-мел», обогащенного витаминами. Эта же фирма производит сгущенное соевое молоко, предназначенное для детского питания,— «инфа-соя», и соевый сыр «чиз-о-соя». Состав этих продуктов, а также соевого напитка фирмы «Сснтрал соя ко.» показан в табл. 34 и 35 [39, 40]. Помимо производства для нужд внутреннего рынка, ряд фирм США
160 Глава четвертая
через свои филиалы и путем продажи лицензий организовали производство искусственных молочных продуктов за границей. Некоторые сведения о искусственных молочных продуктах, выпускаемых в ряде стран мира, приведены в табл. 36 [26, 43—49].
Другой путь получения искусственных молочных продуктов связан с использованием смесей белков с взаимодополняющим содержанием аминокислот, например смеси белков масличных и
Таблица 35 Состав соевого напитка, (фирма «Сентрал соя ко.», США) [40]

Примечание. Продукт содержит также окрашивающие и ароматизирующие агенты
злаковых. На этом принципе основано производство в США ку-курузно-соевого молока и пшенично-соевой смеси, которые широко используют для детского питания в виде напитков и каш [50—54]. Данные о составе и биологической ценности этих продуктов приведены в табл. 37. Их производство стремительно растет. Если с момента организации производства кукурузно-соевого молока в США (в 1966 г.) до 1970 г. было переработано в этот продукт более 190 тыс. т обезжиренной муки бобов сои, то уже в 1970 г. только для целей экспорта было переработано 500 тыс. г. В том же году экспортировано 245 тыс. т кукурузно-соевого молока и 75 тыс. т пшенично-соевой смеси [51, 54]. На внутреннем рынке их потребление также быстро увеличивается.
В последние годы в искусственные молочные продукты, наряду с белками сои, начинают перерабатывать белки других масличных культур [43, 44]. В Индии, где производство арахиса составляет около 30% от мирового, налажено производство обезжиренной муки арахиса и более 10% белка арахиса идет в пищу в виде добавок, а также в форме искусственного молока и творога [55]. В 1970 г. в Индии было начато производство искусственного молока «милтон» из обезжиренной муки арахиса. Оно хорошо сохраняется при 25—28° в течение 6 мес., стоит на 25—30% дешевле коровьего (см. табл. 33 и 36), выпускается в виде напитка, а также и в сухом виде и может перерабатываться в творог
Способы получения ИПП 161
[43, 44]. Процесс получения искусственного молока «милтон» включает щелочную экстракцию белка из обезжиренной муки арахиса, осветление раствора HzOz, кислотную коагуляцию белка, растворение коагулята (изолят белка арахиса), обработку острым паром для дезодорации, добавление в раствор буферных солей, витаминов и глюкозы [43].
Белки зеленых листьев и растений — еще один вид белкового сырья для получения искусственных молочных продуктов, использование которого имеет сравнительно недавнюю историю. Иссле-
Таблица 36 Некоторые виды искусственных молочных продуктов [26, 43—49}

6 В. Б. Толстогузов
162 Глава четвертая
дования были начаты в 1957 г. в Англии [56]. В 1961 г. фирма «Плантмилк лтд.» располагала установкой, которая перерабатывала в день несколько тонн зеленых листьев и извлекала до 25% белка. Белки коагулировали подкислением и промывали. Коагулят, темно-зеленого цвета, имел консистенцию и усвояемость
Таблица, 37
Состав кукурузно-соевого молока (Com-Soy-Milk — CSM) и пшенично-соевой смеси (Wheat-Soy-Blend — WSB)
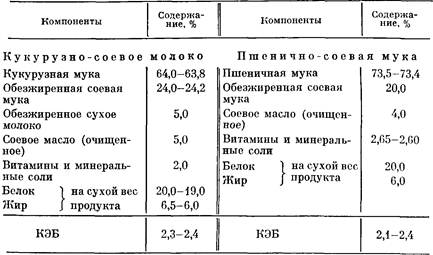
сыра. В дальнейшем удалось экстрагировать до 80% и более белка из зеленых листьев и различных растений (например, клевера, кукурузы, ячменя, капусты, гороха и т. п.), а также разработать процессы осветления экстрактов, с тем чтобы получить продукт белого цвета. Искусственное молоко «плантмилк» — полноценный пищевой продукт с приятным вкусом, напоминает натуральное молоко и имеет в 3 раза более высокую концентрацию сухих веществ. «
ИСКУССТВЕННЫЕ КРУПЯНО-МАКАРОННЫЕ ИЗДЕЛИЯ
Выделение этих форм пищи в один раздел представляется целесообразным ввиду сходства способов их получения, а также состава и ряда характерных особенностей.
Крупы и макаронные изделия относятся к числу наиболее широко потребляемых продуктов, пригодны для продолжитель-
Способы получения ЙПП 163
uoro хранения и просты в употреблении. В настоящее время более 'i/з населения земного шара использует зерновые в пищу преимущественно в виде круп и макарон и менее 'А в форме хлеба [57, 58]. Зерновые продукты, прежде всего крупы и макароны, играют, как показано в гл. I, ведущую роль не только как поставщик калорий (см. табл. 6), но и как основной источник белка (см. табл. 7). Даже в районах развитого животноводства (США, Канада, Скандинавские страны) потребность в белках в значительной мере удовлетворяется за счет зерновых.
ИСКУССТВЕННЫЕ КРУПЫ
Помимо увеличения масштабов производства белковой пищи и расширения ее ассортимента, развитие производства искусственных круп имеет также целью повысить пищевую ценность. потребительские свойства и снизить стоимость крупяных изделий.
Действительно, для аминокислотного состава белка большинства зерновых культур, используемых для производства круп, характерен дефицит незаменимых аминокислот (лизина, триптофа-на, треонина и метионина). К тому же, содержание белка в зерновых невысоко, и он существенно дороже, например, белков семян масличных культур (табл. 38; см. также табл. 11 и 14). Потребление белка зерновых культур в виде круп и макарон сопровождается потреблением значительных количеств углеводов, что рассматривается как важный фактор развития белковой
Таблица 38
Состав (в %) важнейших зерновых культур {при 15%-ном содержании воды)[57}
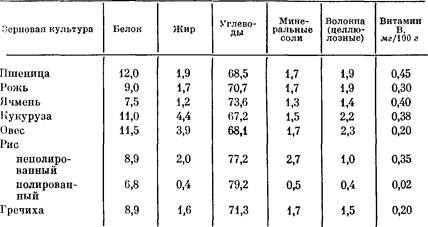
б*
164 Глава четвертая
недостаточности [II]. Обычно невысоко также содержание в крупах витаминов и минеральных солей, особенно солей кальция и железа. Кроме того, при традиционной технологии производства круп (из пшеницы, кукурузы, проса, риса, ячменя и других злаковых) в результате удаления периферийных слоев зерна при шлифовке и полировке (улучшаются потребительские характеристики круп, внешний вид, развариваемость и стойкость при длительном хранении), как правило, снижается биологическая ценность, поскольку удаляемые наружные слои зерна обогащены белком, витаминами, жиром и минеральными солями. В ряде случаев неудовлетворительны и технологические свойства круп. Сюда относится большая продолжительность кулинарной обработки, особенно кукурузной, перловой и гороховой круп, и недостаточная стабильность в горячем состоянии [59, 60].
Отдельные из указанных недостатков могут быть устранены путем совершенствования традиционной технологии производства круп (ограничение толщины слоя, удаляемого при шлифовке, предварительная гидротермическая обработка зерна для перераспределения пищевых веществ из поверхностного слоя в объем зерна путем диффузии и т. п.), обогащением круп витаминами, незаменимыми аминокислотами и минеральными солями [59-61].
Производство искусственных круп было впервые организовано после второй мировой войны в Англии и Голландии, а затем освоено промышленностью ряда стран Европы и Азии [23, 59]. Значительные успехи в разработке полноценных в биологическом отношении искусственных круп, имитирующих рис, были достигнуты в Индии, Японии и США.
Для производства искусственных круп в общем случае готовят смесь различных видов муки, обогащающих добавок и крахмала с водой. Полученную тестовую массу формуют в виде стержней (отсюда сходство способов получения круп и макарон), которые нарезают, подвергают обкатке, тепловой обработке и сушке. Начальная стадия получения искусственных круп заключается, следовательно, в переработке зерна в муку и приготовлении смесей различных видов муки. Отсюда вытекает возможность получения искусственных круп с высокой биологической ценностью, так как, во-первых, переработка зерна в муку исключает шлифовку зерна, сопровождаемую потерями ценных пищевых веществ. Кроме того, обычно используют смеси муки зерновых и масличных с взаимодополняющим содержанием аминокислот и других незаменимых факторов питания. Наконец, к исходной смеси добавляют витамины, минеральные соли и аминокислоты. Одновременно появляется возможность использования для питания в виде искусственных круп дополнительных количеств белка масличных, а также использования отходов производства круп
Способы получения ИПП 165
традиционными методами (измельченный поверхностный слой зерна) и других видов белкового сырья, например, обрата молока, казеина и т. д. Так, искусственный рис, содержащий 18—20% белка, получают на основе смесей арахисовой, соевой или кокосовой муки с кукурузной, пшеничной или рисовой, с добавками лизина, витаминов и минеральных солей. Таким образом, открывается возможность увеличения объема производства, биологической ценности круп и снижения стоимости белковой пищи при их производство.
В качестве студпеобразовате-ия при производстве искусственных круп в большинстве случаев используют крахмал [59, 60, 62—68]. Смесь пищевых компонентов И крахмала диспергируют в воде, нагревают до клейстеризации крахмала, формуют тестовую массу в виде гранул и подсушивают до влажности ниже 15%, с тем чтобы обеспечить продолжительное хранение продукта. Для формования чаще всего используют поршневые или шнековые экструдеры, например, типа макаронного пресса с последующим нарезанием сформированного стержня (крупа-сечка). Зерна обкатывают во вращающемся барабане в токе нагретого воздуха; при этом происходит полная клейстеризация крахмала и подсушива-ние гранул, во избежание их слипания. При низкой влажности тестовой массы для формования применяют также обычную технику гранулирования порошков, подобную применяемой для получения драже и таблеток. Технология получения искусственных круп весьма проста и позволяет использовать обычное оборудование. Она сводится, следовательно, к получению гранулированных студней крахмала, наполненных белками и другими пищевыми веществами. Некоторые сведения о составе производимых искусственных круп приведены в табл. 39 [47].
Предложен ряд способов получения искусственных круп с повышенной биологической ценностью. Так, например, рекомендуется использовать смеси 72—86 вес.% рисовой муки и 14—28% обезжиренной соевой муки. Продукт рекомендуется употреблять с молоком без длительной варки [63]. При получении искусственного риса предложено готовить смесь пшеничной и картофельной муки в соотношении 4: 1, добавлять 35% воды и после кратковременного нагрева и перемешивания при 105° охлаждать смесь до 60—70°, вводить до 10% аминокислот и использовать для формования круп по обычной технологии [64]. Предложено также получать искусственные крупы на основе смеси муки злаковых, масличных, сухого обезжиренного молока с предварительно клейстеризованным крахмалом. Полученную тестовую массу можно формовать на дражировочных машинах [60]. Эти крупы (Пионерская I, II и III) быстро развариваются, имеют высокую биологическую ценность и содержат (на сухой вес) 12—13% белка, 64—73% углеводов и 1,0—5,5% жиров [60, 62].
| Глава четвертая |
Однако, несмотря на очевидную возможность резко увеличить использование белков для питания в виде искусственных круп с высокой биологической ценностью, расширение производства и потребления искусственных круп встретило ряд трудностей ввиду их обычно невысоких потребительских и технологических свойств, определяющих, в частности, поведение круп при варке и при хранении в горячем готовом виде.
Таблица 39
Некоторые искусственные крупы и макаронные изделия повышенной пищевой ценности [47]

Недостатки искусственных круп определяются их природой. Они обычно представляют собой гранулированные студни крахмала с высоким коэффициентом наполнения белками. Варка таких круп сопровождается клейстеризацией и гидролизом крахмала, быстрым и чрезмерно высоким набуханием зерен, их слипанием и разрушением с образованием продукта пастообразной консистенции. Кроме того, варка сопровождается диффузией пищевых веществ из зерен искусственных круп в варочную воду. В результате органолептические свойства и пищевая ценность кулинарных изделий из них может резко снижаться [65—67 ]. Особенно ощутима недостаточная стабильность искусственных круп при продолжительной гидротермической обработке и хранении в горячем виде на предприятиях общественного питания. Здесь обычно применяют котлы большой емкости, готовят значительные количества продукта, который продолжительное время находится в горячем состоянии. В этих условиях возможно полное разварива-ние круп.
Способы получения ИПП 167
Большинство исследователей рекомендуют использовать искусственные крупы в качестве круп быстрого приготовления, т. е. не требующих длительной гидротермической обработки, а также для получения небольших порций кулинарных изделий. Для предотвращения потерь пищевых веществ и ограничения степени набухания искусственные крупы предложено отваривать в меньшем и строго определенном количестве воды, с тем, чтобы крупы поглощали при набухании всю варочную воду, или отваривать в молоке, а кроме того, использовать искусственные крупы для имитации изделий типа манной каши или же в качестве суповых засыпок [60, 65].
Значительное внимание было уделено вопросам регулирования структуры и физических свойств зерен искусственных круп. Так, было предложено вводить в тестовую массу в количестве от 2 до 20% белки, способные повышать прочность и снижать степень набухания поверхностного слоя зерен, например глютен пшеницы. Тем не менее этот продукт также рекомендуется быстро отваривать в ограниченном количестве воды или в молоке [65]. Те же авторы предложили способ снижения времени варки круп за счет более быстрого и равномерного набухания зерен. Такой эффект достигается введением в тестовую массу на основе пшеничной муки перед ее формованием 0,5—2,5% камеди, например, гуммиарабика, карайа или трагаканта. Этот эффект может быть объяснен образованием сильногидратированных, растворимых комплексов кислых полисахаридов с клейковиной пшеницы (см. гл. II). Такие искусственные крупы рекомендуется варить в течение 0,5—1 мин. в малом количестве воды (в 2 раза меньшем, чем обычно) или же в молоке. Они удобны для быстрого приготовления небольших порций кулинарных изделий, однако не стабильны в горячем состоянии и пригодны лишь для немедленного употребления.
Более интересные результаты удалось получить при введении в искусственные крупы пизкомолекулярных поверхностно-активных веществ, например моиоглицоридов жирных кислот [66, 67]. При этом повышается стабильность структуры круп и удается обеспечить рассыпчатую консистенцию изделий даже при длительном их нагреве. В другом случае перед формованием искусственного риса на основе смеси пшеничной, рисовой муки и картофельного крахмала для сохранения целостности зерен при варке в качестве поверхностно-активных веществ добавляют продукты кислотного гидролиза пектина [67].
Улучшить потребительские свойства искусственных круп и снизить потери пищевых веществ при варке удалось также нанесением тонких водоустойчивых оболочек из шеллака или этил-цоллтолозы [68] па имитирующие рис гранулы Крахмального студня, содержащие клейковину пшеницы и смесь аминокислот.
168 Г лав я четвертая
Другой способ получения искусственных круп с хорошими потребительскими свойствами основан на использовании в качестве студнеобразователя альгината или пектината кальция [69—72]. Студни альгината или пектината кальция, содержащие клейстеризованный крахмал, ограниченно набухают в условиях варки, сохраняют форму и целостность при продолжительном гидротермическом воздействии и потому пригодны для получения искусственных круп. Для формования гранул студня использовали прием, который был применен ранее для получения искусственной икры [73] и искусственных ягод [74, 75] на основе студней альгината или пектината кальция. Пищевые вещества (крахмал и белки) диспергируют в растворе альгината или пектина и вводят дисперсию в виде капель в раствор соли кальция. Было покапано, что полученные таким образом искусственные крупы можно подвергнуть различным видам кулинарной обработки — варить в воде, в молоке, на пару, запекать и тушить [70]. Показана также их высокая пищевая ценность [70, 71] и потребительские свойства [72]. Тем не менее этот способ имеет ряд недостатков. Процесс получения гранул студня диффузией ионов кальция в капли исходного раствора альгината протекает медленно и потому недостаточно технологичен. Помимо этого, гранулы получают в водной среде (введение капель в раствор соли кальция, промывка водой). Поэтому потеря водорастворимых пищевых веществ, особенно низкомолекулярных, происходит не только при варке круп, но и при их получении.
ИСКУССТВЕННЫЕ МАКАРОННЫЕ ИЗДЕЛИЯ
Целесообразность разработки способов получения искусственных макаронных изделий определяется рядом причин, которые аналогичны рассмотренным в предыдущем разделе, посвященном искусственным крупам (повышение биологической ценности, улучшение технологических свойств макаронных изделий и расширение ресурсов белка, используемого для питания). Дополнительный аспект проблемы связан с тем, что в ряде стран ощущается дефицит твердых пшениц, из которых вырабатывают высококачественные макаронные изделия. Отсюда вытекает задача получения макарон как из пшеничной муки немакаронных сортов, так и на основе нетрадиционного сырья.
Для повышения биологической ценности макарон в состав тестовой массы перед формованием вводят различные белки и смеси аминокислот, например, казеин, сухое молоко, клейковину, гидролизаты дрожжей [51, 61, 76—80]. Однако наиболее интересные результаты получены при обогащении макарон белками сои [6] и других масличных культур, которые, как и при обогащении зерновых в случае круп, являются мощным источником
Способы полученияИПП 169
лизина (табл. 40). Их добавление к муке зерновых приводит к столь резкому повышению биологической ценности [81—87], что такие продукты могут служить основным или единственным источником белка для детей, а также использоваться для лечения квашиоркора [81—83].
В США в последние несколько лет получило быстрое развитие производство макаронных изделий на основе смесей
Таблица 40
Эффект добавления обезжиренной соевой муки к пшеничной муке (дурум) при производстве макарон [81]
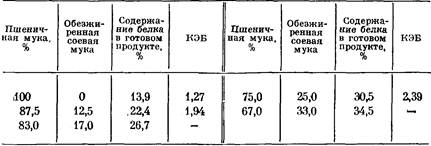
муки зерновых и масличных культур. Технология получения таких продуктов близка к технологии получения искусственных круп. Для производства обогащенных макаронных изделий часто используют смесь муки двух зерновых культур: пшеницы (до 30%) и кукурузы (45—85%), а также 15—40% обезжиренной соевой муки, к которым добавляют витамины, соли железа и кальция (табл. 39, 41 и 42). Макаронные изделия, обогащенные обезжиренной соевой мукой в количестве не менее 12,5%, обычно содержат 20—25% белка и имеют КЭБ около 2,4. Их потребление в 1973 г. в США составило более 50 тыс. т. Производство таких продуктов продолжает быстро расти, особенно после разрешения и рекомендации правительства США использовать обогащенные макароны в рамках программы обедов для школьников, в качестве заменителей мяса [54]. Эти продукты вызвали также интерес со стороны армейских служб США [88].
Совершенствование технологии производства обычных и обогащенных макаронных изделий на основе пшеничной муки позволило разработать способы получения быстроразваривающихся изделий [89], продуктов, пригодных для длительного хранения [90], а также макаронных изделий, хорошо выдерживающих продолжительное гидротермическое воздействие [91, 92]. В последнем случае, аналогично искусственным крупам [66], используют поверхностно-активные вещества [92].
170 Глава четвертая
В отличие от натуральных круп обычные и обогащенные макаронные изделия, форма, структура, состав и комплекс свойств которых создаются искусственным путем в ходе переработки муки, могут рассматриваться как искусственные продукты питания, способ производства которых стал уже традиционным (см. гл. I). Тем не менее, чтобы не вводить новой терминологии, мы будем относить к искусственным лишь макаронные изделия, полученные не на основе пшеничной муки, т. е. из нетрадиционного сырья, учитывая при этом, что такого рода ограничение весьма «искусственно».
Таблица 41
Состав (в %) и биологическая ценность кукурузно-соево-пшеничных макарон (ЖФ-1 и ЖФ-2), производимых фирмой «Дженерал фуда корп.», США [83]
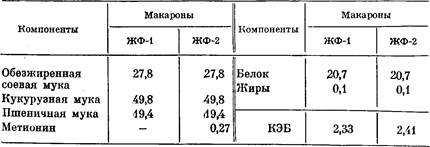
Число работ в области «собственно» искусственных макаронных изделий весьма ограничено. Здесь, так же как и при получении искусственных круп, в качестве основного студнеобразо-вателя чаще всего используют крахмал, который смешивают с белками, другими пищевыми веществами и водой; смесь нагревают до клейстеризации крахмала, формуют методом экструзии и сушат. Таким методом предложено получать искусственные макаронные изделия типа лапши, вермишели, трубчатых макарон и спагетти на основе муки зерновых и бобовых культур, орехов и картофеля [93—97]. Чаще всего используют рисовую и кукурузную муку. Для получения тестовых масс высокой вязкости и с целью снижения липкости изделий рекомендуют добавлять полифосфаты [93], карбонат кальция и сульфат магния [94].
Использование в качестве студнеобразователя крахмала обычно не обеспечивает достаточно высоких потребительских свойств. Тем не менее уже эти начальные работы показали возможность и перспективность производства искусственных макаронных изделий, особенно если бы удалось разработать студнеобразующие системы, обеспечивающие стабильность продукта при кулинарной
Способы получения ИПП
обработке и позволяющие в заметных пределах варьировать состав изделий, в частности степень наполнения белками.
Недавно была показана возможность получения искусственных макаронных изделий (а также круп) с высокими потребительскими свойствами и биологической ценностью [98—100]. Эти продукты получены на основе смешанных студней альгината
Таблица 42
Состав и биологическая ценность макарон иголден элбоу» фирмы «Дженерал фудз корп.»,США [82]
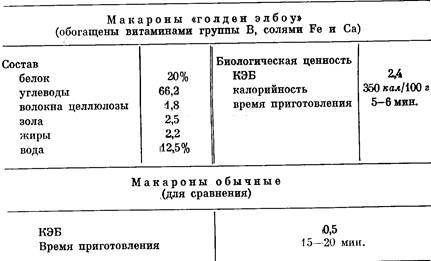
кальция и крахмала, наполненных белками [101, 102]. В качестве наполнителей были использованы казеин, изолят белка соевых бобов и изолят белка семян хлопчатника. При этом показано, что таким путем могут быть получены студни, хорошо воспроизводящие по физико-химическим свойствам студии, приготовленные из муки твердых и мягких пшениц, а также студни пшеничной клейковины. Разработанные рецептуры и технологические режимы позволили получать искусственные макароны, близкие по реологическим и технологическим свойствам к высококачественным макаронам из муки твердых пшениц [98].
В табл. 43 и 44 приведены данные о составе, реологических и технологических свойствах искусственных макарон в сравнении с макаронами из муки твердых пшениц. Что касается биологической ценности, то искусственные макароны на основе казеина и белка соевых бобов значительно превосходят натуральные макароны. Как видно из табл. 44, они содержат в 2,6 раза больше
172 Глава четвертая
Таблица 43
Состав (%) и биологическая ценность искусственных {иакарон в сравнении с натуральными
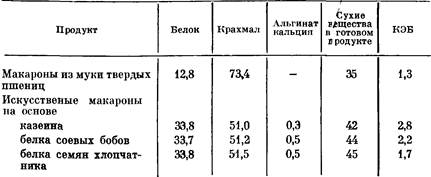
Примечание. Влажность всех исследованных продуктов составляла 12,5%.
Таблица 44
Характеристика искусственных макарон относительно эталона — натуральных макарон высшего сорта
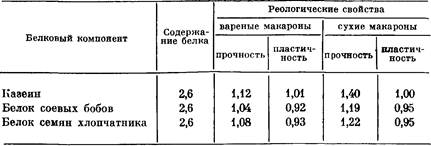
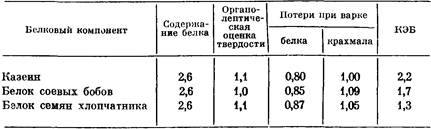
Способы получения ИЛИ 173
белка, обладающего к тому же более сбалансированным аминокислотным составом [99].
На основа алыинат-крахмальных и пектинат-крахмальных студней, наполненных белками, разработаны также методы получения искусственных круп, мучных кондитерских изделий и кар-тофелепродуктов. Способы приготовления этих продуктов в основном идентичны способу получения макарон. Отличия сводятся к составу перерабатываемых систем, условиям их формования и тепловой обработки.
ИСКУССТВЕННЫЕ МЯСОПРОДУКТЫ
Интерес к искусственным мясопродуктам вызван тем, что они имитируют наиболее дорогие, дефицитные, обладающие высокой биологической ценностью и вкусовыми достоинствами продукты питания массового потребления.
Работы в этой области [5, 6, 103—126] направлены на получение искусственных продуктов, имитирующих 1) традиционные изделия из рубленого мяса (технология сравнительно проста, продукты дешевы и удобны для использования) и 2) нерубле-пые мясопродукты волокнистой структуры, т. е. одну из наиболее дорогих форм пищи.
Исследования были начаты в США в конце 40-х—начале 50-х годов Р. Боером («Форд моторе ко.»), М. Ансоном и М. Педером («Юнилевер», «Ливер бразерс ко.»), С. Серклом и Д. Джонсоном («Сентрал соя ко.») и другими учеными. Эти работы велись параллельно по двум указанным направлениям в лабораторном и опытно-промышленном масштабе, вплоть до начала 60-х годов. Впервые в 1958 г. М. Ансон отметил важную роль студнеобразного состояния для имитации мясопродуктов и по существу впервые сформулировал задачу получения студней с определенной структурой и механическими свойствами. Уже в тот период он мог с уверенностью говорить о возможности производства разнообразных сложных продуктов, напоминающих по текстуре рубленое и перублепос мясо, а также о том, что основные методы получения таких продуктов уже созданы, однако детальная разработка этих методов только начата [5]. Результаты большинства утих исследований не были, однако, внедрены в промышленность, прежде всего из-за сравнительно высокой стоимости и неудовлетворительных вкусовых и потребительских качеств искусственных мясопродуктов, получаемых в тот период [124]. Тем не меноо были созданы основные предпосылки для дальнейшего развития работ в этой области и инициирован интерес к ней многочисленных исследовательских групп и ряда фирм в различных странах.
174 Глава четвертая
В период 60-х годов наблюдалось значительное/расширение научных и научно-технических разработок (с 1954/но 1960 г.— 15 патентов, с 1961 по 1972 г.— 67 патентов [120]У преимущественно по второму направлению. В этот период внимание прежде всего было обращено на разработку экономичных ^методов производства основных видов белкового сырья с необходимыми функциональными свойствами (обезжиренной муки, /концентратов и особенно изолятов белка соевых бобов), на поиск экономически эффективных приемов его переработки, методов улучшения биологической ценности, органолептических и потребительских свойств, а также на организацию сбыта искусственных мясопродуктов.
Лишь в конце 60-х годов, и особенно после 1970—1971 гг., произошел переход к полупромышленному и промышленному этапу разработок. Исследования получили быстрое развитие во многих странах (США, Япония, Голландия, Англия, ФРГ), и оказалось возможным приступить к широкому использованию искусственных мясопродуктов для питания.
В зависимости от способа применения искусственные мясопродукты подразделяют на две категории: аналоги и разбавители [121]. Термин «разбавители» означает, что эти продукты используют в комбинации с традиционными. К разбавителям относят, в частности, белки сои, которые после специальной обработки для придания необходимых функциональных свойств смешивают с мясным фаршем и перерабатывают в различные изделия. Этот вид разбавителей мы не будем рассматривать как неперспективный. Более широкое применение (и в больших количествах по отношению к натуральному мясу) получили разбавители на основе текстурированных белков, так как они обладают существенно более высокими функциональными свойствами (высокая степень набухания, водопоглотительная, жиросвязывающая способность и необходимая консистенция), а также макроструктурой, характерной для мясопродуктов.
Термин «аналоги» означает, что эти искусственные мясопродукты имитируют по внешнему виду, консистенции, цвету, вкусу и запаху традиционные мясные, рыбные изделия и изделия из птицы. Они могут быть использованы для приготовления соответствующих блюд, а также в качестве разбавителей, применяемых в больших или неограниченных количествах.
Ниже рассмотрены способы получения искусственных мясопродуктов, имитирующих изделия из рубленого и нерубленого мяса.
Способы получения ИПП
ИСКУССТВЕННЫЕ МЯСОПРОДУКТЫ, ИМИТИРУЮЩИЕ ИЗДЕЛИЯ ИЗ РУБЛЕНОРО МЯСА (ИМР)
К типу продуктов ИМР относятся колбасо-сосисочные изделия, рубленые шниЦели, котлеты, мясной хлеб, холодные мясные завтраки, мясные йасты, паштеты и т. п. Их производят главным образом на основе белков сои и пшеницы, яичного альбумина, казеина или их смесей. Обычно они представляют собой студни, наполненные дисперсиями белков, иолисахаридов (крахмал) и липидов (растительные масла и животные жиры). Пастообразные продукты, как правило, представляют собой тиксотропные и термообратимые студии с температурой плавления около 20—40° и ниже и невысоким предельным напряжением сдвига.
Для получения искусственных мясопродуктов — аналогов изделий из рубленого мяса в раствор или дисперсию белкового или полисахаридного студнеобразователя вводят тонкоизмельченные пищевые вещества, а также вкусовые, ароматические вещества и красители. Полученную дисперсию с жидкой непрерывной фазой помещают в соответствующую оболочку или форму и переводят в студнеобразное состояние. В результате получают изотропные студни, наполненные пищевыми веществами и имитирующие изделия из рубленого мяса.
Можно выделить три основных вида студнеобразующих систем, используемых для получения ИМР:
1) растворы или разбавленные дисперсии белков, образующие
студни при нагреве [127—140];
2) концентрированные дисперсии белков, образующие студни
при нагреве [6, 139—143];
3) растворы кислых полисахаридов (альгинатов или пектинов) , содержащие белки и другие пищевые вещества и образующие студни при действии ионов кальция [144—146 ].
Соответственно далее мы будем говорить о трех методах получения ИМР.
Согласно первому методу, для получения студней при нагреве
используют яичный альбумин [132, 133], свежевыделенную клейковину пшеницы [128, 133—136] и изоляты соевого белка. С целью модификации свойств белковых студней, прежде всего механических и осмотических, в жидкие системы вводят небольшие количества солей кальция, алюминия [139, 140] или же кислого полисахарида, например каррагенина [127].
В качестве пищевых наполнителей используют тонкие дисперсии крахмала [127], белков сои и арахиса [128, 131 ], растительных масел [127—132, 137 ], животных жиров [133, 138] и отходов мясопереработки [138]. В качестве вкусовых и ароматических компонентов обычно применяют поваренную соль, глютаминат
| Глава четвертая |
натрия, гидролизаты белков (чаще всего кислотные гидролизаты растительных белков), мясные бульоны, животные жиры, специи (порошки лука, перца, чеснока), коптильные жидкости, а иногда также мясную муку и тонкоизмельченное мясо низших сортов [6, 127—145]. Для имитации цвета мясных изделий используют
растительные пищевые красители, карамельные красители и пищевой альбумин.
Важным фактором при получении этих искусственных мясопродуктов является стабильность исходных суспензий и эмульсий пищевых веществ. Для получения таких дисперсий используют поверхностно-активные вещества [133—137] иди препараты белков, например казеинат натрия [128] или яичный альбумин [132]. Часто в липидной фазе предварительно диспергируют белки и таким путем готовят сложные дисперсные системы с высоким содержанием белка и жира [132].
Методы получения ИМР, относящиеся к первой группе, весьма просты и позволяют получить широкий ассортимент изделий. Недостатки этих методов связаны с необходимостью применения сравнительно дефицитных и дорогих белков, а также с высокими требованиями к стандартности используемого белкового сырья,
режимам получения исходных дисперсий и перевода их в студнеобразное состояние.
Вторая группа методов основана на получении студней при нагреве концентрированных дисперсий белков. На практике к смеси порошкообразного белка (обезжиренная соевая мука, казеин) с буферными солями и солями кальция, алюминия или магния (в случае белка соевых бобов) добавляют воду, затем при перемешивании вводят жиры, специи и красители. Жидкую высоковязкую систему нагревают в форме или же шприцуют в оболочку и варят на пару для получения колбасо-сосисочных изделий. Нагрев порошкообразных частиц белка в водной среде сопровождается их набуханием и при достаточной концентрации и степени набухания белковых частиц приводит к их физическому взаимодействию и образованию макроскопического студня во всем объеме системы (области контакта частиц — узлы сетки студня). Так можно получать искусственные мясопродукты с высоким содержанием белка, поскольку образование достаточно прочных
студней возможно лишь при нагреве дисперсий, содержащих не менее 20—50% белка.
Основное условие получения высококачественного продукта заключается в правильном подборе рецептуры жидких систем и условий их перевода в студнеобразное состояние, что необходимо для обеспечения требуемой степени набухания дисперсных частиц белка без их растворения, нужных когезионных и адгезионных свойств этих студнеобразных частиц и в конечном счете для образования прочного белкового студня. Эти условия, как ира-
Способы получения ИПП
вило, находят эмпирическим путем [143], так как наждому виду используемого белкового сырья (а при недостаточной степени чистоты и каждой его партии) отвечает свой и довольно узкий интервал концентраций дисперсии, значений рН системы и содержания в ней солей, а также определенный режим ее тепловой обработки (температура, продолжительность, интенсивность перемешивания) и созревания перед нагревом. Поэтому общий недостаток этих способов связан с высокими требованиями к чистоте и однородности белкового сырья и трудностью урегулирования состава продукта, например содержания белка и жира,
Условия получения таким путем искусственных колбасо-сосисочных изделий на основе казеина исследовали Кенде и Кет-тинг [141, 142], на основе белков соевых бобов—Френк и Серкл
[6, 143].
ИМР на основе казеина содержат 30—40% белка и имеют
рН 4,9—5,3. Продукт можно нарезать ломтиками, он хорошо сохраняет форму и консистенцию при кулинарной обработке. Для его получения используют 30—40% суспензии казенна с рН 5,0— 5,2. При рН ниже 4,9 продукт приобретает зернистую консистенцию и кислый вкус, а при рН выше 5,3 легко теряет форму при нагреве. Для повышения устойчивости продукта к яагреву в водную суспензию казеина добавляют соли кальция и алюминия, а также белки или белковые продукты, образующие студни при нагреве, например, яичный альбумин, муку сои, пшеницы или арахиса в количестве '/в—*/з от веса казеина. Роль добавок солей кальция и алюминия заключается в предотвращении растворения казеина и регулировании степени набухания и когезионных свойств дисперсных частиц. Интересна возможность частичной или полной замены поваренной соли хлористым калием, введение которого в искусственный мясопродукт, полученный на основе казеина, не вызывает появления горького привкуса. Такой продукт может быть рекомендован для лечебного питания.
Для получения ИМР на основе концентрата или изолята белка сои [6] к дисперсиям белка добавляют Na2HPOi и Ca(OH)z. Обычно используют дисперсии с рН 5,5—6,0. Ирм рН ниже 5,5 получают продукт жесткой зернистой консистенции. Влияние различных параметров процесса и состава исходной жидкой системы на качество искусственных сосисок и вареных колбас на основе белка соевых бобов исследовано в работе [143].
Несмотря па указанные выше общие недостатки рассматриваемого способа получения ИМР, искусственные сосиски на основе белка соевых бобов производят в промышленном масштабе. Такие продукты имеют высокие пищевые и вкусовые достоинства.
Еще один способ получения ИМР основан на использовании студней альгината и пектината кальция, которые устойчивы к гидротермическим воздействиям в условиях варки и жарения
178 Глава четвертая
[144—146 ]. Белки и белоксодержащие продукты выступают здесь в роли наполнителей полисахаридных студней или одновременно в роли дополнительных студнеобразователей (смешанные студни). В этом случае допустимы более низкие требования к чистоте и стандартности белкового сырья, что открывает возможность использования различных видов пищевого сырья. Например, в растворе альгината или пектина диспергируют мясной фарш, полученную массу формуют и нарезают ломтиками в растворе CaCl2. Ломтики колбасоподобного продукта промывают водой от избытка хлористого кальция и обжаривают [144]. Основной недостаток этого способа связан с использованием медленного процесса диффузии ионов кальция в объем формуемых изделий, а также с необходимостью промывки их водой. Низкая скорость диффузии делает этот процесс малоэффективным в технологическом плане. Продолжительная обработка продукта в водных средах (раствор CaCL, вода) неизбежно сопровождается потерями водорастворимых пищевых и ароматических веществ. Недостатки здесь, следовательно, те же, что и при получении искусственных круп с использованием альгинатов и пектинатов кальция (см. выше). По-видимому, по этим причинам способ не нашел промышленного применения.
Аналогичным образом альгипатные студни предложено также использовать при производстве традиционных колбасо-сосисочных изделий, где кислые полисахариды, прежде всего водорастворимые альгинаты, рекомендуется добавлять в мясные фарши (источник ионов кальция) для регулирования консистенции и улучшения качества изделий [147, 148 ].
ИСКУССТВЕННЫЕ МЯСОПРОДУКТЫ ВОЛОКНИСТОЙ СТРУКТУРЫ (ИМВ)
Для производства ИМВ обычно используют белковые волокна, получаемые методом мокрого прядения растворов белков. Волокна затем склеивают пищевым связующим, содержащим различные пищевые вещества и красители. Варьируя состав и физические параметры волокон и связующего, их соотношение и характер укладки волокон, удается в достаточной мере полно воспроизводить волокнистую структуру, органолептические и потребительские характеристики большого числа традиционных мясопродуктов. Так получают широкий ассортимент аналогов мяса животных, рыбы и птицы.
По существу все ИМВ представляют собой анизотропные пищевые студни волокнистой структуры с различным соотношением волокон и связующего и с разной степенью ориентации волокон. Под структурой ИМВ понимают видимую невооруженным глазом макроструктуру, характеризуемую наличием волокон (основным
Способы полученияИПП
структурным элементом), их параметрами и взаимным расположением.
Известны два основных вида ИМВ, отличающихся составом и
способами получения. Первый представляет собой пищевые студни (связующее), наполненные съедобными волокнами белков или полисахаридов. Во втором случае ИМВ — это система пищевых волокон, скрепленных связующим. В первом случае основное количество пищевых, вкусовых и ароматических веществ содержится в студне, который наполнен (армирован) волокнами. Требования к механическим и физико-химическим свойствам студня и его устойчивости к нагреву весьма высоки. Волокна могут обладать пониженной биологической ценностью (велокна на основе изоля-та соевого белка) или вообще не перевариваться в желудочно-ки-шечном тракте (волокна на основе кислых полисахаридов или целлюлозы). Они придают продукту неоднородную (по органо-лептической оценке) мясоподобную консистенцию и волокнистую
структуру.
Во втором случае используют преимущественно белковые волокна, которые соединены малым количеством связующего или заливочными композициями. Связующими обычно служат жидкие растворы или дисперсии, образующие студни при нагреве (см. ниже). Заливочными композициями могут быть расплавленные животные жиры, растворы желатины и другие жидкие системы, переходящие в твердое состояние при охлаждении. В этих продуктах выше степень ориентации и плотность упаковки волокон, но существенно ниже требования к прочностным свойствам связующего. Для них характерна более высокая анизотропия механических свойств и большее различие прочностных характеристик связующего и волокон, например прочности на срез. Поэтому разрушение и измельчение ИМВ при пережевывании сопровождается разделением волокон и имитирует неоднородную мясоподобную консистенцию. Эта последняя особенность ИМВ была впервые отмечена Ансоном [5].
Исследования в области ИМВ второго типа развивались особенно интенсивно па начальном этапе работ. Был разработал ряд приемов регулирования механических и физико-химических характеристик волокон, их обработки различными видами связующих, а также способы ориентации и объединения волокон в продукт, в том числе и способы, исключающие применение связующих (сплавлеппе волокон в областях контакта). На этом этапе было показано, что количество и степень ориентации волокон в продукте могут быть снижены без ухудшения его консистенции и других органолоптичсских и потребительских характеристик.
Первый тип ИМВ получил развитие в недавнее время. Это позволило снизить стоимость и повысить пищевую ценность продук-
180 Глава четвертая
тов за счет снижения содержания в них волокон на основе изоля-тов белка соевых бобов, биологическая ценность которых обычно не высока.
Важной предпосылкой быстрого развития работ в области ИМ В явилась возможность использования опыта, накопленного в 30—40-х годах при организации производства искусственных белковых волокон для текстильной промышленности.
В отличие от большинства полимеров (термопластичных), перерабатываемых через расплавы, белки не могут быть переведены при нагреве в вязкотекучее состояние. Поэтому белки перерабатывают в волокна через растворы, в основном методом мокрого прядения, т. е. переводят в вязкотекучее состояние путем растворения, формуют концентрированные растворы белка в виде тонких струй, фиксируют форму струй переводом их в студнеобразное состояние, подвергают студнеобразные нити ряду обработок и высушивают для получения текстильных волокон. Изучение методов переработки биополимеров и, в частности, белков в волокна было начато еще в прошлом веке [149]. Здесь целесообразно кратко остановиться лишь на работах по получению текстильных белковых волокон.
Искусственные белковые волокна со свойствами, близкими к свойствам шерсти, были получены впервые на основе казеина, а затем из белков сои, арахиса и кукурузы [150—152]. Технология мокрого прядения текстильных казеиновых волокон, включая их дубление формальдегидом и солями алюминия и хрома, была разработана Феррети [153, 154]. Эти волокна начали производить в промышленном масштабе в Италии в 1937 г. под названием «ла-ниталь», а в США — в 1939 г. под названием «аралак». Так же как и шерсть, казеиновые волокна подвержены действию моли и плесени, но основным их недостатком была низкая прочность во влажном состоянии. В 1938 г. была разработана технология получения текстильных волокон на основе белков арахиса, и в 1946 г. в Англии начато их производство под названием «ардил». Эти волокна были в 2 раза дешевле шерсти, но поражались молью и обладали меньшей горючестью.
В 1948 г. в США было начато производство искусственного волокна «викара» па основе белка кукурузы, которое было устойчиво к действию моли и плесени и более устойчиво к действию микроорганизмов и щелочей, чем натуральные белковые волокна. В результате разработок [155, 156 ], выполненных Р. Боером (сотрудником фирмы «Форд мотор ко.»), в США с 1939 по 1956 г. производили искусственные волокна на основе белков сои. Их использовали для изготовления обивочных тканей для автомобилей. Были также разработаны способы производства текстильных белковых волокон на основе других видов растительных белков, белков сыворотки крови, дрожжей и т. д.
Способы получения ИПП
Во всех случаях мокрого прядения белковых волокон первая стадия процесса состоит в приготовлении прядильного раствора белка. Обычно перерабатывают глобулярные белки, макромолекулы которых сравнительно слабо взаимодействуют в растворах. С тем чтобы вызвать умеренную денатурацию белков и повысить межмолекулярное взаимодействие, их обычно растворяют в растворах щелочи, мочевины или поверхностно-активных веществ [113, 149]. Как известно, способность образовывать стабильные жидкие нити связана с наличием в растворе' асимметричных, сильно взаимодействующих частиц и сильно зависит от его реологических и поверхностных свойств. Для придания свойств прядо-мости прядильные растворы белков подвергают созреванию. Затем их продавливают через фильеру в коагуляционную ванну. Формование волокна осуществляют в кислотно-солевых коагуляционных ваннах, где тонкие струи прядильного раствора переводят из жидкого в студнеобразное состояние. Обычно используют несколько последовательно расположенных ванн, содержащих растворы кислот, солей (натрия, алюминия, хрома), Сахаров и формальдегида с различной концентрацией и температурой. После коагуляцион-ной ванны для упрочнения и повышения водостойкости тонкие нити подвергают одноосному растяжению (ориентационная вытяжка). Эту операцию обычно выполняют при нагреве в горячей воде или в паре. Текстильные волокна сушат затем до влажности 10—15%. Более детально методы получения искусственных белковых волокон рассмотрены в [149]. Физико-химические аспекты получения волокон макромолекулярных веществ рассмотрены в работах Папкова [158—160].
Искусственные белковые волокна производились во многих странах в качестве заменителей шерсти, но в настоящее время выпускаются в очень небольших масштабах. Быстрое свертывание их производства в послевоенное время обусловлено недостаточно высокой прочностью этих волокон во влажном состоянии, высокой стоимостью и дефицитом сырья — чистых пищевых белков, производство которых в атот период было весьма ограниченным, а также сильной конкуренцией со стороны других искусственных и синтетических (полиэфирные, полиамидные и др.) волокон. В это же время были начаты исследования по получению белковых волокон для пищевых целей. В отличие от текстильных они должны содержать большое количество воды или легко набухать после высушивания. Прочностные характеристики волокон здесь играют меньшую роль, однако такие волокна должны выдерживать нагрев в условиях кулинарной обработки (варка — около 100°, жарение и печение — 140—220°).
Первые пищевые соевые волокна были получены Боером в 1947 г., а в 1953—1954 гг. ему были выданы первые патенты на получение ИМВ [157]. Принцип получения ИМВ, предложенный
| Глава четвертая |
в работах Боера, не претерпел затем существенных изменений [157, 161-163].
В конце 60-х годов был разработан новый принцип получения искусственных мясопродуктов — экструдирование концентрированных водных дисперсий белков под давлением и при температуре выше температуры кипения воды. В результате получают анизотропные пористые (открытые асимметричные ячейки) продукты, хорошо имитирующие традиционные мясные изделия. Этот метод получил развитие в течение нескольких последних лет для производства аналогов и разбавителей низкой стоимости.
В настоящее время метод прядения белковых волокон и метод экструзии широко используются для производства искусственных мясопродуктов в промышленном масштабе. Ниже оба метода будут рассмотрены несколько подробнее. Сведения о процессах изложены исключительно в патентных публикациях.
Прядение белковых пищевых волокон и. их переработка в искусственные мясопродукты
Согласно способу Боера [157], прядильный раствор белка в растворе щелочи подают через фильеру в кислотно-солевую коагу-ляционную ванну и полученные волокна подвергают ориентацион-ной вытяжке на 50—400%. Ориентационная вытяжка является существенным элементом процесса. Она приводит к упрочнению волокон и частичной потере ими воды в результате вынужденного синерезиса. Неподвергнутые вытяжке волокна хрупки, недостаточно прочны и легко сминаются. Волокна смешивают со связующим, содержащим пищевые, вкусовые, ароматические вещества и красители, и пропускают через ванну с нагретым жиром. Боер предложил приемы получения ИМВ — аналогов различных мясопродуктов, предусмотрел возможность обогащения продукта аминокислотами, витаминами и белками и «мягчения» готового искусственного мясопродукта с помощью протеолитических ферментов. Для улучшения вкуса, цвета и биологической ценности продукта он предложил [161] эмульгировать липиды в прядильном растворе белка и вводить в него ароматизирующие вещества и красители.
Белковые волокна было предложено также использовать без связующего для получения ИМВ путем их нагрева в форме до частичного сплавления [164, 165 ]. Ряд работ относится к введению в прядильные растворы белка натуральных и синтетических отдушек и получению таких отдушек, имитирующих запах различных видов традиционных мясных изделий [5, 108, 113, 124, 166—175].
Боер [162] отметил далее существенное влияние величины рН белковых волокон на их прочностные свойства и на консистенцию
Способы полученияИПП
искусственного мясопродукта. Он предложил вместо промывки волокон водой обрабатывать их после коагуляционной ванны раствором щелочи в пейтрализациоиной ванне с тем, чтобы рН волокон был около 4,7—7,0 (преимущественно 5,5—6,2). Коагуляци-онная ванна обычно имеет рН 3,0 и ниже; значение рН волокон того же порядка. При рН ниже 4,0 белковые волокна очень жестки, на вкус они сухие и кислые. При рП выше 7,0 волокна очень эластичны, слишком нежны па вкус и при пагрове могут необратимо набухать и растворяться. После обработки в исйтрализаци-опиой ванне (0,5—12% NaCI и 3,5% NaOH) волокна приобретают необходимые прочностные и осмотические свойства. При переже-выиапии они очень похожи па подокна натурального мяса.
Еще одно усовершенствование процесса, сделанное Боером [163], относится к стадии получения прядильного раствора. Созревание прядильного раствора белка в щелочи при рП 12—13 продолжается до 24 час. Процесс сопровождается частичным гидролизом пептпдных цепей белка и разрушением некоторых аминокислотных остатков. Прядильный раствор приобретает поэтому специфический неприятный запах. Это явление может быть частично или полностью устранено добавлением к прядильному раствору сульфитов. В результате улучшается вкус, запах и консистенция готовых искусственных мясопродуктов. Механизм действия сульфитов и других серусодержащих соединений обсуждался во многих работах, по остается невыясненным [113, 115 ]. Было предложено также добавлять сульфиты к готовым белковым волокнам [163], вводить их в коагуляциопную или промывную ванну [176], а также использовать SOa для осаждения белков из щелочных растворов при получении изолятов белка соевых бобов, предназначенных для переработки прядением [177].
Ряд работ посвящен снижению продолжительности процесса созревания прядильного раствора строгой дозировкой щелочи, поддержанием температуры и концентрации белка в определенном узком интервале [177—179], а также добавлением поверхностно-активных веществ [180] и кислых полисахаридов [181]. Были разработаны устройства, позволяющие сократить время созревания прядильного раствора и осуществить процессы получения раствора и его прядение по непрерывной схеме [177, 179]. Кроме того, разработаны технология и аппаратура для непрерывной обработки белковых волокон в коагуляциошюй, промывной и нейтрализационной ваннах [177, 182, 183], непрерывного пропитывания волокон связующим [179], ориентирования пучков волокон и отверждепия связующего (рис. 30) [177, 179, 188].
Дальнейшее совершенствование способов получения ИМВ шло как в направлении придания волокнам и продукту достаточной устойчивости к нагреву в условиях кулинарной обработки [185— 187 ], так и регулирования состава, биологической ценности про-
184 Глава четвертая
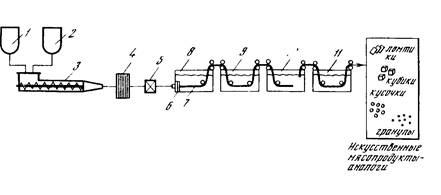
|
| f | /ff | |
| gLrU | ||
| s | Ш qa» |
ffcvyrcmffemw
WnWffflffl7ffK/77W-
awawzu
Рис. 30. Схема производства белковых волокон и искусственных мясопродуктов (ИМВ) с использованием техники мокрого прядения
1—аппарат для приготовления концентрированного раствора белка; 2—аппарат для раствора щелочи; з — шнековый смеситель-дозатор; 4 — фильтр; 5 — прядильный насос; 6 — фильера; ? — белковые волокна; s — коагуляционная ванна; 9 — промывная ванна; 10 — ванна со связующим; и — ванна для обработки жиром (ванна может содержать ароматические вкусовые вещества и красители)
дукта [184, 189] и переработки в искусственные мясопродукты волокнистой структуры различных белков, например изолята белка подсолнечника [188].
Степень набухания и прочностные свойства белков предложено регулировать путем добавления в коагуляционную ванну полиак-риловой кислоты [190] при рН, близких ИЭТ белка, введения в прядильные растворы кислых полисахаридов [181] и прядения смесей белков, например изолята соевого белка и казеина [184]. В последнем случае, помимо повышения прочности волокон соевого белка за счет введения казеина, возрастает также и биологическая ценность искусственного мясопродукта.
Для повышения прочности и стабильности при нагреве белковых волокон предложено также вводить в коагуляционную ванну алюминиевые квасцы [186]. Более интересное решение вопроса состоит, однако, в получении альгинатпых и пектиновых волокон, которые содержат белки в качестве наполнителя. В этом случае можно перерабатывать белки различного происхождения, в том числе имеющие более низкие функциональные свойства. Иными словами, способ достаточно «универсален по белку» и позволяет регулировать состав и снизить стоимость искусственных мясопродуктов волокнистой структуры. Кроме того, такие искусственные продукты пригодны для многих видов кулинарной обработки, так как студни альгината и пектипата кальция не плавятся при нагреве. В прядильные растворы альгината или пектината вводят белки, например, казеин, яичный альбумин, клейковину, изолят белка бобов сои и т. п., а также вкусовые, пищевые и ароматизи-
Способьг полученияИПП
рующие вещества или продукты, такие, как жиры (говяжий, бараний, куриный), растительные масла, муку семян масличных или злаковых' культур, глютаминат натрия и красители. Раствор продавливают через фильеру в коагуляционную ванну, содержащую раствор солей кальция. Волокна диаметром 0,075—1,3 мм подвергают ориентационной вытяжке и затем соединяют с помощью связующего (альбумин, крахмал, высокоплавкие жиры и т. п.) или же без связующего нагревом в форме. Так получают аналоги мяса животных, рыбы или птицы. Недостаток этого способа связан с низкой стабильностью студней альгината и пектината кальция в присутствии избытка поваренной соли. Ионный обмен (в процессе варки в подсоленной воде) может приводить к чрезмерному набуханию продукта и ухудшению его консистенции. Поэтому предложено [187] добавлять в коагуляционную ванну соли алюминия, обмен которого на ионы натрия протекает
значительно медленнее, чем ионов кальция.
Еще один метод, позволяющий регулировать состав искусственных мясопродуктов волокнистой структуры, состоит в использовании полых пищевых волокон [189]. Эти волокна в процессе прядения, с помощью специальной смесительной фильеры, или же после прядения (под давлением) заполняют пищевыми веществами. Концы волокон после их заполнения могут быть закрыты оплавлением, с помощью связующего или заливочных композиций. В полые волокна можно вводить вещества, чувствительные к кислороду воздуха, например, прогоркающие жиры или полиненасыщенные жирные кислоты, а также неприятные на вкус вещества
для маскировки их вкуса.
Интересный прием получения искусственных мясопродуктов волокнистой структуры, принципиально отличающийся от предложенного Боером, был разработан в 1955 г. Ансоном и Педером [191, 192]. Для получения белковых студней они воспользовались методом нагрева концентрированных дисперсий белков, т. е. методом, применяемым для получения ИМР (см. выше). Это позволило отказаться от обычной техники мокрого прядения. Дисперсию белка (20—W°lo белка сои) экструдируют в виде сравнительно толстых нитей (диаметр до нескольких миллиметров), которые посыпают порошкообразным связующим (смесь крахмала с сухим молоком), слегка спрессовывают и нагревают (рис. 31). Тонкие жесткие слои связующего заполняют пространство между нитями белкового студня и создают характерное ощущение при пережевывании, сообщая продукту мясоподобную неоднородную консистенцию.
Этот способ получения искусственных мясопродуктов волокнистой структуры был разработан почти одновременно с первыми работами Боера, но не получил дальнейшего развития и, как недавно сообщено [124], не был использован в промышленности.
186 Глава четвертая
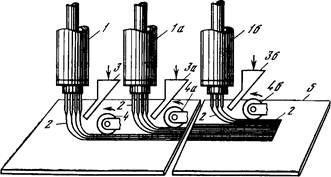
Рис. 31. Схема получения искусственных мясопродуктов волокнистой структуры по Ансону и Педеру
1—16—экструдеры; s—белковые нити; S—зб—сухое порошкообразное связующее;
4—46 — прессующие валики
Основной путь получения искусственных мясопродуктов волокнистой структуры связан, следовательно, с мокрым прядением белковых волокон (см. рис. 30).
Для получения пищевых волокон, в отличие от текстильных, в качестве прядильных растворов используют только щелочные растворы белка, частично нейтрализованные за счет буферной емкости белка и продуктов его гидролиза.
Жидкая струя прядильного раствора при выходе из отверстий фильеры в коагуляционную ванну имеет диаметр, приблизительно равный диаметру отверстий фильеры, хотя диаметр струи может несколько возрасти за счет ее эластического расширения. Обычно используют кислотно-солевые коагуляционные ванны. Переход жидкой струи в студень цилиндрической формы, т. е. образование волокна, сопровождается рядом сложных, протекающих во времени процессов, учет которых весьма важен и определяет выбор характеристик коагуляциопной ванны (состав, температура, протяженность) , скорости прядения и других параметров процесса.
Наряду с кислотой (нейтрализация щелочного прядильного раствора) п объем жидкости струи из коагуляционной ванны диффундируют соли, которые могут изменить растворимость и углубить процесс коагуляции отдельных фракций белка. Снижение величины рН прядильного раствора в область ИЭТ белков сопровождается нарастанием межмолекулярного и межагрегатного (элементы структуры студня) взаимодействий, резким повышением вязкости струи, образованием в потоке студня ориентированной структуры. Дополнительное количество соли, образующееся при нейтрализации жидкой струи, изменяет осмотические свойства во
Способы полученияИПП
локна. Образование волокна обычно заканчивается на начальном участке коагуляционной ванны. Ввиду того что диаметр струи весьма мал, процессы диффузии протекают быстро. Этому способствуют высокие градиенты концентрации компонентов между струёй и ванной, нагрев и перемешивание содержимого ванны. При нейтрализации струи, образовании студня, а также за счет вынужденного синерезиса при фильерной вытяжке выделяется вода. Диффузионный перенос воды из струи прядильного раствора и волокна в коагуляционную ванну разбавляет содержимое последней и ведет к выравниванию осмотических свойств волокна и ванны. Значительная потеря воды волокном происходит далее за счет синерезиса студня и вынужденного синерезиса при ориента-ционной вытяжке. Поэтому если на начальном участке коагуляционной ванны объем студня близок к исходному объему прядильного раствора, то к концу коагуляционпой ванны он резко снижается за счет потери воды. В результате конечный диаметр волокон обычно в 2—4 раза ниже, чем диаметр отверстий фильеры.
Ориентационную вытяжку волокна обычно производят после коагуляционной ванны на последовательно расположенных роликах, вращающихся с возрастающими скоростями. Эту операцию выполняют при нагреве, что облегчает ориентацию элементов структуры студня в поле сдвига за счет увеличения их подвижности. Поскольку значительная степень сшивки макромолекул и элементов структуры студня, как правило, затрудняет вытяжку волокон, их дополнительное дубление (например, алюминиевыми квасцами) производят после ориентациопной вытяжки. Повышение степени ориентации структурных элементов и их взаимодействие приводит к резкому повышению прочностных свойств волокна и снижению содержания в нем воды. Последнее, однако, не всегда желательно с точки зрения состава и свойств конечного мясопродукта, и поэтому содержание воды в волокнах строго контролируется.
Ориентационную вытяжку чаще осуществляют одновременно с промывкой волокон для удаления компонентов коагуляционной ванны или же с нейтрализационной обработкой волокон. В ней-трализационной ванне величина рН волокон возрастает до 5—7, т. е. обычно несколько выше ИЭТ белка, и позволяет регулировать степень набухания волокон. Готовые волокна обычно хранят в растворе Nad.
Характеристики сырья и режимы большинства стадий процесса описаны в патентных публикациях [157, 161—165, 176—192] лишь в самом общем виде. Анализ патентной литературы дает возможность выделить следующие характерные особенности процесса. Прядильные растворы представляют собой 10—30%-ные растворы белка, преимущественно изолят белка соевых бобов, в 5—10%-ном растворе NaOH. Величина рН прядильного раство-
| Глава четвертая |
pa 9—13,5; вязкость 100—200 пз при 45°. Для прядения используют фильеры с 5 000—20 000 отверстий диаметром 0,02—0,2мм (чаще 0,08—0,1 мм). Коагуляционные ванны содержат 0,5—12% NaCI и 0,5—10% кислоты (уксусная, соляная, молочная, лимонная, фосфорная и т. д.) и имеют рН 1,0—4,0. Степень ориентаци-онной вытяжки составляет 50—400%. После нейтрализационной ванны волокна имеют рН 5,5—6,4, что соответствует рН большинства видов натурального мяса [193]. Сульфиты щелочных или щелочноземельных металлов добавляют на различных стадиях процесса. Волокна часто продолжительное время (неделя и более) выдерживают в коагуляционной ванне для старения. Готовые волокна поступают в продажу в увлажненном виде (3—6%-ный раствор NaCI при 5°). Большинство связующих — растворы или эмульсии типа «масло в воде», содержащие яичный альбумин (см. ниже). Готовые продукты нарезают, высушивают, консервируют или замораживают.
Фирма «Дженерал миле» применяет для получения пучков волокон (по 96 тысяч моноволокон) 6 платино-родиевых фильер, каждая с 16000 отверстий диаметром 0,025—0,075 мм [103—105, 107, 111]. В качестве сырья используют изолят белка соевых бобов 95—98%-ной чистоты. 16%-ный раствор изолята соевого белка в растворе NaOH с рН 12 выдерживают около 10 мин. при комнатной температуре и прядут через фильеру в коагуляционную ванну (рН 3,5), содержащую уксусную, соляную кислоты и NaCI.
Фирма «Вортингтон фудз» использует 20%-ные прядильные растворы изолята белка бобов сои с высоким КДБ, не содержащие примесей целлюлозных волокон [121]. Фильера имеет 15000 отверстий диаметром 0,1 мм. Коагуляционная ванна (рН 2,5) содержит 8% NaCI и фосфорную кислоту. После нейтрализационной ванны волокна имеют рН 5,0—6,0. Их промывают водой и нарезают (длина около 150 мм).
Реологические свойства прядильного раствора белка сои и во-доудерживающая способность волокон и искусственных мясопродуктов волокнистой структуры обсуждаются в работах [194, 195]. Хотя получение искусственных мясопродуктов волокнистой структуры является наиболее развитой областью производства искусственных продуктов питания, этот процесс явно недостаточно проработан в научном и технологическом отношении [116]. Весьма актуальны задачи удешевления процесса, повышения биологической ценности продуктов и переработки белкового сырья высокой гетерогенности. Повысить биологическую ценность волокон можно, в частности, исключив применение щелочи для получения изолята белка сои и его прядильных растворов. В этом отношении интересны работы [124, 181, 185, 187] (см. также гл. II).
Использование белков в качестве студнеобразователей (в том числе при производстве волокон) связано с высокими требования
Способы получения ИПП
ми к стандартности, однородности и функциональным свойствам белкового сырья. Оно, как отмечалось выше (см. гл. II и III), обычно представляет собой сложную смесь белков с различной растворимостью (альбумины, глобулины, глютелины, проламины), отличающихся условиями коагуляции, студнеобразования и свойствами студней. Это обстоятельство существенно усложняет переработку белков в сравнении, например, с синтетическими полимерами. Поэтому весьма сложно получить изоляты белка и переработать их в волокна без существенных потерь белка. Даже в случае белков соевых бобов ввиду различия условий коагуляции и студнеобразования отдельных фракций потери достигают 70% [120]. Между тем белки сои и другие, перерабатываемые в настоящее время в волокна резервные белки семян, имеют сравнительно невысокую гетерогенность. Фракционный состав таких белков обычно становится более узким при получении изолятов. В то же время наиболее перспективные виды белкового сырья, такие, как белки дрожжей, других одноклеточных культур и зеленых листьев, представляют собой сложную смесь функциональных белков. Поэтому гетерогенность этих видов белкового сырья принципиально очень высока. В связи с этим представляют интерес методы переработки белков без использования мокрого прядения. Предложено, например [196], продавливать через капилляры нагретые концентрированные растворы дрожжевого белка с под-сушиванием и ориентационной вытяжкой волокон на воздухе, т. е. использовать технику сухого прядения.
Пищевые связующие для получения ИМВ
Способы получения искусственных мясопродуктов волокнистой структуры без использования связующих [164, 165] составляют скорее исключение, так как основаны на сплавлении белковых волокон при нагреве, в результате чего такие мясопродукты могут быть использованы лишь в холодном или слегка подогретом виде. Кроме того, при их получении вкусовые, ароматические и окрашивающие вещества вводят в исходные прядильные растворы, а не в связующее. Это усложняет процесс прядения волокон и приводит к потерям указанных веществ за счет диффузии в коагуляцион-пую, промывную и нейтрализационную ванны. Так же редко применяют и заливочные композиции (жиры) [189].
Сведения о составе, способах получения и применении связующих содержатся в ряде патентных сообщений. В большинстве случаев связующее представляет собой водный раствор или дисперсию белков, образующих при нагреве студни. Кроме того, в нем содержатся (в виде раствора эмульсии или суспензии) пищевые вкусовые ароматизирующие вещества и красители [197— 199 ]. Способы получения связующих по существу аналогичны
190 Глава четвертая
рассмотренным выше способам получения ИМР. Практически большинство студнеобразующих систем для получения ИМР [127—142] может быть применено в качестве связующих для белковых волокон.
В качестве белков, образующих при нагреве студни, для получения связующих используют яичный альбумин, клейковину пшеницы и изолят соевого белка (обычно в форме протеината натрия) [197, 199, 200], а также смеси этих белков, например, яичного альбумина и изолята белков соевых бобов [201], яичного альбумина и клейковины пшеницы [198, 199 ]. Для получения ИМВ, устойчивых при продолжительном нагреве, предложено применять связующее на основе комплекса белка с каррагенином [202] или альгинатом натрия [203].
Обычно для получения связующих в растворе или коллоидной дисперсии белка эмульгируют растительные масла и расплавленные жиры [198—201, 205]. Для эмульгирования в растворы белка вводят поверхностно-активные вещества, например моно- и дигли-цериды жирных кислот.
Для придания продукту необходимого вкуса и запаха используют гидролизаты растительных белков или дрожжей, глютаминат натрия, коптильные жидкости и копченые дрожжи, пряности и специи, животные жиры и бульоны. Кроме того, в состав связующих предложено вводить небольшие количества фарша или тонкоизмельченного мяса низших сортов, мясную муку и подобные натуральные компоненты [206—209 ]. В свою очередь, связующие используют для соединения волокон натурального мяса [210] и небольших кусочков мяса низших сортов [211, 212], что позволяет повысить эффективность мясоперерабатывающсй промышленности, а также однородность и качество ее продукции. Благодаря доступности и дешевизне отходов производства и переработки мяса синтетические добавки и ароматические композиции применяются пока весьма редко [108]. Тем не менее предложен ряд процессов получения таких композиций, имитирующих запах различных традиционных мясопродуктов.
В качестве красителей используют красные пищевые красители, карамельные красители, карамелизованный сахар, порошок какао и т. п.
Для непрерывного пропитывания волокон связующими предложена различная аппаратура [199, 200, 204 ]. При получении ИМВ с высокой степенью анизотропии пучки коротких волокон ориентируют с помощью специальных устройств [198] или непрерывно пропускают волокна через ванну со связующим и ориентирующие нагреваемые ролики [199]. При получении искусственных мясопродуктов, имитирующих бекон, волокна хаотически располагают в макроскопических слоях, содержащих окрашенное и неокрашенное связующие [201].
Способы получения ИПП 191
Обычно содержание белковых волокон в ИМВ (на сухой вес) составляет 20—50% (фирма «Вортингтон фудз») [121] или 30—60% [104] (фирма «Дженерал миле»), т. е. в среднем эти продукты содержат около 40% волокон, а 60% приходится на компоненты связующего (белок—10%, жир—20%, другие пищевые, вкусовые вещества, отдушка и красители—30%) [105]. В готовом виде ИМВ содержат 50—70% воды. Сведения о составе, калорийности и биологической ценности этих продуктов приведены в табл. 45 и 46 (см. стр. 196—197).
ИСКУССТВЕННЫЕ МЯСОПРОДУКТЫ ПОРИСТОЙ СТРУКТУРЫ (ИМП)
Для получения этих искусственных мясопродуктов не обязательно применять дорогостоящие изоляты белка бобов сои, не нужно получать волокна и использовать связующие. Основным сырьем служат концентраты белка и обезжиренная мука соевых бобов с соответствующими функциональными свойствами, перерабатываемые в виде высококонцентрированных водных дисперсий. Существует два основных приема получения подобных продуктов, различающихся режимом деформирования дисперсий белков.
В первом случае дисперсии интенсивно перемешивают при нагреве. При этом возникает анизотропный студень волокнистой структуры, который в условиях непрерывной деформации может быть разорван механически на отдельные кусочки небольшого размера, высушиваемые при высоких температурах для получения искусственных мясопродуктов. Этот прием иногда называют методом раздира [НО].
Во втором случае высококонцентрированную дисперсию белка экструдируют при температуре выше 100°, под давлением в среду с более низкой температурой и давлением, так, чтобы на выходе из головки экструдера в результате сброса давления происходило вскипание воды экструдата. Экструдат затем нарезают на небольшие кусочки и подвергают дополнительной сушке. Этот прием называют экструзионным [110, 114].
Продукты, полученные методами раздира и экструзии, имеют структуру типа пен, с открытыми асимметричными ячейками, вытянутыми в направлении деформации, и непрерывной белковой фазой в виде ламелей или волокон. При описании структуры этих продуктов обычно говорят о поропластах с волокнистой макроструктурой. Для обозначения искусственных мясопродуктов этого вида часто используют термины: текстурированные растительные белки (TVP — Textured Vegetable Protein) или текстурированные соевые белки (TSP—Textured Soy Protein). Иногда этими тер-
192 Глава четвертая
минами обозначают также и искусственные мясопродукты волокнистой структуры. Поэтому, во избежание путаницы, мы будем использовать термин «искусственные мясопродукты пористой структуры» (ИМП).
Искусственные мясопродукты пористой структуры по внешнему виду, макроструктуре и консистенции хорошо имитируют некоторые виды традиционных мясопродуктов. Они используются в виде аналогов и разбавителей традиционных мясопродуктов. В последнем случае окрашивание и ароматизация ИМП не обязательны. В качестве аналогов небольших кусочков сухого мяса, которые хорошо хранятся и быстро набухают при варке, ИМП применяют, например, для приготовления сухих супов, соусов, мясных начинок, рагу и других блюд. Как разбавители ИМП находят применение при производстве колбасо-сосисочных изделий, рубленых мясопродуктов, котлет и т. п. Содержание разбавителя может достигать 45% и выше от количества натурального мяса [121].
Исходные высококонцентрированные дисперсии белков обычно получают добавлением воды к КБ или ОМ сои в виде сухого порошка или же коагуляцией изолята белка сои из раствора. В дисперсию вводят различные пищевые, вкусовые, ароматизирующие и окрашивающие вещества и композиции, особенно при получении ИМП-аналогов.
Метод раздира был предложен несколько раньше [213—217] метода экструзии [218—223]. Этим методом перерабатывают дисперсии белков, близкие по составу дисперсиям, используемым для получения ИМР и связующих, но более концентрированные. Образование студня здесь происходит в потоке при высоких градиентах скорости сдвига, в температурном режиме, обеспечивающем достаточную пластичность дисперсных частиц белка. Исследование механизма образования анизотропных студней, выполненное на модельных системах (см. гл. II), показало, что в основе предложенных способов получения ИМП лежит процесс деформации двухфазных жидких систем с переводом одной из фаз в студнеобразное состояние с образованием анизотропных студней капиллярной структуры (см. рис. 9). Важными параметрами процесса являются концентрация дисперсии, величина рН, содержание солей, температура и режим деформирования. Нагрев дисперсии обеспечивает на первой стадии процесса необходимую степень набухания и пластичность дисперсных частиц белка, а на второй — перевод деформированных в потоке дисперсных частиц в студнеобразное состояние. Концентрация белковой дисперсии должна быть достаточно высокой, чтобы обеспечить сильное взаимодействие пластичных дисперсных частиц, их деформацию в потоке с образованием непрерывной волокнистой макроструктуры. Анизотропный студень затем высушивают.
Способы получения ЙШ1 193
Для получения искусственных мясопродуктов методом раздира используют, например, 50—80%-ную водную дисперсию на основе изолята или концентрата соевого белка (можно вводить обезжиренную муку соевых бобов, муку мяса, рыбы и т. п.), которую нагревают в автоклаве при перемешивании (30— 500 об/мин) за 1—2 мин. от комнатной температуры до 165— 180°, а затем быстро охлаждают до 35—65°. Получают продукт в виде кусочков небольшого размера, с концентрацией на 5— 10% выше, чем исходной дисперсии, сушат и используют как аналог или разбавитель [213]. В другом случае в 30%-ную дисперсию свежеприготовленной клейковины пшеницы вводят сухой яичный альбумин и обезжиренную соевую муку. После интенсивного перемешивания (около 10 мин.) композицию с волокнистой структурой нагрепают в течение нескольких минут при 115° и получают устойчивый к нагрову искусственный мясопродукт [215]. Подобный продукт на основе клейковины, изолята белка соевых бобов, казеина или смеси этих белков предложено [217] также получать коагуляцией белков из щелочных растворов при нагревг л интенсивном перемешивании. Волокнистая структура коагулята фиксируется нагревом или введением солей кальция. Коагулят содержит 40-70% воды. Его нейтрализуют, тщательно промывают водой и сушат. Продукт пригоден для продолжительного хранения и использования в качестве разбавителя.
Метод раздира обычно требует более высокоочищенных форм белка, чем метод экструзии. Кроме того, он может быть применен лншт, для переработки студнеобразующих (при нагреве) систем строго определенного состава. Здесь к тому же используют весьма дефицитные и более дорогие белковые студнообразователи, например свежевыделенпую клейковину пшеницы, яичный альбумин, изоляты и концентраты белка соевых бобов или смеси этих белков.
Метод экструзии получил большее распространение. Он позволяет перерабатывать белковое сырье с 40—75'%-пым содержанием белка, т. о. обезжиренную муку и концентраты белка соевых бобов.
Принципиальная схема получения искусственных мясопродуктов пористой структуры методом экструзии показана на рис. 32 [222].
Первый патент, описывающий метод экструзии, был выдан в 1966 г. [218]. Согласно этому способу, перерабатывают белки масличных культур в виде обезжиренной муки, концентратов или изолятов белка. Дисперсия содержит более 30% белка, 10— 60% воды и до 3% поваренной соли и хлористого кальция, который повышает вязкость экструдата и действует как сшивающий агент. Температура смеси составляет от 115 до 175°. В этих условиях не происходит заметной деструкции экструдата. Давление в экструдере более 7 кГ/см'1, но предпочтительно около 70 кГ1см1.
Ч^? В. Б. Толстогузов
194 Глава четвертая
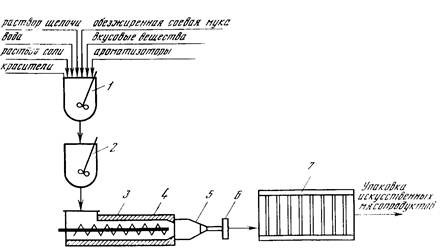
1*110. 32. Схема производства искусственных мясопродуктов (ИМИ) методом ;жструзии
1—аппарат для смешения компонентов; 2—аппарат для созревании системы;
S—экструдер; 4—обогрев икструдера; Л—акструзионная голоикн; в - - нож для нарезки экструдата; 7 -- аппарат для охлаждения и гушки
Повышение давления увеличивает скорость экстру дировання, повышает пористость продукта и его способность к рептдратации после сушки, а также придает ему более отчетливую волокнистую
макроструктуру.
Была также разработана специальная аппаратура для экструзии белковых дисперсий [219, 220, 222]. Пластичную белковую дисперсию перемешивают под давлением при нагреве в шнековом смесителе и непрерывно экструдируют через узкий длинный капал, на конце которого крепится экструзиопная головка [219]. Экструдат с хорошо ориентированной структурой поропласта разрезают и сушат.
С целью улучшения пористой волокнистой структуры продукта, его консистенции и органолептичсских свойств (в сваренном виде) предложено вводить в исходную дисперсию белка элементную серу, а также сульфиды натрия или калия в количестве 0,01—0,5% [220]. При экструзии дисперсий белков семян масличных большое значение имеет рН системы, который составляет 6,5—7,5 [218, 221 ]. При рН ниже 5,5 экструзия затруднена высокой вязкостью системы и продукт имеет низкую пористость. При рН выше 8,5 продукт приобретает горький вкус. Регулирование рН дисперсии, содержания в ней GaCL и режима экструзии позволяет получать ИМП (волокнистой макроструктуры), имитирую-
Спосибы полученияИПП
щне мясо цыпленка, говядину и другие мясные продукты. Плотность ИМИ составляет 0,5—1,3 г/см3. Они быстро набухают в кипящей воде, увеличивая свой вес за 15 мин. в 3—9,5 раза.
Для равномерной гидратации сухих ПМП и предотвращения их разрушения при варке Хоффман [223] предложил перед варкой пропитывать ИМП при нагреве растительным маслом или эмульсией пищевых масел. Эмульсия пищевого масла (преимущественно кокосового) в водной среде содержит также гидролизат растительного белка, соль и карамелизовапный сахар в качестве красителя. Кокосовое масло используют ввиду его сравнительно
высокой стабильности при хранении.
Хоффман [223] предложил'также получат!, ИМП не методом икструдироиания, а прессованием обезжиренной соевой муки под давлением выше 127 кГ/см2, преимущественно при Ю—350 кГ/см2, н при температуре, достаточной для нррсхода воды в перерабатываемой системе в пар при нормальном давлении. Полученный продукг имеет пористую волокнистую структуру, аналогичную мясной. Кроме того, удаление воды в виде пара при сбросе давления позволяет устранить свойственный обезжиренной соевой муке горьковатый вкус. По внешнему виду и консистенции он
имитирует изделия из говядины.
Рассмотренные выше методы раздира и акструзии, а также относящийся к этой группе методов способ переработки сокоагу-лятов белка и кислого полисахарида [224] являются частным случаем рассмотренного в гл. II способа переработки двухфазных систем с целью получения анизотропных студней капиллярной структуры. Как было показано выше, при переработке двухфазных жидких систем имеются и другие принципиально возможные способы получения искусственных мясопродуктов и белковых волокон без использования техники мокрого прядения (см. рис. 9,
гл.11).
Подавно был предложен еще один пуп. получении искусственных мясопродуктов — аналогов и разбавителей. Он заключается в получении пористых материалов волокнистой структуры, которые могут быть пропитаны пищевым связующим. Способ получения пористой губки на основе белка бобов сои предложили Окумура и Уилкинсои [30]. Он основан на способности соевого белка денатурировать при медленном замораживании водных дисперсий [27], т. с. эффекта, издавна используемого в Японии для получения пористого сооиого творога кори-тофу. С ;)той целью сравнительно разбавленную дисперсию соевого белка в воде замораживают в виде блока, состоящего из мелких кристаллов льда волокнистой формы, и после оттаивания и удаления воды получают пористый продукт волокнистой текстуры. Создание подобных пористых структур на основе кислых полисахаридов [225] представляет собой более универсальный путь получения искусствен-7*
190 Глава четвертая
пых мясопродуктов. Это объясняется прежде всего том, что в состав связующего можно вводить и перерабатывать таким путем различные белки, ;i кроме того, образующиеся при этом ионотроиные студни кислых полисахаридов устойчивы к нагреву [226, 227] (см. гл. TI).
Производство искусственных мясопродуктов пористой структуры успешно конкурирует с производством искусственных мясопродуктов волокнистой структуры. Пока только эти два нроцес-са освоены в крупном промышленном масштабе. Преимущество
Таблица •/.7
Спстип (в %) iicm/rr'i'RdtHbl.T мясопрпдчктоп /шлпкнистпи структуры— аналогии типа «Гкштррй» фирмы ^Джгперпл миле», США Ю-'i]

процесса прядения волокон заключается в высокой технологической гибкости [121, 125]. Комбинирование волокон со связующим при варьировании состава и (ризических параметров обоих компонентов позволяет производить широкий ассортимент аналогов традиционных изделии из мяса животных, птицы и рыбы. Производство искусственных мясопродуктов волокнистой структуры (фирмы «Дженерал миле инк.» и «Майлз лебореториз») основано, однако, на прядении изолятов белка, т. с. на переработке наиболее дорогого вида белкового сырья. Этот процесс сопровождается значительными потерями (до 70%) белка бобов сон и снижением биологической ценности продукта, для компенсации чего приходится прибегать к обогащению аминокислотами или же использовать в составе связующего белок со взаимодополняющим содержанием аминокислот. Отсюда сравнительно высокая стоимость белковых волокон. Пх поэтому используют для имитации наиболее дорогих мясопродуктов, а также в качестве разбавителя дорогостоящих натуральных мясопродуктов [228] или же, наконец, вводят в искусственные мясопродукты, получаемые методом экструзии.
Состав некоторых искусственных мясопродуктов волокнистой структуры приведен в табл. 45 и 46.
Как отмечено выше, методом экструзии перерабатывают обезжиренную соевую муку и концентраты белка соевых бобов, т. е. значительно более дешевые виды белкового сырья. Их переработка
Способы получения ИПП
Таблица 46
Счета» и биологическая ценность (КЭБ) некоторых натуральных nil'life я ы. г продуктов и искиест'венных мясопродуктов — аналогов говядины [ 70.7, 107, У/О, 1J3, 115}
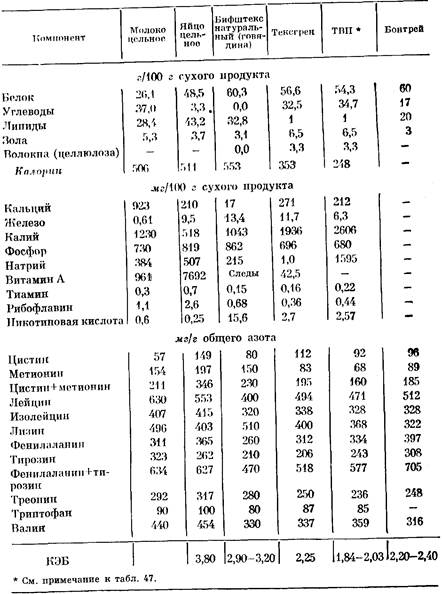
198 Глава четвертая
v ИМП не сопровождается потерями белка и снижением биологической ценности; напротив, для обезжиренной соевой муки она даже возрастает. Кроме того, стоимость оборудования для производства ИМП приблизительно вдвое ниже, чем в случае волокнистых продуктов. Поэтому в готовом виде ИМП и 3—8 раз дешевле ИМП [229]. ИМП производят фирмы «Арчер Даниельс мидланд ко.», «Свифт энд ко.» и др. (табл. 46 и 47). Будучи
Таблица 47
Состав (в %) искусственных мясопродукта пористой структуры, производимых методом, экструзии на. основе обезжиренной соевой лп/h-ii. некоторыми фирмами США [108, 242-245, 249]
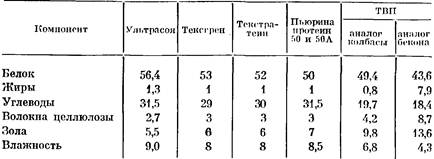
П р и м с ч а и и е. Торгопыс марки продуктов: ультрасоя—фирма «Фар-Мар ко.»;
тексгрен — фирма «Свифт энд ко.»; текстратеин — фирма «Каржил корп.»:
пыорина протеин 50 и 50А—фирма «Ральстон пыорина но.»; ТВП—фирма АДМ.
сварены в экструдорс н высушены, ИМП содержат около 50% белка и хорошо сохраняются продолжительное время. Метод экструзии не позволяет, однако, получать аналоги дорогостоящих мясопродуктов: бифштексов, отбивных, крупных кусков ветчины, мяса дичи и т. д.
Придание искусственным продуктам питания необходимого вкуса и запаха решается различными н [темами. Для производства ряда форм искусственной нищи, особенно молочных, крупя-но-макаронпых н т. it., основное значение имеет задача получения белкового сырья, лишенного постороннего вкуса и запаха как при комнатной температуре, так и при нагреве в увлажненном или сухом состоянии. Это важно также и при получении искусственных мясопродуктов. Г5о многих случаях идентифицированы соединения, определяющие специфический запах белкового сырья. и разработаны методы их удаления перегонкой с водяным паром, экстракцией полярными растворителями, микробиологическими методами.
Существен также учет химического взаимодействия компопен-
Способы получения ИПП 1?9
тов искусственного продукта с образованием вкусовых и ароматических веществ. Для придания необходимого вкуса и запаха искусственным мясопродуктам и другим искусственным продуктам питания используют гидролизаты белков, натуральные и синтетические композиции. Натуральные композиции дешевы, широко используются, но имеют тенденцию дорожать, нестандартны по свойствам, составу и неудобны в хранении. Многочисленные синтетические композиции представляют собой продукты реакции Майара [5, 27, 108, 113, 120, 124, 166-176, 230-234].
Сложнейшая научная задача в этой области связана с взаимодействием (обратимым, необратимым и конкурентным) компонентов вкусовых и ароматических веществ и других добавляемых в искусственный пищевой продукт низкомолекулярных вещеста (аминокислоты, красители) с белками, полисахаридами и липи-дами продукта. Солюбилизация бпоиолимерами, растворение н Л1ШИДНОЙ и водной фазах, сорбция на границе раздела фаз и ряд других сложных физико-химических процессов способны изменить равновесные концентрации вкусовых и ароматических веществ в растворе и давление паров летучих компонентов. Поэтому при добавлении какой-либо композиции к белку или искусственному пищевому продукту запах может исказиться или исчезнуть. В связи с этим исследуют взаимодействие индивидуальных компонентов запаха с белками и модельными системами в зависимости от характера их структурирования [175, 235—238 ].
Что касается стремления к возможно более полной имитации традиционных продуктов питания, то можно согласиться с точкой зрения Ансона [5] о его временном характере. Он отметил, что традиционные продукты сами по себе необычайно разнообразны, например мясопродукты, сыры и т. д., так что при создании аналогов можно стремиться лишь не выйти за чрезвычайно широкие пределы. Искусственные продукты питания должны быть, следовательно, привлекательны, но в будущем могут иметь оригиналь цый вкус, внешний вид и структуру.
ИСКУССТВЕННЫЙ ЖАРЕНЫЙ КАРТОФЕЛЬ
Интерес к искусственным картофслепродуктам обусловлен значительными потерями при производстве и хранении картофеля, трудностью его продолжительного храпения и необходимостью рационального использования продуктов переработки картофеля, пригодных для продолжительного хранения, таких, как картофельная мука, крупка и крахмал. Картофелепродукты отличаются слабой приедаемостыо и являются продуктами массового потребления в Европе п Америке [246]. В последнее время во многих странах мира получило распространение производство жареного
| Глава четвертая |
хрустящего картофеля как наиболее дорогого и удобного в использовании картофедепродукта. Поэтому работы в области искусственных картофелепродуктов посвящены преимущественно переработке картофельной муки, крупки и крахмала в различные виды искусственного жареного картофеля. При этом, учитывая низкое содержание белка в традиционных картофелепродуктах, предпринимают попытки повысить биологическую ценность искусственного жареного картофеля за счет введения белковых обогатителей.
Студнеобразующие системы для получения искусственных картофелепродуктов [247—255] в основном те же, что и для получения искусственных круп и макарон, а также некоторых связующих для искусственных мясопродуктов. В этом случае студни должны выдерживать нагрев при 140—220° в режиме жарения без существенного изменения формы. Вскипание воды при обжаривании в масле может сообщать продукту пористую структуру, напоминающую структуру искусственных пористых мясопродуктов, полученных прессованием. Для формования продукта обычно используют шнековые экструдеры, широко применяемые в пищевой промышленности [247, 255]. Экструдат нарезают кусочками, обжаривают к масле, посыпают солью, различными добавками и упаковывают.
В 1957 г. Райвоч [144, 145, 248] предложил два варианта процесса получения искусственного жареного картофеля на основе устойчивых к нагреву студней альгината кальция, наполненных картофельной мукой. В первом случае смешивают альгинат натрия, крахмал, картофельную муку и лактат кальция, добавляют воду; полученную тестообразную массу формуют в виде тонких пластин, которые после обжаривания в масле воспроизводят картофельные чипсы. Студни альгината кальция образуются в
результате растворения при нагреве и диссоциации лактата кальция.
В другом случае [249] для получения студня альгината или пектината кальция в раствор альгината натрия или пектина вводят нерастворимую в воде соль кальция, пищевые компоненты (крахмал, картофельную муку) и затем перед формованием системы быстро добавляют какую-либо пищевую кислоту, вызывающую образование растворимой соли кальция в системе и переход последней в студнеобразное состояние. Основной недостаток способа связан с высокой скоростью образования студня альгината или пектината кальция. Растворение солей кальция как при нагреве, так и при подкислении системы приводит к быстрому образованию микрочастиц студня вокруг растворяющихся частиц соли и, следовательно, к гетерогенности системы. Этим обусловлена трудность регулирования кинетики процесса и необходимость использования компонентов в тонкоизмельченном, тщательно перемешанном виде и применения высокоскоростных смесителей для быстрой
Способы полученияИПП 201
гомогенизации системы перед ее формованием. Практически смесь крахмала и тонкоизмельченного СаСОз диспергируют в растворе альгината натрия и затем быстро вводят смесь сухого крахмала с лимонной кислотой. После кратковременного интенсивного перемешивания смесь экструдируют в виде стержня, который нарезаю! на тонкие диски и обжаривают в масле. Райвоч предложил затем использовать в качестве студнеобразующей системы 2—4%-ный раствор метилцеллюлозы. В нем диспергируют овсяную, пшеничную муку или другие крахмалсо держащие продукты: тестовую массу экструдируют в виде ленты, нарезают и обжаривают [249].
Искусственный жареный картофель может быть приготовлен на основе наполненных белками смешанных студней альгината или пектината кальция и крахмала [250]. Такие студни получают при нагреве растворов кислых полисахаридов, содержащих в диспергированном виде крахмал, белок и глюконат кальция. Последний служит источником ионов кальция, освобождающихся при нагреве системы. Условия образования и свойства таких студней описаны в работах [101, 251 ]. В атом случае можно использовать белковые наполнители с весьма низкими функциональными свойствами, например сухое молоко, обезжиренное или необезжирен-иое, а также различные виды крахмалов (кукурузный, пшеничный, картофельный) или же картофельную крупку. По вкусу искусственный жареный картофель практически неотличим от натурального, а по биологической ценности значительно его превосходит [100].
Смесь компонентов для получения искусственных картофеле-продуктов может быть использована в виде сухого порошкообразного концентрата. При добавлении к концентрату горячей воды в соотношении от 1 : 5 до 1: 12, после перемешивания в течение нескольких минут могут быть приготовлены картофельный суп, пюре и подобные блюда; при соотношении от 1 : 0,8 до 1 : 2— тестообразная масса, из которой готовят искусственный жареный картофель. Такой концентрат пригоден для продолжительного хранения, легко транспортируется и может быть переработан в готовые изделия как на предприятиях общественного питания, так и в домашних условиях.
В большинстве других работ в качестве основного студнеоб-разователя предлагается использовать крахмал или его смеси с белками. Так, хрустящий искусственный картофель предложено получать смешением картофельной муки, крахмала, соли и воды [252]. Тестообразную массу экструдируют в виде ленты (IX Х3,2 мм}, которую режут и подсушивают до влажности 6—10% для образования плотного наружного слоя. Содержание воды снижают, чтобы устранить излишнюю пористость продукта за счет вскипания воды при обжаривапии. Жарение производят в горячем (180—210°) масле в течение 6—10 сек. Подобным же образом
8 В. Б. Толстогузов
| Глава четвертая |
[253] тесто с влажностью 12—35% готовят смешением кукурузной муки, крупы или других крахмалсодержащих продуктов с водой и солью, пропускают через тестомесилку-экструдер специальной конструкции, где тесто быстро нагревают до клейстеризации крахмала, охлаждают до 70—90°, выводят в виде непрерывной ленты, разрезают, сушат до влажности 5—12% и обжаривают в масле. Получают хрустящий продукт пористой структуры.
Аналогичным образом предложено получать чипсы, аромати-зированные и окрашенные под цвет обжаренного бекона [254]. Для этого в тестовую массу на основе смеси пшеничной и овсяной муки добавляют гидролизат растительного белка, соль, аромати-зирующие вещества и краситель. Тесто раскатывают, нарезают ломтиками, сушат 10 мин. при 140—220° и пропитывают растительным маслом.
Для получения искусственного жареного картофеля повышенной биологической ценности [255] в качестве студнеобразовате-ля наряду с крахмалом используют клейковину пшеницы. Тестовую массу получают смешением клейстеризованного крахмала восковидной кукурузы (амилопектина), клейстеризованного картофельного крахмала, клейковины, маргарина и воды. Тесто формуют в виде ломтиков толщиной около 2,5 мм, подсушивают в вакууме до влажности около 12% и обжаривают при 135—150°. Содержание белка (клейковины) в продукте около 15%, общее содержание жира 22—25%, в то время как ч обычном жареном картофеле оно составляет 40% и выше. Готовый продукт по вкусу не отличается от жареного картофеля или превосходит его. Такой способ, однако, относительно сложен (сушка в вакууме), а требования к сырью весьма жесткие. Необходимый комплекс физических свойств смешанного студня, клейковины и крахмала, обеспечивающий требуемую консистенцию готового продукта, достигается лишь при строго определенном соотношении компонентов и при определенном составе смеси различных видов крахмала (предложено уравнение для расчета состава смеси, учитывающее содержание амилозы, амилопектина и клейковины), а также при условии осторожного подсушивания сформованного полупродукта во избежание денатурации клейковины перед его тепловой обработкой.
ИСКУССТВЕННАЯ ЗЕРНИСТАЯ ИКРА
Задача получения искусственной зернистой икры была впервые сформулирована академиком А. Н. Несмеяновым. Выбор объекта определялся следующими соображениями. Натуральная икра — общепризнанный деликатесный продукт с высокой пищевой ценностью. Его успешная имитация способна поэтому наиболее
Способы получения ИПП
убедительным образом демонстрировать возможности нового направления в производстве пищи, т. е. возможность производства вкусных и привлекательных искусственных продуктов питания. Так можно преодолеть затруднения психологического порядка уже на начальной стадии организации производства и сбыта искусственных продуктов. Кроме того, поскольку натуральная зернистая икра — дорогостоящий и дефицитный продукт, ее производство может представить интерер уже при сравнительно небольших масштабах. Это обстоятельство, равно как и несомненная коммерческая привлекательность продукта для промышленности, должно было облегчить внедрение первого в пашей стране искусственного
продукта питания.
В результате исследований, начатых в 1963 г. под руководством А. Н. Несмеянова, в Институте элементоорганических соединений АН СССР были разработаны способы получения ряда вариантов искусственной зернистой икры [256—263]. Согласно этим способам, в искусственную зернистую икру можно перерабатывать различные белки, например белки молока, бобов сои, дрожжей, рыбы и т. п. В настоящее время производство продукта основано на переработке казеина. Первая установка для получения искусственной зернистой икры была создана в 1965 г. а Институте элементоорганических соединений АН СССР [264]. Выпускаемый промышленностью продукт носит название «икра белковая зердистая».
Для разработки процесса получения искусственной зернистой икры было необходимо решить задачи приготовления гранулированных студней определенного состава, формы, размера, с требуемым комплексом свойств, а также получения на гранулах студня оболочек, окрашивания этих оболочек в требуемый цвет, придания продукту необходимых органолептических свойств, и, наконец, объективной оценки последних [260—263,265—271].
Следует отметить, что до последнего времени для имитации икры осетровых и лососевых рыб в ряде стран используют специальным образом обработанную икру малоценных пород рыб,
например тресковых.
Единственный ранее известный способ получения искусственной зернистой икры был предложен Накамура [73]. По этому способу соус или измельченную массу пищевых продуктов, таких, как мясо, рыба, овощи, фрукты, водоросли и т. п., смешивают с водорастворимыми альгинатами и смесь вводят по каплям в раствор хлористого кальция. При этом получают гранулы студня альгината кальция, наполненные пищевыми веществами и имитирующие по внешнему виду зернистую икру. Использование альгината кальция в качестве студнеобразователя приводит, однако, к тому, что зерна продукта не изменяют механических свойств при повышении температуры, не плавятся и не растворяются
204 Глава четвертая
даже в кипящей воде. Естественно поэтому, что по вкусу продукт не мог близко имитировать натуральную икру.
При разработке способа основное внимание было поэтому уделено студням желатины, которые плавятся при температуре около 30°. Это позволяет обеспечить необходимые органолептические свойства искусственной икры, содержимое зерен которой плавится при температуре полости рта. Другая причина, определившая выбор желатины, заключается в возможности получения на поверхности студня тонких плотных оболочек продуктов дубления гранул растительными дубильными веществами. И, наконец, третья причина состоит в том, что студни желатины легко могут быть наполнены белками различного происхождения, без существенных изменений условий получения и объемных свойств студня (см. гл. II). Таким образом, использование желатины обеспечило универсальность по белку способа получения искусственной зернистой икры и возможность регулировать состав продукта в весьма широких пределах.
В основе способа получения искусственной зернистой икры лежат следующие известные приемы и физико-химические явления:
I. Получение гранулированных студней желатины, содержащих фармацевтические и пищевые вещества, путем введения по каплям нагретых концентрированных растворов желатины, содержащих эти вещества, в охлажденные органические растворители или масла. Этот прием был предложен в 1915 г. Ашкенази [272] и был затем усовершенствован и применен для капсулирования медицинских и пищевых препаратов [273—276], а также для получения имитаторов икры рыб, используемых в качестве корма и насадок для рыбной ловли [277, 278].
II. Явление образования пленок на поверхности студней желатины при их обработке раствором таннина, открытое Траубе в 1867 г. [279]. Образование пленки и ее уплотнение происходит вследствие прекращения диффузии таннидов в студень при возникновении на его поверхности плотного слоя продуктов дубления. Обзор литературы по этому вопросу приведен в [69].
III. Явление образования окрашенных комплексов ионов трехвалентного железа с фенольными соединениями [280, 281 ]. Это явление также известно очень давно и используется для получения чернил, а также для открытия фенольных соединений. Характер окраски зависит от природы фенольного соединения и аниона соли железа. Так, с хлорным железом гидролизуемые танниды дают сине-черное окрашивание [281].
Существо способа приготовления искусственной зернистой икры [256—263, 267—270] сводится к следующему. Для получения гранулированных студней раствор желатины, содержащей казеин, подают в виде капель в предварительно охлажденное пищевое
Способы получения ИПП 205
масло и выдерживают в нем до образования достаточно прочного студня. Полученные гранулы отделяют от масла, промывают водой и обрабатывают водными экстрактами чая для образования на гранулах оболочек. Окрашивание оболочек гранул в серо-чер-пый цвет для имитации цвета икры осетровых производят их обработкой водными растворами солей трехвалентного железа пищевых кислот. Для получения готового продукта к гранулированным студиям, покрытым окрашенными оболочками, добавляют попаренную соль, глютаминат натрия, растительное масло, рыбий жир и другие ароматические и вкусовые вещества, натуральные или синтетические. В качество натуральных ароматизирующих и вкусовых композиций могут служить, например, добавки 1—3% икры осетровых, диспергированной в растительном масле, сок сельди и т. п. Синтетические ароматизирующие композиции были разработаны в результате анализа состава летучих компонентов натуральной зернистой икры [262].
Приготовленная на основе полноценного белка и высококачественных растительных масел (кукурузное, хлопковое, подсолнечное) искусственная зернистая икра обладает высокой биологической ценностью (см. стр. 206). По содержанию витаминов она близка к натуральной икре осетровых [268].
Искусственная зернистая икра, полученная согласно описанному выше способу, характеризуется недостаточной температурной стабильностью. Это объясняется тем, что оболочка сама по себе не обладает достаточной прочностью и поэтому не способна обеспечить сохранение формы зерна после плавления студня (при температуре около 30°). Был разработан способ получения на поверхности зерен искусственной зернистой икры дополнительной оболочки, образованной альгинатами или пектинатами кальция и железа [270]. Так получают искусственную икру, зерна которой выдерживают нагревание при 40—45° в течение нескольких часов. Зерна продукта, производимого в настоящее время промышленностью, представляют собой жидкие при температуре полости рта капли, покрытые двумя оболочками. Одна из них обеспечивает окраску, другая — температурную стабильность гранул.
Еще одна физико-химическая задача, связанная с улучшением качества искусственной зернистой икры, касается необходимости изменения консистенции продукта «в массе». Зерна искусственной икры обладают низкой адгезией друг к другу, и получаемый таким образом продукт имеет рассыпчатую консистенцию, что, как показал опыт, не соответствует привычным вкусам потенциальных потребителей. Для уменьшения рассыпчатости искусственной икры предложено вводить в продукт эмульсию растительных масел в растворе казеина [270, 27I]. Был разработан способ получения концентрированных белково-масляных эмульсий, агрегативпо устойчивых в течение нескольких месяцев [271 ].
| Глава четвертая |
Таблица 48
Аминокислотный состав искусственной зернистой икры в сравнении с другими пищевыми продуктами
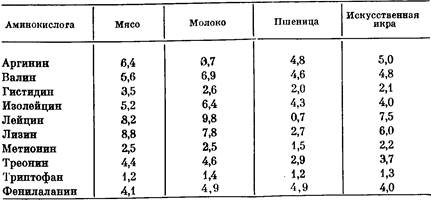
Дополнительная стабилизация эмульсий достигается за счет образования на поверхности капель масла защитного слоя студия альгината или пектината кальция, играющего роль структурно-механического барьера. Добавление белково-масляной эмульсии в количестве 3—12% улучшает консистенцию продукта «в массе». Указанные эмульсии могут иметь и самостоятельное значение, например для приготовления искусственных молочных продуктов.
Физико-химические процессы, протекающие на отдельных стадиях получения искусственной зернистой икры, и некоторые пути улучшения качества продукта рассмотрены в работах [261, 263, 267—269]. Ниже приведен состав искусственной зернистой икры (в %):

Способы полученияИПП 207
Состав искусственной икры может быть легко и в широких пределах изменен. На стадии кулинарной обработки к продукту могут быть добавлены отдельные аминокислоты, их смеси, а также водорастворимые белки, соли, водо- и жирорастворимые витамины (в исходный раствор для формования гранул рекомендуется вводить лишь высокомолекулярные водорастворимые вещества во избежание потерь пищевых веществ на последующих стадиях процесса за счет диффузии в водные среды). Способ, следовательно, позволяет производить продукты питания широкого назначения, в том числе диетические и лечебные. Искусственная икра используется так же, как и натуральная. Идентификация искусственной икры легко выполняется с помощью простой качественной реакции — добавление кислоты изменяет окраску продукта.
ДРУГИЕ ВИДЫ ИСКУССТВЕННЫХ ПРОДУКТОВ ПИТАНИЯ
В заключение рассмотрим искусственные продукты, имитирующие ягоды, фрукты, орехи, устриц и другие традиционные пищевые продукты. Хотя эти продукты не содержат или содержат незначительное количество белка и не служат решению проблемы белкового дефицита," они тем не менее демонстрируют возможности получения разнообразной привлекательной искусственной пищи и расширяют ее ассортимент.
Впервые способ получения искусственных вишен предложил Пешард [74]. Для их получения в раствор сахара вводят альги-нат натрия, красители и ароматизирующие вещества, после чего смесь подают в виде капель в коагуляционную ванну, содержащую раствор солей кальция. На каплях раствора быстро образуется оболочка студня альгината кальция. Ее толщина и структура зависят от продолжительности пребывания капель в коагуля-ционной ванне и се состава. Процесс диффузии ионов металла в капли раствора альгината натрия был подробно исследован в работах Тиле (см. гл. II). Этот прием был использован затем для получения гранулированных пищевых продуктов [283], имитаторов икры [73], круп и окрашенных пищевых частиц для декоративного оформления продуктов питания[284]. В отличие от искусственных круп при производстве ягод, не 'подвергающихся продолжительной варке, этот процесс оказался технологичным, так как в последнем случае достаточно получать на гранулах тонкие оболочки студня альгината кальция.
Производство таких вишен было впервые организовано в Англии около 15 лет назад. Они были хорошо приняты потребителем л затем получили распространение в Голландии, Франции,
208 Глава, четвертая
Италии, Швейцарии, Австрии и ряде других стран, где этот продукт заменяет до 25% натурального [75]. Преимущество искусственных ягод состоит в том, что они хорошо выдерживают нагрев и замораживание, однородны по весу и размерам. В США производство искусственных вишен было начато в 1962 г. Существо процесса осталось тем же. Сырьем служат вишневое пюре, кукурузная патока, сахар, альгинат натрия, краситель и искусственная отдушка. Продукт выпускают в виде гранул трех размеров и используют для декоративных целей, приготовления вы-печных изделий, в составе сухих смесей для тортов, кексов и т. п.
Способ получения гранулированного пищевого продукта, имитирующего плоды, предложил Стенли [285]. Сухие, измельченные в порошок фрукты, например яблоки или виноград, смешивают с сахаром, крахмалом или мукой (студнеобразователь — крахмал), добавляют глицерин, ароматизирующие вещества и небольшое количество воды (до 6%). Полученную вязкую массу гранулируют, например встряхиванием, и калибруют гранулы по размерам (от 1,6 до 12,5 мм). Продукт сохраняется при комнатной температуре в течение 6 мое. без каких-либо изменений. Его введение в тесто дает те же результаты, что и применение свежих плодов высокого качества. Аналогичным образом, с применением в качестве студнеобразователя крахмала, пектина или желатины, предложено получать гранулированные продукты для быстрого приготовления десертов и приправ [286]. Искусственный зеленый горошек получают, используя в качестве студнеобразователя крахмал, например в виде пшеничной муки [287].
Для получения искусственных орехов используют белковые волокна, которые готовят обычным способом мокрого прядения, нарезают (длина 12,5 мм), нагревают 20 мин. при 130° до сплав-ления и обезвоживания и пластифицируют, выдерживая 2 часа в четырехкратном (по весу) количестве глицерина. Избыток глицерина удаляют и к продукту добавляют отдушку, имитирующую запах грецкого ореха [288].
Способ получения искусственных устриц и других съедобных моллюсков был предложен в 19;')9 г. Денисенко [289]. Для этого в 2—4%-ный раствор альгината натрия добавляют 1,5—2,5% яичного альбумина, небольшое количество лимонной кислоты и эмульгируют 2—6% кокосового масла и рыбьего жира, а также ароматические композиции (например, бульон рыбы, крабов, экстракт огурцов и глютаминат натрия). Эмульсию помещают в форму, имеющую размер и форму устрицы, стенки которой пропитаны раствором соли кальция. Прием фиксации формы продукта, следовательно, аналогичен используемому для получения искусственных ягод, круп и икры.
Интересный способ получения искусственных фруктов и овощей, таких, например, как огурцы, арбуз, дыни и т. п., разрабо-
Способы полученияИПП 209
таи Щестняк [290] на основе работ Тиле по ионотропным студням (см. гл. II). В 0,5—5%-ный раствор альгината натрия вводят в количестве до 25% сахар, крахмал, жиры (кокосовое масло), возможно белки, а также другие кислые полисахариды (например, 2—5% пектина или 0,3—1% трагаканта) и в эту систему через полупроницаемую мембрану осуществляют диффузию ионов кальция из 1—12%-ного раствора соли кальция до образования студня альгината кальция с содержанием 0,61—0,67 з-экв кальция на молг. альгипата. Блок студня медленно замораживают до —10——28,5° и после оттаивания получают пищевой продукт пористой структуры с величиной нор до 3 мм, но преимущественно (более 50%) 0,1—07 мм. Продукт хорошо имитирует кусочки фруктов или овощей.
Можно сформулировать следующие общие требования к искусственным продуктам питания, обеспечивающие их широкое потребление. Прежде всего к их числу, очевидно, относится достаточно низкая стоимость. Последняя, однако, не должна ассоциироваться с недостаточно высоким качеством продукта и его назначением для питания населения с низким уровнем дохода. Искусственные продукты должны быть привлекательны для широких слоев населения, напоминать традиционные продукты по внешнему виду, цвету, вкусу и запаху, отвечать местным привычкам и требованиям к пище, а также быть пригодными для традиционных методов кулинарной обработки. Эти продукты должны характеризоваться высокой биологической ценностью и быть пригодными для ежедневного потребления в значительных количествах. Наконец, свойства искусственного продукта должны обеспечивать простоту его сбыта и удобство использования.
Хотя к настоящему времени разработаны способы получения многих форм искусственной пищи, однако развитие научных проблем, связанных с регулированием состава, потребительских и ор-ганолептичсских свойств искусственных продуктов питания, т. е. разработка научных вопросов, призванных обеспечивать выполнение перечисленных выше требований, только начаты.
Искусственные продукты питания в общем случае представляют собой студни с определенным составом, формой, структурой и комплексом механических и других физико-химических свойств, сообщающих этим продуктам требуемые технологические, орга-нолептические характеристики и биологическую ценность. Такие студни подвергают кулинарной обработке, сушке, консервированию, замораживанию и используют как аналоги или разбавители. Искусственные мясопродукты волокнистой и пористой структуры представляют собой анизотропные студни. Другие искусственные продукты питания — обычно изотропные студни, иногда
210 Глава четвертая
покрытые оболочками (икра, ягоды), наполненные эмульсиями, суспензиями (искусственные мясопродукты, имитирующие изделия из рубленого мяса), и т. д. Исключение составляют искусственные молочные и другие жидкие продукты. Однако и здесь студнеобразное состояние пищевых веществ играет важную роль в организации структурно-механического барьера на границе раздела фаз, стабилизирующего эмульсии.
В общем виде процесс получения искусственного продукта питания включает две стадии. На первой получают жидкую многокомпонентную систему необходимого состава. Эта система обычно представляет собой раствор, суспензию или эмульсию пищевых веществ и обязательно содержит студнеобразователь — компонент, обеспечивающий в определенных условиях (при изменении температуры, рН, ионного состава) перевод системы из жидкого состояния в твердое агрегатное. В качестве студнсобразоватслей используют белки, крахмал, кислые полисахариды. Их выбор в значительной мере определяет комплекс свойств продукта. На второй стадии процесса жидкую систему подвергают формованию и переводят в студнеобразное состояние, фиксируя таким образом форму изделия.
Очевидна, следовательно, ведущая для рассматриваемой проблемы роль двух физико-химических аспектов, анализируемых в гл. II. Первый связан с необходимостью получать и перерабатывать жидкие многокомпонентные водные системы пищевых веществ; второй — с получением многокомпонентных студней требуемого состава, свойств и макроструктуры. Для случая искусственных мясопродуктов волокнистой структуры этот второй аспект был четко сформулирован уже в 1958 г. Ансоном [5]. Оба эти аспекта проблемы, однако, очень слабо разработаны в научном отношении. Это справедливо даже для искусственных мясопродуктов волокнистой структуры как наиболее развитого в практическом плане направления.
ЛИТЕРАТУРА
1. П. Л. Ребинде.р.— В кн. «Коллоиды в пищевой промышленности», сб. 2. М., Пищепромизлат, 1949, с. 21.
2. П. А. Ребиндер, К. А. Поспелова.—В кн.: В. Клейтон. «Эмульсии,их теория и техническое применение». М., ИЛ, 1950, с. 11 [вступительная статья].
3. Я. И. Козин. Применение эмульсий в пищевой промышленности. М., Пищепромиадат, 1966, с. 224.
4. С. А. Матц. Структура и консистенция пищевых продуктов. М., Пище-промиздат, 1972, с. 101—115.
5. М. L. Anson.— In: «Processed plant protein foodstuffs», ch. 11. A. М. Alt-schul (Ed.). N.Y., Acad. Press, 1958, p. 277—289.
6. S. J. Circle, D. W. Johnson.—Ibid., ch. 15, p. 399—418.
7. Т. М. Bayless, N. S. Rosensweig.—l. Am. Mod. Ass., 197, N 12, 968 (1966).
Способы получения ИПП 211
8. /V. Kretvhmer.—In: «Food». San Francisco, W. H. Freeman со., 1973, p. 35—4,1
9. /. С. Jacqaemet.— Ind. alim. agric., 89, N 9-10, 1301 (1972). К). Л. А. Покровский.— Вопросы питания, 23, № I, 3 (1964).
11. А. А. Покровский.— ЖВХО,10, № 3, 247 (1965).
12. В. П. Ржехии— Там же, с. 295.
13. К. С. Петровский. Гигиена питания. М., «Медицина», 1975, гл. 3, с. 40 ел.
14. Я. Романская, В. Тылкин, Л. Зайцев.—Сов. торговля, № 2, 40 (1965).
15. Я. Я. Козин, H. И. Галицкая.— Вопросы питания,29, № 5, 13 (1970).
16. E. Mann.— Dairy Ind.,36, N 10, 557, 585 (1971).
17. A. A. Levinson, J. F. Lemancik.— J. Am. Oil Chcm. Soc.,51, N 1, 135 (1974).
18. S. Saperstein. Пат. США 3174866 (1965).
19. A. Decock— J. Am. Oil Chem. Soc.,51, N 1, 199 (1974).
20. S. G. Colon.— Food Proc. Ind., 40, N 481, 51, 53, 55 (1971).
21. D. L. Call— Meat, N 1 (1968).
22. Kao-Chun-Chin— Compt. rend.,224, 62 (1947).
23. £>. S. Bhatia, G. S. Bains.—Food Manuf.,31, N 9, 376, 390 (1956).
24. Tan Вое Han. Technology of soymilk and some derivatives. Wageningen, 1958.
25. A. Smith, T. Watanabe.— Food Technol., 14, N 7, 332 (1960).
26. А. К. Smith, S. J. Circle.— In: «Soybeans: Chemistry and technology», v. 1. Ed. A. K. Smith, S. J. Circle. Westport, Connecticut, AVI. Publ. со., 1972, ch. 1, p. 1—27, ch. 10, p. 356—362.
27. T. Watanabe— J. Аш. Oil Chem. Soc.,51, N 1, 111 (1974).
28. T. Watanabe, E. Ebine, М. Okada.— In: «New protein foods», ch, 9 A. М. Altschul (Ed.). N. Y, Acad. Press, 1974, p. 415—450.
29. /. Mauron— Bibl. Nutr. Diet.,16, 169 (1971);21, 147 (1975).
30. G. K. Okumara, 1. E. WUkinson. Пат. США 3399997 (1968); 3490914 (1970). :il. S. Kakuchi— J. Am. Oil Chem. Soc.,51, N 1, 189 (1974).
32. Л. Л. Levinson, ]. F. Lemancik.— Ibid., p. 135.
33. /. T. Lawthon e. a.- Cereal Sci. Today, 17, N 9, 240 (1972).
34. S. J. Circle.—!. Am. Oil Chem. Soc.,51, N 1, 198 (1974). 3;i. W. S. Claus.— Ibid., p. 197.
36. Л W. Mansvell—Ibid., p. 202.
37. E. Kolb.— Ibid., p. 200.
38. Technical data: Supro-6; Snpro-610; Saint Louis, Missouri, USA («Ralston purina со.»).
39. Technical data: Soyamel, Banana beveridge. Infra-soy, Cheze-o-soy. Wor-thington, Ohio, USA («Worthington foods inc.»).
40. J. Bakoski/, Ir. Soy proteins - t.lieir functions in food applications. Central soya со., 1*168.
41. D. С. Cngan. Seminar on U'xtiircd vegetable protein, its past, present future. N.Y., 1973. Miles Lab. Elkhart,Indiana, 1973.
42. E. A. Peilegrini.—Rev. med. vet.,54, N 2, 105 (1973).
43. М. R. Chandarasekhara, В. Я. Ramanna, К. S. Yagamnalh, P K. Ramana-than.— Food Technol.,25, N 6, 32 (1971).
44. М. A. Krishnasway, Y. D. Datel, S. Dhanaraj, V. S. Govindrajan — J Food Sci. Technol., 8, N 2, 41 (1971).
45. Л. М. Altschul— Chem. Eng. News, 47, N 49, 68 (1969).
46. S. M. Weisberg.— J. Am. Oil Chem. Soc., 51, N 1 204 (1974)
47. Chem. Eng. News, 48, N 33, 36 (1970).
48. A. N. Meiss, S. M. Cantor.— J. Am. Oil Chem. Soc., 48, N 9 473 (1971)
49. /. Lefebvre.— Cah. nutr. diet.,5, N 4, 46 (1971).
ЗД. D. B. Walker с.а.— Food Technol.,25, N 8, 54 (1971)
51. Я. L. Kellur.— J. Am. Oil Chem. Soc., 48, N 9, 481 (1971).
Глава четвертая
52. С. Л'. Bookwalter, П. A. Mosser, W. T. Kwoiek e.a.—L Food Sci.,36, N 5, 732 (1971). /
53. G. N. Bookwalter, H. A. Moser, L. T. Black, E. L. Griffin, ]r.-+- J. Food Sci., 36, N5, 737 (1971). /
54. F. R. Senti.—]. Am. Oil Chem. Soc,51, N 1, 138 (1974).
55. Д. /, Dimler- J. Am. Oil Chem. Soc., 48, N 8, 400 (1971).
56. Chem. Hundsch, N 7, 207 (1965).
57. Autorenkollektiv. Ernahrungs- und Lebensmittellohre. Leipzig, VEB Fach-buchverlag, 1966, S. 244.
58. II. А. Манкеева. Повышение биологической ценности макаронных изделий. М., Пищопромиздат, 1973.
59. E. П. Козьмина— ЖВХО,10, № 3, 307 (1965).
60. С. Н. Лопатинский, А. А. Покровский.— Хранение и переработка зерна, № 8, 8 (1966).
61. H. Mitsuda, К. Yasumofo.— In: «New protein foods», ch. 3. A. М. Altschul (Ed.). New York — London, Acad. Press, 1974, p. 121—156.
62. С. Н. Лопатинский.— Мукомольно-элеваторная пром., № 9, 33 (1966).
63. С. В. Allie, F. Little. Пат. США 2991181 (1961).
64. Л. Танинака, М. Хорн. Пат. Японии 8387 (1959).
65. S. М. Cantor, 0. Hills, P. Faller e. а. Пат. США 2890117 (1959).
66. L. J. Lee. Пат. США 3113868 (1963).
67. К. Ому pa, М. Аодзима. Пат. Японии 3626 (1961).
68. Н. Кацуя, Т. Сагавара, Р. Такахаси и др. Пат. Японии 29178 (1971).
69. В. А. Ершова, E. E. Браудо, В. Б. Толстогузов и др.— Труды МИНХ им. Г. В. Плеханова, вып. 58, 125 (1968).
70. E. Козьмина, Э. Бондарева, Г. Слонимский, В. Толстогузов.— Мукомольно-элеваторная пром., № 1, 29 (1969).
71. Г. Л. Слонимский, E. E. Браудо, И. Д. Ертанов и др.— Вопросы питания, 29, № 6, 25 (1970).
72. E. П. Козьмина, Э. С. Бондарева, В. Б. Толстогузов.—Хранение и переработка зерна, вып. 7, 23 (1968).
73. X. Накамура. Пат. Японии 15088 (1961).
74. W. J. S. Peschardt. Пат. США 2403547 (1946).
75. М. Glicksman.— Adv. Food Res.,11, 109 (1962); Food Process.,22, 50 (1961).
76. К. А. Степчков, Е. Н. Волков. Производство и использование белковых гидролизатов в пищевой промышленности. М., Пищепромиздат, 1964.
77. К. А. Степчков. Синтетические белковые продукты и их использование в пищевой промышленности. М., Пищепромиздит, 1967.
78. В. Н. Козлов.— Хлебопек, п копдитерск. пром., № 3, 25 (1969).
79. E. F. Glabe, P. W. Anderson, P. F. Goldman— Cereal Sci. Today,12, N 12, 510, 532 (1967).
80. T. J. Jakubczyk, П. Piesiewicz.— Prz. zboz.-mlyn.,13, N 3, 78 (1969).
81. R. L. Ke.llor— J. Am. Oil Chem. Soc.,51, N 1, 77 (1974).
82. Л. S. Clausi— Food Technol.,25, N 8, 63 (1971).
83. G. G. Graham, J. M. Baerti— J. Am. Oil Chem. Soc.,51, N 1, 152 (1974).
84. N. R. Lockmiller.— Cereal Sci. Today, 18, N 3, 77 (1973).
85. /. D. DeRuiter.— J. Am. Oil Chem. Soc.,51, N 1, 187 (1974).
86. H. U. Zaenecke, U. Pefzold— Backer und Koditor, 27, N 10, 292 (1973).
87. F. E. Ho ran— Cereal Sci. Today, 18, N 1, 11 (1973).
88. A. A. Levinson, J. F. Lemancik.— J. Am. Oil Chem. Soc.,51, 135 (1974).
89. N. S. Katz, D. J. Donovan. Пат. США 3138462 (1964).
90. К. Maku. Пат. Японии 14481 (1960).
01. Я. Накаока, С. Мицунага, С. Араи. Пат. Японии 15418 (1960).
92. L. S. Lee. Пат. СШЛ 3113869 (1963).
i»:i. X. Огава. Пат. Японии 4786 (1959).
91. Т. Мори. Пат. Японии 17976 (1969); 16768 (1970).
Способы полученияИПП 213
95. Т. W. Ohih, T. N. Kiat. Пат. Англии 1097795 (1968).
96. H. W. Bakkeren. Пат. Франции 1567617 (1969).
97. R. D. Retnhart, R. W. Stephensen. Пат. США 3458321 (1969).
98. W. B. Toistogasow, /u. /. Tschimtrow, E. E. Braudo e. a— Nahrung,19,N 1, 33 (1*175).
99. W. B. Tolsogusow, Ju. I. Tschimirow, B. P. Suchanow e. a.—Nahrung,20,N3,329.(1976).
100. E. Козьмина, Ю. Чимиров, Д. Изюмов, В. Толстогузов.— Обществ, питание, № 4, 48 (1973).
101. Ю. И. Чимирлв, Д. Б. Изюмов, В. Б. Толстогузов.—Труды МИНХ им. Г. В. Плеханова, № 2, 83 (1974).
102. W. B. Tolstogasow, E. E. Braudo, E. S. Weinerman.— Nahrung,19, N 9/10, 973 (1975).
103. A. D. Odell. Meat analogues from modified vegetable tissues, ABS-71-35.— Proc. Int. Conf. Soybean Protein Foods, USA, 17—19 Oct. 1966. Peoria, Illinois, 1966.
104. W. W. Thulln— Canner/Packer,134, N 9, 2 (1965).
105. W. W. thulin, S. Kv.ra.moto— Food Technol., 21, N 2, 64 (1967).
106. R. E. Martin, D. V. Leclair.— Food Eng.,39, N 4, 66 (1967).
107. R. Bressani, F. Viteri, L. G. Elias e.a.—f. Nutr.,93, N 3, 349 (1967).
108. R. Hamm— Fleischwirtschaft, 48, N 5, 597 (1968).
109. II. Linke— Fleischwirtschaft, 49, N 4, 469 (1969),
110. A. Gordon,—Food Proc. and Market, N 7, 267 (1969).
111. D. С. Wosje, J. Milk— Food Technol.,33, N 9, 405 (1970).
112. Meat Manag. Aug., 1970, p. 94.
113. M. R. Ashton, С. S. Burke, A. W. Helmes— Brit. Food Manuf. Ind. Res. Assoc. Sci. and Technol. Surveys, N 62, 1 (1970).
114. J. Rakosky, Ir.—J. Agr. Food Chem., 18, N 6, 1005 (1970).
115. /. Lefebvre— Cah. nutr. diet.,5, N 4, 46 (1971).
116. M. D. Wilding—J. Am. Oil Chem. Soc., 48, N 9, 489 (1971).
117. A. B. Childers— J. Milk and Food Technol.,35, N 10, 604 (1972).
118. N. B. Lockmiller— Food Technol., 26, 56 (1972).
119. Д. F. Robinson.— Ibid., p. 59.
120. M. Gutcho. Textured foods and allied products. N. Y. Noyes data corp., 1973; Food Technol., 27, N 8, 79 (1973).
121. D. Rosenfield, W. E. Hartman.— J. Am. Oil Cheni. Soc.,51, N 1, 91 (1974).
122. К. Yasuda— Ibid., p. 195.
123. К. М. Wolfotd— Ibid., p. 131.
124. E. H. M. Greaell— Ibid., p. 98.
125. F. E. IIoran— Ibid., p. 67.
126. F. E. Horan.—In: «New protein foods»,ch. 8. A.M. Altschul (Ed.). New York—London, Acad. Press, 1974, p. 366—411.
127. С. L. Wrenshall. Пат. СП1Л 2560621 (1951).
128. M. L. Anson, M. Pader. Пат. США 2802737 (1957).
129. M. L. Anson, M. Pader. Пат. США 2802738 (1957).
130. M. L. Anson, M. Pader. Пат. США 2813024 (1957).
131. M. Pader, H. D. Hamilton p.. а. Пат. США 2874049 (1959)
132. /. P. Durst.Пат. США 3108873 (1963).
133. К. Кинеи, Д. Кавпч.Пит. Японии 15251 (1962).
134. А. Фудзита, Ю. Фудзита. Пат. Японии 1780 (1960).
135. Токио униоп когио ко. Пат. Японии 20190 (1964).
136. Т. Ki/рати. Пат. Японии 10841 (1963).
137. W. E. IIartman. Пат. США 3290152 (1965).
138. General Mills. Пат. Голландии 6612299 (1967).
139. M. L. Anson, M. Pader. Пат. США 2813794 (1957).
140. М. Накамура, И. Татида, X. Иидзума. Пат. Японии 6565 (1963).
Глава четвертая
141. 3. Кенде, Ф. Кеттинг—XV Международный конгресс по Молочному делу. М., Пищепромиздат, 1961, с. 246—248. /
142. Z. Kende, F. Retting. Пат. ФРГ 1069458 (1959). /
143. S. S. Frank, S. J. Circle— Food Technol.,13, N 6, 307 (1959). /
144. E. J. Rivoche. Пат. США 2786763 (1957). /
145. E. J. Rivoche. Пат. США 2786764 (1957); пат. ФРГ 1197738 М966).
146. J. Green, E. J. Schuller, J. A. Rickert, B. Borders. Пат. США'2992925 (1961).
147. F. Epstein. Пат. США 2876115 (1959). /
148. G. Maiichand. Пат. Франции 1421416 (1965).
149. H. P. Landgreen— Adv. Protein Chem.,5, 305 (1949).
150. 3. А. Роговин. Основы химии и технологии производства химических волокон. М.— Л., «Химия», 1964.
151. Р. У. Монкрифф. Химические волокна. М., «Легкая индустрия», 1964, с. 237-268.
152. G. Champetier. Lee macropolymeres et leurs application: Textiles naturels, artificiels et synthetiques. Les cours de Sorbonne, CDU, 1956, p. 116.
153. A. Ferretti— Ind. Textile, 54, 446 (1937).
154. A. Ferretti—Textile Manuf.,66, 235 (1940).
155. R. A. Boyer, J. Crapi, W. T. Atkinson («Ford motor со.»). Пат. США 2377853 (1945); Д. A. Boyer, W. T. Atkinson, C. F. Robinette («Ford motor со.»). Пат. США 2377854 (1945).
156. Д. А. Boyer— Ind. Eng. Chem.,32, N 12, 1549 (1940).
157. Л. А. Boyer. Пат. США 2682466 (1954); пат. Англии 699692 (1953); пат. Канады 512626 (1955).
158. С. П. Папков. Докт. дисс. М., НИФХИ им. Л. Я. Карпова, 1966.
159. С. П. Папков. Физико-химические основы переработки растворов полимеров. М., «Химия», 1971.
160. С. П. Папков. Студнеобразное состояние полимеров. М., «Химия», 1974.
161. Л. А. Boyer («Swift and со.»). Пат. США 2730447 (1956).
162. Л. А. Boyer, H. E. Seawert («Swift and со.»). Пат. США 2730448 (1956).
163. Л. А. Boyer, A. A. Schalz, E. A. Schatzman («Ralston purina со.»). Пат. Англии 958873 (1964); пат. Бельгии 627598 (1963); пат. Канады 727064 (1965).
164. Л. К. Dadman («Swift and со.»). Пат. США 2785069 (1957); пат. Канады 534716 (1957).
165. М .L. Anson («Lever brothers со.»). Пат. США 2833651 (1958).
166. /. ]. Broderick, L. L. Linteris. Пат. США 2955041 (1960).
167. L. J. Haber, S. Kuramoto, F. Smith («General mills inc.»). Пат. США 3157516 (1964); пат. Голландии 6607279 (1966).
168. Т. М. Hoersch («Swift and со.»). Пат. США 3316099 (1967).
169. Intern. Flavors and Fragrances. Пат. Англии 1069104 (1967).
170. Л. S. Kiratsous.— Cereal Sci. Today,14, N 4, 147 (1969).
171. Л. Prof fit,— Franco ct parfums,9, N 47, 39 (1966).
172. H. M. Cole— Baker's Dig.,34, N 6, 46, 70 (1960).
173. W. J. Downey, R. 1. Eiserle.— J. Agr. Food Chem., 18, N 6, 938 (1970).
174. /. G. Keppler— Ibid., p. 988.
175. Я. G. Maier— Angew. Chem., 82, N 24. 965 (1970); 83, N 22, 919 (1971).
176. S. Kuramoto, R. W. Westeen, J. L. Keen («General mills»). Пат. США 3177079 (1965); пат. Англии 979695 (1965); пат. Бельгии 635727 (1963).
177. Л. W. Westeen, S. Kuramoto ^«General mills»). Пат. США 3118959 (1964);
пат. Англии 987348 (1965).
178. E. Green, R. W. Graham, H. S. Gardner, A. W. Holmes («Lever brothers со.»). Пат. Англии 742580 (1955); пат. США 2958606 (1960).
179. E. East, E. Green («Lover brothers со.»). Пат. Англии 757215 (1956)- пат США 2809090 (1957).
180. Т. Окухаси, Я, Ватапаби, А. Симидзу. Пат. Японии 4144 (1971).
Способы полученияИПП
181. С. Giddey («F. P. research»). Пат. США 2947644 (1960); пат. Англии
886486 1962).
182. Л. С. Derhaine, R. W. Caltaghan («General mills»). Пат. США 3269841 (1966); пат. Англии 1047965 (1966).
183. Л. С. Dechaine, R. W. Callaghan. Пат. США 3314356 (1967).
184. A. S. Szczevniack, E. Engel.Пат. США 2952543 (1960).
185. ;V. H. JshUr, V. Cottage, R. V. MacAllister e. a. («General foods corp.»). Пат. США 3093483 (1963).
186. P. D. Haas, В. Adair («General mills»). Пат. Голландии 6609102 (1967);
пат. Франщп1( 1484991 (1967).
187. W. T. Atkinson («Archer daniels midland со.»). Пат. США 3455697 (1969).
188. L. F. Elmquist («General mills»). Пат. США 3175909 (1965).
189. Я. /. Dif.lsrh, Л. Kruger, A. Ciotto (,«Ur. A. Wander AG»). Пат. Швейцарии 422498 (1967); пат. Франции 1530427 (1968).
190. К. Мимото, Т. Сакчта, М. Эбчдзава («Ниссиц сайю кабусики кайся»). Пат. Японии 3101 (1971).
191. М. L. Anson, M. Pader («Lever brothers со.»). Пат. США 2830902 (1958);
пат. ФРГ 951970 (1956); пат. Англии 746859 (1956); пат. Бельгии 522160 (1955).
192. M. L. Anson, M. Pader («Lever brothers со.»). Пат. США 2879163 (1959).
193. H. Baumgartner.— Fleischermeister, 9, N 9, 7 (1955).
194. /. /. Kelley, P. Pressey— Cereal Chem.,43, N 2, 195 (1966).
195. C. Giddey.— Cereal Sci. Today,10, N 4, 56 (1965).
196. F. Haang, Cho Kyan Rha.— Biotechnol. and Bioeng., 14, 1047 (1972).
197. M. L. Anson, M. Pader («Lever brothers со.»). Пат. США 2813025 (1957).
198. N. A. Kjelson («General mills»). Пат. США 3343963 (1967); пат. Бельгии 634140 (1963).
199. N. A. Kjelson, 1. A. Page («General mills»). Пат. США 3210195 (1965).
200. General mills inc. Пат. Англии 9772338 (1964).
201. W. E. Ha.rtn.an («Wortington foods»). Пат. Франции 1400678 (1965); пат. США 3320070 (1967).
202. С. Giddey («F. P. research ltd.»). Пат. Англии 886487 (1962); пат. США 2952542 (1960).
203. /. L. Boyle («Alginate industries»). Пат. Англии 1118730 (1968).
204. /. Л. Page, W. G. Bauer («General mills»). Пат. США 3403027 (1968); пат. Англии 1152327 (1969).
205. X. Миятатэ. Пат. Японии 24574 (1971).
206. General mills. Пат. Голландии 6612299 (1965).
207. Unilever. Пат. Голландии 6715346 (1968).
208. Л. }. Coleman, N. S. Creswick («Unilever ltd.»). Пат. США 3253931 (1966);
пат. Англии 922759 (1955).
209. N. S. Creswick, К. W. Henderson («Lever brothers со.»). Пат. Англии 1173976 (1970).
210. G. T. Carlin («Swift and со.»). Пат. США 3100710 (1963).
211. Л. Mainhardt, A. T. Biehl («The union stock jard and transit Co.») Пат. США 3163541 (1964).
212. Ю. Синэмчти, X. Хара, Л. Окцра («Нпссап сэйю кабусики кайся»). Пат. Японии 18578 (1971).
213. /. Л Russoff, W. J. Ohan, C. J. Long ('«General foods corp.»). Пат США 3047395 (1962); пат. Англии 883976 (1962).
214. Л. V, MacAllister, T. P. Funucane («General foods corp.»). Пат. США 3102031 (1963).
215. N. A. Kjelson («General mills»). Пат. США 3197310 (1965).
216. И. Хасзбэ, К. Минагава («Синсип секуро коге кабусики кайся») Пат Японии 1963 (1965).
217. Т. Нагасава, М. Томита, Т. Обаяши и др. («Морпнага милк индастри ко. лтд.»). Пат. Японии 93762 (1968); пат. США 3674500 (1972).
Глава четвертая
/
218. A. F. Arnold, С. G. Hartland, A. Sjedsma («Archer daniels mi(fland со.»). Пат. Англии 1049848 (1966). '
219. Ralston Purina со. Пат. Англии 1105904 (1968). /
220. S. L. Jenkins («Ralston purina со.»). Пат. Англии 1174906/(1969); пат. Франции 1505075 (1967). /
221. W. T. Atkinson («Archer daniels midland со.»). Пат. Голландии 6506477
(1965); пат. США 3488770 (1970). /
222. W. T. Atkinson («Archer daniels midland со.»). Пат. Франции 1444264
(1966). /
223. H. A. Huffman. Пат. США 3485636 (1970). )
224.В, Б. Толстогузов, А. И. Мжельский, В. Т. Чеховская., H. В. Михеева. Авт. свид. СССР 301014, 301939 (1970); пат. Франции 2090572 (1972);
пат. Англии 1310005 (1972); пат. Канады 924175 (1973).
225. В. Б. Толстогузов, А. И. Мжельский, В. А. Ершена и др. Авт. свид. 301015 (1970); пат. Франции 2090571 (1972); пат. Англии 1311581 (1973);
пат. Канады 923752 (1973).
226. W. B. Tolstogasow.—Nahrung, 18, N 5, 523 (1974).
227. W. B. Tolstogiisow, E. E. Braudo, E. S. Wainerman— Nahrung,19, N 9/10, 973 (1975).
228. Д. A. Boyer, A. A. Schalz («Ralston purina со.»). Пат. Канады 867687
(1970).
229. D. B. Walker, F. E. Horan, R. E. Burket.— Food Tochnol.,25, N 8, 54
(1971).
230. /. A. A. Maga— J. Agr. Food Chem.,21, N 5, 864 (1973).
231. /. Mauron.—l. Int. VitaminoL, 40, N 2, 209 (1970).
232. W. E. Moore, I. L. Carter— J. Texture Studies,5, 77 (1974).
233. /. H. Qvist, E. С. F. Sydow.—L Agric. Food Chem., 22, N 6, 1077 (1974).
234. /. Adrian.—World Rev. Nutr. Diet, 19, 71 (1974).
235. Я. G. Maier— Naturwis.,55, N 4, 180 (1968).
236. Я. G. Maier.—]. Chromat., 45, N 1, 57 (1969).
237. Я. G. Maier— Z. anal. Chem.,250, N 2, 115 (1970).
238. K. L. Franzen, J. E. Kinsella— J. Agr. Food Chem., 22, N 4, 675 (1974).
239. Technical data. Textured simulated miats («Wortington foods»).
240. Miles laboratories, Temptein, The spun textured protein 1972, How to reduce food costs and boost nutrition in school lunch programs.
241. Loma linda foods. Vegetable protein recipes for every occasion.. Mount Vernon, Ohio, USA.
242. Far-mar-co., Foods div. techn. bull. Textured vegetable protein products, Product information shoot Ultra-soy. Hutchinson, Kansas 67501, USA.
243. Swift edible oil со. Div. Swift and со., Chicago, Illinois 60604, Food ingredient products texgran. FID-T-100-73.
244. Cargill, Processing and refining div., Soy special products for the food industry — textratein, 10-1-1971.
245. Halston purina со.. Food proteins. Summary product specifications and applications, Purina protein Europe, 1050 — Brussels, Belgium
246. M. Zobel— Nahrung,14, N 6, 503 (1970).
247. /. L. Rossen, R. С. Miller— Food Techn., 27, N 8, 46 (1973).
248. E. ]. Riuoche. Пат. США 2791508 (1957); пат. ФРГ 1197738 (1966).
249. E. J. Rivoche. Пат. США 3114639 (1963).
250. B. R. Толстогузов, Д. Б. Изюмов. Авт. свид. 296554 (1969); Бюлл. изобр., № 9 (1971); Изобретатель и рационализатор, Х° 11, 7 (1971).
251. Д. Б. Изюмов, Ю. И. Чимиров, В. В. Толстогузов.— И.чв. вузов Пищевая технология, № 1, 40 (1973).
252. D.R.A. Gerkens. Пат. США 3076711 (1963).
253. W. W. C amp field. Пат. США 3150978 (1964).
254. /. Cooper, D. Melnik. Пат. США 3589914 (1971).
255. /'. Markakis, T. M. Freeman, W. H. Harte. Пат. США 3027258 (1962)
Способы полученияИПП 217
256. А. H. Несмеянов, Г. Д. Слонимский, E. К. Браудо, В. Б. Толстогузов. Авт. CBitfl. 218652 (1964); Бюлл. изобр.. Я? 9 (1973).
257. А. Я. Несмеянов, С. В. Рогожин, Г. Л. Слонимский, В. Б. Толстогузов, В. А. Ершова. Авт. свид. 228521 (1965); Бюлл. изобр., № 31 (1968); пат. США 3589010 (1971); пат. Англии 1167507 (1969); 1300721 (1972); пат. ФРГ 1692683 (1971); 19657443 (1971).
258. Г. Л. Слонимский, С. В. Рогожин, В. Б. Толстогузов, В. А. Ершова. Авт. свид. 231314 Y1965); Бюлл. изобр., № 35 (1968).
259. Г. Л. Слонимский, M. И. Кабачнчк, E. E. Браудо, В. Б. Толстогузов. Авт. свид. 282918 (1965); Бюлл. изобр., № 30 (1970).
260. С. В. Рогожин. Докт. дисс. M., ИОХАН СССР, 1971.
261. E. E. Браудо. Канд. дисс. M., ИНЭОСАН СССР, 1971.
262. Р. В. Головня. Докт. дисс. M., ИНЭОС АН СССР, 1973.
263. В. Б. Толстогузов. Докт. дисс. M., ИНЭОС АН СССР, 1975.
264. А. H. Несмеянов, С. В. Рогожин, Г. Л. Слонимский и др. Авт. свид. 276725 (1966); Бюлл. изобр., № 23 (1970); пат. США 3499379 (1970); пат. Англии 1190407 (1970); пат. ФРГ 1692684 (1971).
265. С. В. Рогожин, E. E. Браудо, В. В. Толстогузов, В. И. Мисюрев. Авт. свид. 435489 (1972); Бюлл. изобр., № 25 (1974).
266. С. В. Рогожин, В. И. Мисюрев, В. Б. Толстогузов. Авт. свид. 448383 (1973);
Бюлл. изобр., № 40 (1974).
267. В. Б. Толстогузов, В. А. Ершова, E. E. Браудо.— Журн. прикл. химии, 46,2534 (1973).
268. S. W. Rogoshin, W. B. Tolstogusow.— Nahrung,19, N 1, 5 (1975).
269. S. W. Rogoshin, W. B. Tolstogusow, A. N. Nesme/anow.—Ibid., p. 987.
270. A. H. Несмеянов, С. В. Рогожин, В. Б. Толстогузов и др. Авт. свид. 552738 (1972).
271. В. Б. Толстогузов, E. E. Браудо, Я. В. Михеева. Авт. свпд. 303819 (1969);
Бюлл. изобр., № 29 (1971).
272. Р. Askenasy. Пат. США 1201133 (1916).
273. С. E. Fischer, fr., C. H. Wilson. Пат. Канады 649041 (1962).
274. Л С. Hecker, 0. D. Hawks. Пат. США 3137630 (1964); пат. Англии 1007465 (1965).
275. A. Koff, P. F. Widmer. Пат. США 3143475 (1964).
276. F. H off man. Пат. Голландии 6404962 (1965).
277. W. R. H. Brener. Пат. США 2827376 (1955).
278. Д. Е. Humphreys. Пат. США 3421899 (1969).
279. M. Traube.— Arch. anat. physiol. und wiss. mod., 1867, S. 87; цит. по кн. А. Я. Михайлова. Коллоидная химия таниидов. M.—Л., Гизлегпромиз-дат, 1935, с. 258.
280. А. H. Михайлов. Коллоидная химия таинидов. M.— Л., Гизлегпромиз-дат, 1935, с. 257.
281. К. Я. Gustavson. The chemistry of tanning processed N Y.. Acad Press 1956.
282. W. Bock, D. Lange, K. Taafel. Пат. ГДР 36655 (1965).
283. DCA food inds inc., Пат. Франции 2052785 (1971).
284. G. E. Livingstoa. Пат. США 3111411 (1963).
285. В. Stanley. Пат. США 3105766, 3102820 (1963).
286. A. Schapiro. Пат. США 3100909 (1965); пат. Франции 1347910 (1963)
287. И. Кавагути. Пат. Японии 22609 (1961).
288. Я. Andregg («Swift and со.»). Пат. США 2776212 (1957)
289. S. Denissenko. Пат. Франции 1229528 (1960).
290. A. S. Szcsesniak («General foods Corp.»). Пат. Англии 1099820 (1968).
| ГЛАВА ПЯТАЯ ИГ |
ИСКУССТВЕННЫЕ ПРОДУКТЫ ПИТАНИЯ
НОВАЯ ОБЛАСТЬ / КРУПНОТОННАЖНОГО ПРОИЗВОДСТВА
ПОТРЕБЛЕНИЕ ИСКУССТВЕННЫХ ПРОДУКТОВ ПИТАНИЯ
Становление любой крупнотоннажной отрасли производства обычно связано с необходимостью развития уровня знаний как в данной, так и многочисленных смежных и вновь возникающих областях науки и техники, а кроме того, развитием смежных отраслей производства. Это тем более справедливо в рассматриваемом случае, так как речь идет о новом направлении в производстве пищевых продуктов массового потребления. Помимо широких медико-биологических исследований и официального одобрения ответственными медицинскими инстанциями, организация производства искусственной пищи возможна при условии решения ряда сложных вопросов, определяющих масштабы их потребления, в том числе научно-технических, экономических, организационных, а также вопросов, связанных с психологией потребителя. Очевидна необходимость разработки методов контроля качества, идентификации и стандартов на эти продукты, методов рекламы, наименования и описания продуктов, тщательное изучение рынка и требований потенциальных потребителей, а кроме того, обучения и подготовки персонала, занятого их производством, продажей, использованием, а также информацией потребителя об особенностях состава, технологических свойствах и преимуществах новых пищевых продуктов.
В США в 1962 г. было официально разрешено добавлять белки сои в мясопродукты из рубленого мяса, в 1966 г.— использовать соевые волокна в пищу, в 1968 г.—использовать искусственные продукты — аналоги говядины, индюшатины, ветчины, мяса цыплят и т. п., а также искусственные мясопродукты — разбавители. В последующие годы в США было также разрешено потребление искусственных пищевых продуктов на основе белков семян хлопчатника, подсолнечника и арахиса [1—З]. Использование разбавителей па основе белка бобов сои разрешено в Англии, Франции, Швеции и ФРГ [4—7]. По стандарту Министерства сельского хозяйства США изоляты соевого белка должны содержать 0,1% двуокиси титана. Эта добавка позволяет идентифицировать искусственные мясопродукты, а также определять количество белка сои в традиционных мясопродуктах [8, 9]. Добавки
ИПП — новая область крупнотоннажного производства 219
двуокиси титана разрешены не во всех странах, и разрабатываются другие Методы контроля содержания искусственных мясопродуктов-разбавителей в натуральных мясопродуктах [6, 7, 10, II]. С этой целЫо используются иммунологические, электрофоретиче-ские и другие методы анализа.
Во Франции было использовано в 1972 г. около 2000 т соевых разбавителей [5]. В Швеции уже в 1968 г. были снижены пошлины на обезжиренную соевую муку и концентраты белка бобов сои, а также организована широкая реклама продуктов на основе сои [б]. Эти продукты начали в последнее время производиться и потребляться во все возрастающих масштабах в Англии, ФРГ и других высокоразвитых странах Европы. Наибольшие успехи достигнуты в США. Здесь начиная с середины 60-х годов была организована продажа опытных партий искусственных мясопродуктов, проведены многочисленные апробации и широкие исследования приемлемости этих искусственных продуктов для различных групп населения, разработаны стандарты на искусственные мясопродукты, правила этикетирования и методы рекламы [12—22].
Практика продажи искусственных продуктов питания показывает, что их широкое потребление, особенно на начальном этапе, тормозится рядом причин. К ним прежде всего относятся причины психологического порядка. Сложившиеся привычки большинства населения развитых стран к потреблению мясных и других высококачественных животных продуктов, вкусовые достоинства которых наиболее высоко оцениваются, привела к непризнанию первого поколения новых продуктов, лишь весьма отдаленно напоминавших мясные. Учитывая сложность и неблагодарность задачи изменения привычек потребителя, внимание было направлено на совершенствование качества и, в первую очередь, вкусовых достоинств искусственных продуктов питания, а также на их использование в качестве разбавителей натуральных продуктов. В обоих этих направлениях достигнуты положительные результаты. Помимо этого усилия были сосредоточены па разъяснении массовому потребителю природы новых продуктов, их высокого качества и диетических достоинств. Важно отметить, что реакция потребителя существенным образом зависит от уровня его информированности о составе продукта, а также от того, знает ли он о том, что потребляет искусственный продукт питания. Показано, что если не предупреждать потребителя, то большинство предпочитает полностью мясным рубленым продуктам мясопродукты с разбавителем. Аналогичная картина наблюдалась и при многочисленных апробациях искусственной зернистой икры. Этот продукт хорошо принят.
Другая причина, ограничившая потребление в США искусственных мясопродуктов, заключалась в том, что потребитель, как правило, не в состоянии дать верную оценку их действительной
220 Глава пятая
стоимости. Ситуация здесь не столь проста. При сравнительно близких розничных ценах на искусственные мясопродукты-аналоги и на натуральное мясо в первом случае речь идет (» готовых к употреблению изделиях, тогда как натуральное мясо поступает в продажу в сыром виде со значительным количеством костей и жира. И в этом случае необходима дополнительная информация, разъясняющая потребителю преимущества новых продуктов.
По мере того как качество искусственных продуктов питания улучшалось и они приближались по органолептическим и технологическим характеристикам к натуральным продуктам, возникло новое затруднение. Оно заключалось в отсутствии достаточно точного и универсального термина для обозначения широкой гаммы новых продуктов, который мог бы быть использован на этикетках для информирования потребителя о реальной природе продукта. В качестве такого термина можно было бы использовать, например, такие, как «искусственный», «имитирующий», «аналог» и т. п., однако был принят другой путь, более полно учитывающий как психологию потребителя, так и требования законодательства. Пять ведущих фирм, производящих искусственные продукты питания, в США: «Арчер даниельс мидланд ко.», «Дженерал миле инк.», «Свифт энд ко.», «Ральстон пьюрина ко.» и «)Вор-тингтон фудз инк.» (с 1970 г. входит в «Майлз лебореториз»), разработали проект общего стандарта на новые продукты. Он включает родовое наименование «Текстурированные белковые продукты» («Textured Protein Products»—ТРР), описание основных характеристик текстуры продукта, сохраняющейся при нагреве в условиях кулинарной обработки, данные о минимальном содержании белка, витаминов и минеральных солей (в расчете на 100 ккал) и требования к биологической ценности белка (КЭБ); последняя не должна быть ниже 70% от казеина. Этот стандарт был принят в 1970 г. ФДА («Фуд энд драг администрей-шен») и стал руководством для этикетирования новых продуктов [13,14,23,24].
Указанные меры, в сочетании с улучшением качества, позволили преодолеть трудности начального этапа производства повых продуктов.
Можно отметить ряд причин, обусловивших рост потребления искусственных продуктов питания, наблюдаемый в последнее время. Во-первых, по мере совершенствования технологии они становятся все более привлекательными и по своим оргаполептиче-ским, потребительским характеристикам и по биологической ценности удовлетворяют требованиям все более широких кругов потребителей. Во-вторых, этому в немалой степени способствовало повышение цен па пищевые продукты. В табл. W приведены данные о росте цен на натуральное мясо в США. Дополнительным
ИЦП — новая область крупнотоннажного производства 221
стимулом послужили две наблюдаемые в последнее время тенденции, а именно, рост числа работающих женщин, а также все возрастающее стремление потребителя экономить на обслуживании и готовить пищу самостоятельно, что привело к росту спроса на более удобную в приготовлении и использовании пищу. Немаловажную роль играют также диетические функции искусственных продуктов питания. Так, при рекламе, например, искусственных
Таблица 49
Стоимость натуральных мясопродуктов (рубленой говядины) в США [25]
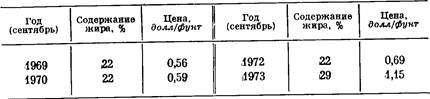
мясопродуктов делается упор на более высокое, в сравнении с натуральными, содержание белка и полиненасыщенных жирных кислот, пониженную калорийность, отсутствие холестерина, а также соответствие аминокислотного, витаминного и минерального состава медико-биологическим рекомендациям. Сведения о биологической ценности некоторых искусственных мясопродуктов
приведены в табл. 50.
Выше уже отмечалось, что более половины взбитых сливок и
отбеливателей кофе, потребляемых в США, а также значительное количество мороженого и молочных напитков являются искусственными продуктами. Что касается искусственных мясопродуктов, то опытные партии мясопродуктов волокнистой структуры (ИМВ-аналоги) поступили в пробную продажу начиная с середины 60-х годов. Несколько позднее начали использовать искусственные мясопродукты пористой структуры (ИМП-разба-вители), производство которых сразу же получило быстрое развитие.
Одним из первых искусственных мясопродуктов волокнистой
структуры, достигшим успеха па рынке США, был аналог бекона в виде небольших кусочков сухого или замороженного продукта. Он удобен в использовании, пригоден для приготовления салатов, соусов, применяется как добавка к спагетти, жареному картофелю, 'яичнице и т. п. При тех же розничных ценах, что и на натуральный продукт, он уже кулинарно обработан и готов к употреблению, не требует дорогостоящей упаковки, а в сухом виде — использования холода для хранения. Необходимо отметить, что после жарсния натурального бекона он резко уменьшается в вс-
222 Глава пятая
Таблица 50
Биологическая ценность искусственных мясопродуктов и некоторых натуральных продуктов [12, 13, 16, 26—29]

се, чего не происходит с искусственным аналогом. В результате стоимость последнего составляет около 50% от стоимости готового к употреблению натурального бекона. Другим аргументом потребления искусственного продукта является то, что его калорийность не превышает 30% от калорийности натурального. Уже в 1968 г. потребление этого продукта в США составило 1,3% от общого потребления бекона в стране (1,5 млрд. фунтов).
ИПП — новая область крупнотоннажного производства 223
К числу других искусственных мясопродуктов волокнистой структуры, завоевавших признание, относятся аналоги ветчины, мяса, цыплят и индюшатины. Оценка экономичности их использования также производится сопоставлением цен этих продуктов с ценами на готовые к употреблению натуральные продукты. Так, цена сформованной ветчины без костей составляла в 1971 г. около 1,3—1,4 долл/фунт, в то время как стоимость аналога — около 0,7 долл/фунт, т. е. экономия достигает 50%.
В 1971 г. постановлением Министерства сельского хозяйства (MGX) СШЛ [24] было рекомендовано использовать искусственные мясопродукты и другие искусственные продукты питания в программах детского питания. Цель этого постановления заключалась в том, чтобы улучшить белковое питание детей при меньших затратах и подготовить население страны к широкому потреблению искусственных продуктов питания в будущем. Оно, естественно, расширило рынок сбыта искусственных пищевых продуктов [3, 12, 20, 30—32]. Наибольшую роль искусственные продукты питания играют в программе школьных обедов.
В этих программах используют искусственные мясопродукты в виде разбавителей и аналогов (ИМП и ИМВ), искусственные молочные продукты (в частности, КСМ и ПСС; см. гл. IV), искусственные макароны (например, «голден элбоу») и ряд других [3, 24, 30, 31, 33, 34]. В постановлении МСХ США отмечено, что тскстурированныс белковые продукты могут быть использованы в комбинации с рубленым или нарезанным мясом в количестве до 30 ч. на 70 ч. основного продукта. При этом биологическая ценность (КЭБ) конечного продукта должна быть не меньше, чем для казеина (КЭБ — 2,5; см. табл. 50). В постановлении указаны также требования к химическому составу текстурированното белкового продукта, а именно, к содержанию белка, витаминов и минеральных солей в 100 з сухого продукта.
При получении рубленых мясопродуктов па 100 вес. ч. говядины использовали 12 вес. ч. ИМП, регидратировапного 24 вес. ч. воды. Экономия составляла около 21% [13]. При использовании искусственных мясопродуктов волокнистой структуры — аналогов, например цыплячьего мяса, экономия достигала 45% [13,14]. В 1973 г. экономический выигрыш от использования искусственных мясопродуктов возрос в результате общего подорожания натурального мяса в США [3, 32, 34] (см. табл. 49).
Сведения об экономической эффективности использования в качестве разбавителя искусственных мясопродуктов волокнистой структуры (типа «бонтрей») в количестве 25%, а также данные о биологической ценности и технологических свойствах готовых изделий приведены в табл. 51 [33].
По данным МСХ США, лишь в соответствии с программой школьных обедов в 1971/72 учебном году было потреблено около
| Глава пятая |
Таблица 51
Сравнение стоимости, состава, пищевой ценности и технологических свойств изделии из рубленого мяса (А) и тех же изделий с 25% разбавителя бонтрей (Б) [S3]. Цены на продукты приведены на сентябрь 1973 г. Продукт А
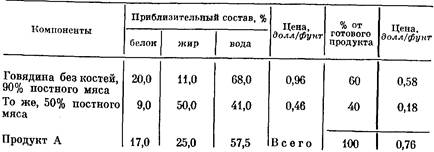
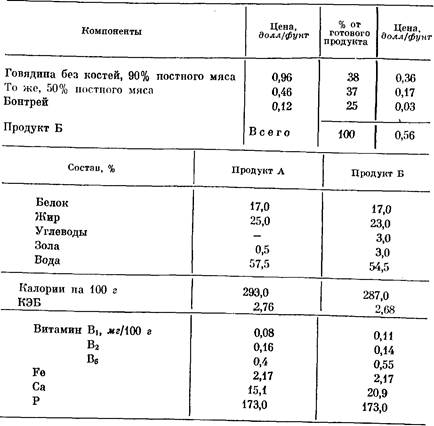
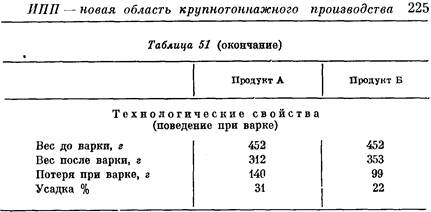
10 тыс. т искусственных мясопродуктов. Потребление искусственных макаронных изделий (20—25% белка, КЭБ выше 2,4) составило в 1973/1974 г. около 40 тыс. т [3, 32]. Министерство просвещения Японии также ведет подготовку к широкому использованию искусственных продуктов на основе сои по программе школьных обедов [35].
ПРОИЗВОДСТВО
ИСКУССТВЕННЫХ ПРОДУКТОВ ПИТАНИЯ И ЕГО ПЕРСПЕКТИВЫ
В настоящее время ата новая отрасль производства продуктов питания лишь начинает формироваться даже в тех странах, где существуют необходимые для этого предпосылки (прежде всего сырьевые, технологические, научно-технические и др.).
В 1973 г. в США было переработано в продукты питания до 0,5 млн. т белков обезжиренной соевой муки, что, однако, составляет лишь около 3% ее производства (16—17 млн. т обезжиренной муки в 1973 г.). Около 100 тыс. т обезжиренной муки бобов сои было использовано для производства концентратов и изолятов соевого белка. Из 125 заводов США, производящих обезжиренную соевую муку, только 12 перерабатывали ее в искусственные продукты питания. Производство искусственных мясопродуктов в США и Японии достигло уровня нескольких десятков тысяч тонн (см. табл. 21 и табл. 24). В США их производством было занято 6 фирм в 1967 г., 12 — в 1971—1972 гг. и порядка 15 — в 1974 г., а в Японии в 1974 г.— более 20 фирм [3, 12—14, 19, 36].
Производство искусственных продуктов питания в США развивается не только для нужд внутреннего рынка. Во все возрастающих масштабах США экспортируют сырье, продукцию и строят заводы в различных странах мира. Стоимость экспорта бобов
226 Глава пятая
сои из СШЛ возросла со 100 млн. долл. п 1960 г. до 2 млрд. долл. в 1972 г. Общий объем поставок из США обогащенных и искусственных продуктов питания на базе белка бобов сои составил за год (1.VII.1972 — 30.VI.1973) более 460 млн. т [32, 37].
Для области производства искусственных продуктов питания характерны высокие темпы развития [12, 20, 26, 38, 39]. Предполагается, что в 1985 г. общий объем производства искусственных мясопродуктов в Западной Европе составит около 2,8 млн. т, а искусственного молока — около 3,5 млн. г.
Предполагается, что производство и потребление искусственных мясопродуктов в Англии (в 1972г.— 1,5 г) составит в 1980 г.— 10%, а к 1990 г.—более 25% от объема потребления натуральных мясопродуктов. Потребление искусственного молока в 1980 г. будет на уровне 5% от натурального [38].
Текстурированные белковые продукты (ИМВ и ИМИ — аналоги и разбавители) в настоящее время заменяют в США около 1% мяса. Если, однако, в 1966 г. было продано искусственных мясопродуктов на 2,5 млн. долл., то в 1970 г. на 10 млн. долл., а в 1972 г. уже на 82 млн. долл. Научный отдел МСХ США оценивает рост продажи искусственных продуктов питания на основе сои до 2 млрд. долл. к 1980 г. Прогнозы производства искусственных мясопродуктов в США весьма разноречивы. Так, научный отдел МСХ США и некоторые университеты считают, что к 1980 г. их производство будет эквивалентно 8 или 10—20% от производства натуральных мясопродуктов, не считая мяса птицы [3, 12, 26, 40—43]. Однако ряд руководящих сотрудников МСХ и фирм США считают, что эти величины составят к 1980 г. более 20% [3] и даже более 25—50% [26, 44, 45]. Между тем производство в размере 10—20% от натурального мяса, т. е. в соответствии с умеренными прогнозами, отвечает 0,9—1,8 млн. г готовых к употреблению искусственных продуктов питания [26]. Предполагается также, что мясо птицы будет заменяться искусственными аналогами не столь быстро (около 3,9% к 1980 г.) ввиду сравнительно низкой стоимости и лучших диетических качеств. По той же причине производство искусственного молока к 1980 г. составит чуть больше 3% от потребления молочных продуктов в США, т. е. около 1,4 млн. т (в пересчете на цельное коровье молоко) [42]. Считают, что к 1980 г. производство искусственных продуктов в США позволит сократить поголовье молочных коров не менее чем на 260 тыс. голов, крупного рогатого скота мясных пород — па 3,7 млн. голов, овец — на 0,6 млн. и свиней — на 6,4 млн., а также высвободить около 1,2 млн. га земли, занятой под производство кормов. При этом появится возможность сократить затраты на сельскохозяйственную технику, удобрения, компоненты кормов, топливо и другие материалы.
Организация производства искусственных продуктов питания
ИПП — новая область крупнотоннажного производства 227
как совершенно новой крупнотоннажной отрасли промышленности требует известного времени. Как было показано выше, даже начальный этап развития производства искусственной пищи, отвечающий 10—20% объема производства традиционных продуктов питания массового потребления, займет в наиболее промышленно развитых странах не менее 15—20 лет. В этот ближайший период уровень питания населения будет поэтому зависеть почти исключительно от эффективности традиционной сельскохозяйственной технологии, животноводства и рыболовства. Однако уже на начальном этане развитие промышленности искусственных пищевых продуктов способно существенным образом повысить эффективность традиционной технологии за счет переработки белков, белковых отходов и других ценных пищевых веществ (казеин, сумма белков обрата и сыворотки, растительных белков, белков морепродуктов, муки зерновых низших сортов, крахмала и т. д.) и снижения потерь пищевого сырья при хранении (переработка картофеля, зерна и т. п.) и таким образом улучшить и удешевить белковое питание.
Возвращаясь к проблеме дефицита белка и ряда других компонентов питания и учитывая неотложность решения этой проблемы, необходимо отметить, что путь развития и совершенствования традиционной технологии, очевидно, не всегда самый доступный и экономичный. Расширение площадей возделываемых земель, повышение их плодородия, использование более интенсивных культур и приемов, обеспечивающих лучшую сохранность сезонной продукции, позволяют увеличить продуктивность сельского хозяйства и общий объем пищевой продукции при условии реализации сложного комплекса мероприятий и больших капиталовложений. В то же время освоение производства искусственных продуктов питания позволяет уже при существующей сельскохозяйственной базе лишь путем промышленного развития достичь резкого повышения объема и экономичности производства пищи за счет более глубокой переработки имеющейся сельскохозяйственной продукции и ее более полного использования для питания. При планировании развития производства сельского хозяйства и пищевой промышленности целесообразно поэтому рассматривать вопрос о возможности и сравнительной экономической эффективности производства традиционных и искусственных продуктов питания с целью достижения рациональных соотношений в производстве пищи традиционными и новыми методами и наиболее экономичного удовлетворения потребностей населения в сбалансированном питании.
Исследования в области искусственной пищи в нашей стране возникли по инициативе академика А. Н. Несмеянова как результат глубокого анализа общего хода научного познания, тщательного учета современного уровня развития научного знания в об-
228 Глава пятая
ласти химии, физической химии и биологии при учете практических потребностей общества в самом широком их понимании. Такой подход потребовал разработки общих научных закономерностей получения и прямой переработки в пищу различных пищевых веществ. Он служит поэтому решению проблемы питания человечества как на базе сельскохозяйственного, так и нетрадиционного пищевого сырья, как в ближайшей, так и отдаленной перспективе, и создает научную базу для более рационального использования природных ресурсов в интересах общества.
Рассмотренные в данной книге научные основы области переработки белка в искусственные продукты питания находятся в стадии формирования и в первую очередь связаны с решением ряда сложнейших вопросов физической химии биополимеров.
Последующее развитие этой области производства позволит не только ликвидировать дефицит белка, но и улучшить питание и здоровье людей. Оно способно решительным образом снизить нагрузки на биосферу, обеспечить питание во много раз большего населения планеты.
ЛИТЕРАТУРА
1. V. О. Wodicka.—J. Am. Oil Chem. Soc.,51, N 1, 101 (1974).
2. H. C. Mussman— Ibid., p. 104. 3 E. L. Blitz— Ibid., p. 57.
4. A. G. Ward— Ibid., p. 107.
5. A. Lacourt.—Ibid., p. 190.
6. Д. Ohison— Ibid., p. 134.
7. H. Linke— Fleischwirtschaft,49, N 4, 469 (1969).
8. J. Rakosky, Jr— J. Agr. Food Chem., 18, N 6, 1005 (1970).
9. /. Rakosky, /r.—J. Am. Oil Chem. Soc.,51, N 1, 123 (1974).
10. Д. Hamm— Fleischwirtschaft, 48, N 5, 597 (1968).
11. A. Frown.— J. Am. Oil Chem. Soc.,51, N 1, 188 (1974).
12. Л. F. Robinson.— Food Technol., 26, N 5, 59 (1972).
13. D. B. Walker, F. E. Horan, R. E. Burket— Food Technol., 25, N 8, 54 (1971).
14. F. E. Horan.—In: «New protein foods», ch. 8. A. M. Altschul (Ed.). New York — London, Acad. Press, 1974, p. 367—411.
15. /. Coppock— J. Am. Oil Chem. Soc.,51, N 1, 59 (1974).
16. W. W. Thalin, S. Kuramoto.— Food Technol.,21, N 2, 64 (1967).
17. A. Gordon. Food Processing and Marketing. 1969, p. 267.
18. Meat menagement, Aug., 1970, p. 24.
19. M. R. Ashton, C. S. Burke, A. W. Holmes— Scientific and Technical Surveys, N 62, 1 (1970).
20. N. L. Lockmiller— Food Technol.,26, 56 (1972).
21. Д. Logon, E. Meddred— Food Technol., 20, N 5, 107 (1966).
22. A. R. Bailer, J. R. Klis— Food Process., 26, N 9, 115 (1965).
23. Federal Register, 35,236, 1830 (1970).
24. United States Department of agriculture. Food and nutrition service. Washington, D. C., 20250, F. N. S. Notice 219, 22.2.1971.
25. /. Т. McCloud— J. Am. Oil Chem. Soc.,51, N 1,141 (1974).
ИПП—новая область крупнотоннажного производства 229
26. M. D. Wilding— Ibid., p. 128.
27. /. Lefebvre.—СаЪ.. nutr. diet.,5, N 4, 46 (1971).
28. D. Rosenfield, W. E. Hartman.—l. Am. Oil Chem. Soc.,51, N 1, 91 (1974).
29. /. Bombal, L. N'Diaye, F. Fenardji, R. Ferrando.— Rev. mod. vet.,125, N 4,
469 (1974).
30. Food Technol., 27, N 8, 14 (1973).
31. D. Rosenfield.— Food Technol., 27, N 8, 36 (1973).
32. F. R. Senti— J. Am. Oil Chem. Soc.,51, N 1, 138 (1974).
33. K. M. Wolford— Ibid., p. 131.
34. R. W. Fischer.— Ibid., p. 178.
35. Т. Watanabe.— Ibid., p. 111.
36. F. E. Horan.— Ibid., p. 67.
37. Л Baltes.— Ibid., p. 52.
38. В. J. F. Hudson— Chem. Ind., N 6, 251 (1972).
39. H. L. Wilcke— J. Am. Oil Chem. Soc., 51, N 1, 175 (1974).
40. J. Маигоп.—ШЫ. Nutr. Diet.,21, 147 (1975).
41. E. L. Butz. U. S. Secretary Departement of agriculture, USDA 3427—73:
Soy protein — basis for better eating, 1973.
42. W. W. Gallimor. Synthetics and substitutes for agricultural products. Projections for 1980 marketing res. rept N 947, USDA. Washington, D. C., 1972.
43. W. A. Compton. Vegetable protein its future. Seminar on textured vegetable protein, its past, present, future. 3.12.1973. N. Y., Elkhart, Indiana, Miles Lab., 1973.
44. A. M. Altschul. Ibid.
45. D. C. Cogan. Ibid.
ОГЛАВЛЕНИЕ
ПРЕДИСЛОВИЕ .................................. 5
Глава первая
ИСКУССТВЕННЫЕ ПРОДУКТЫ ПИТАНИЯ — НОВОЕ НАПРАВЛЕНИЕ В ПРОИЗВОДСТВЕ ПИЩИ ........................ 9
Традиционные продукты питания ...................... 9
Пищевые продукты повышенной биологической ценности ........ 21
Искусственные продукты питания — новые формы пищи ........ 28
Общая характеристика ............................ 28
Основные особенности искусственных продуктов питания .... 30
Литература . . . . . . ............................... 35
Глава вторая
ФИЗИКО-ХИМИЧЕСКИЕ ОСНОВЫ ПЕРЕРАБОТКИ БЕЛКА
В ИСКУССТВЕННЫЕ ПРОДУКТЫ ПИТАНИЯ ............... 38
Искусственные продукты питания как многокомпонентные студни 38 Совместимость и взаимодействие белков и полисахаридов в водных средах ......................................... 42
Термодинамическая совместимость белков и полисахаридов ... 44 Реологические свойства и структура двухфазных жидких систем белок — полисахарид — вода ........................ 52
Электростатическое взаимодействие белков и полисахаридов в водных средах . . . . . ............................ 59
Студнеобразное состояние и проблема получения искусственных продуктов питания .................................. G9
Регулирование состава, свойств и структуры студней .......... 78
Наполненные студни ............................. 78
Смешанные студни ............................. 82
Комплексные студни . . . ......................... 86
Анизотропные студни ............................ 89
Получение анизотропных студней путем деформации двухфазных систем и их перевода в студнеобразное состояние ... 90 Ионотропные студни .......................... 96
О значении исследований процессов переработки белка в искусственные продукты питания . . . . ......................... 105
Литература . . . . . ................................ 107
Глава третья
БЕЛОК КАК СЫРЬЕ ДЛЯ ПОЛУЧЕНИЯ ИСКУССТВЕННЫХ ПРОДУКТОВ ПИТАНИЯ ............................... 114
Понятие о функциональных свойствах белка . . ............. 114
Оглавление
Белок соевых бобов ... ...............•....••...•••• 11°
Другие растительные белки . . . . ..............•.•...••• 131
Белки животного происхождения . . . . ................... 138
Белки дрожжей, водорослей и других одноклеточных .......... 141
Аминокислоты . . . . . . .............•...•••••.•••••• 1^6
Литература . . . . . ................................ 149
Глава четвертая
СПОСОБЫ ПОЛУЧЕНИЯ ИСКУССТВЕННЫХ ПРОДУКТОВ ПИТАНИЯ 152
Искусственное молоко и молочные продукты ................ 153
Искусственные крупяно-макаронные изделия . . . . ........... 162
Искусственные крупы . . . . . ....................... 163
Искусственные макаронные изделия . . . . .............. 168
Искусственные мясопродукты . . . . . .................... 173
Искусственные мясопродукты, имитирующие изделия из рубленого мяса (ИМР) ................................ 175
Искусственные мясопродукты волокнистой структуры (ИМВ) . . . 178
Прядение белковых пищевых волокон и их переработка в искусственные мясопродукты ......................... 182
Пищевые связующие для получения ИМВ ............... 189
Искусственные мясопродукты пористой структуры (ИМП) .... 191
Искусственный жареный картофель ...................... 199
Искусственная зернистая икра . . . . ..................... 202
Другие виды искусственных продуктов питания . . . .......... 207
Литература . . . . . ................................ 210
Глава пятая
ИСКУССТВЕННЫЕ ПРОДУКТЫ ПИТАНИЯ — НОВАЯ ОБЛАСТЬ
КРУПНОТОННАЖНОГО ПРОИЗВОДСТВА ................. 218
Потребление искусственных продуктов питания . . . .......... 218
Производство искусственных продуктов питания и его перспективы 225
Литература . . . . . ................................ 228
– Конец работы –
Используемые теги: Искусственные, Продукты, питания0.069
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Искусственные продукты питания
Что будем делать с полученным материалом:
Если этот материал оказался полезным для Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов