рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Медицина
- /
- Установления причины болезни при генетических, инфекционных заболеваниях, отравлениях
Реферат Курсовая Конспект
Установления причины болезни при генетических, инфекционных заболеваниях, отравлениях
Установления причины болезни при генетических, инфекционных заболеваниях, отравлениях - раздел Медицина, Тема Занятия: Основы Организации Лабораторной Службы. Клиническ...
Тема занятия: Основы организации лабораторной службы. Клиническая биохимия в структуре клинико-диагностических исследований. Основные задачи и методы лабораторного обследования, клиническая характеристика лабораторных тестов. Получение и подготовка крови и мочи для лабораторного исследования.
Клиническая лабораторная диагностика представляет собой медицинскую диагностическую специальность, состоящую из совокупности исследований in vitro биоматериала человеческого организма, основанных на использовании гематологических, общеклинических, паразитарных, биохимических, иммунологических, серологических, молекулярно-биологических, бактериологических, генетических, цитологических, токсикологических, вирусологических методов, сопоставления результатов этих методов с клиническими данными и формулирования лабораторного заключения.
В клинической медицине методы КЛД применяют для:
- подтверждения клинического диагноза или его уточнения,
- установления причины болезни (при генетических, инфекционных заболеваниях, отравлениях),
- характеристики формы, тяжести течения и определения прогноза болезни,
- выбора этиологической и патогенетической терапии,
- контроля за результатами лечения,
- обнаружения патологии при скрининговых исследованиях в диспансеризируемых контингентах населения.
Эти цели определяют КЛД как самостоятельную научную клиническую дисциплину, основными задачами которой являются:
1) разработка методов лабораторных исследований;
2) разработка требований к качеству выполнения аналитических методов и средств обеспечения этих требований;
3)установление пределов нормальных индивидуальных колебаний каждого исследуемого параметра состава и свойств биологических жидкостей и тканей;
4)изучение закономерных связей лабораторно выявляемых патологических отклонений с сущностью патологического процесса при конкретных заболеваниях;
5)установление диагностической, дифференциально-диагностической и прогностической ценности отдельных лабораторных тестов и их комбинаций;
6)создание диагностических лабораторных программ для оптимизации диагностики.
Первые три задачи выполняются специалистами лабораторного дела, остальные – в совместной работе с клиницистами.
В соответствии с объектами и методами исследования в КЛД выделяют следующие субдисциплины:
- Клиническая биохимия
- Гематология
- Цитология
- Лабораторная генетика
- Общеклинические исследования
- Иммунология
- Изосерология
- Молекулярная биология
- Бактериология
- Паразитология
- Вирусология
- Токсикология
- Коагулология
Цель занятия: Знакомство с основными принципами клинической лабораторной диагностики. Знание методов получения и подготовки биоматериала для лабораторного исследования.
Знать:
- основы организации лабораторной службы;
- цели, задачи и место клинической лабораторной диагностики в практической медицине;
- понятия диагностической чувствительности и специфичности теста;
- основные принципы получения биоматериала для биохимического исследования
Уметь:
- оценить правильность получения биоматериала для биохимических исследований,
Рассчитать диагностическую чувствительность и специфичность теста.
Надежность результатов зависит от качества применяемых лабораторией методов, приборов, реактивов, калибровочных материалов, от тщательности работы… Некоторые лабораторные тесты специфичны для нарушений деятельности… · Диагностическая чувствительность теста при определенной болезни представляет собой процентное выражение частоты…Технические средства для количественных и качественных исследований
Эти методы основываются на том, что различные вещества имеют максимум светопоглощения в определенных участках спектра. Наиболее широко распространенными приборами для морфологических исследований… В гематологических исследованиях применяются различные счетчики клеток крови, например, для измерения концентрации…Венозная кровь
В настоящее время взятие венозной крови осуществляется одноразовым шприцем с толстой иглой в стеклянную или пластиковую пробирку или вакуумными…Капиллярная кровь
Свернувшаяся и гемолизированая пробы не подлежат исследованию. Количество собираемой крови зависит от количества назначенных анализов и требуемых… Основные химические добавки, используемые при взятии крови на анализ: Этилендиаминтетраацетат (ЭДТА) – антикоагулянт, который предохраняет кровь от свертывания, связывая и эффективно…Сыворотка
Сыворотку получают из спонтанно свернувшейся цельной крови путем центрифугирования (1000–1200 об в течение 10–15 минут). Она не содержит факторов свертывания крови. Центрифугирование свернувшейся крови с целью получения сыворотки следует выполнять, только убедившись в том, что кровь полностью свернулась (в нормальных условиях кровь свертывается около 30 минут).
Плазма
Плазма получается из крови путем отделения клеток крови. В противоположность сыворотке она содержит факторы свертывания крови, т. е. является бесклеточной надосадочной жидкостью, получаемой при центрифугировании крови, свертываемость которой ингибирована добавлением антикоагулянтов. После этого полученную плазму (верхняя фаза) отобрать индивидуальным наконечником с фильтром (аэрозольным барьером) в количестве не менее 1 мл в сухую стерильную пластиковую пробирку типа Эппендорф.
Получение мочи для клинических лабораторных исследований
Сбор мочи проводится после тщательного туалета наружных половых органов, чтобы в мочу не попали выделения из них.
Далее сбор мочи, в зависимости от вида исследования, имеет свои особенности. 1. Для проведения общего анализа мочи собирают только утреннюю мочу, взятую в… 2. Для проведения пробы по Зимницкому (оценка концентрационной способности почек) за сутки собирают 8 порций мочи.…Сбор суточной мочи. Пациент собирает мочу в течение 24 часов, соблюдая обычный питьевой режим (1,5 - 2 л в сутки). Утром в 6 - 8 часов он опорожняет мочевой пузырь и отмечает время (эту порцию мочи выливают), а затем в течение суток собирают всю мочу в чистый широкогорлый сосуд емкостью не менее 2 л, с плотно закрывающейся крышкой. Последняя порция берется точно в то же время, когда накануне был начат сбор (время начала и конца сбора отмечают). Если не вся моча направляется в лабораторию, то количество суточной мочи измеряют мерным цилиндром, отливают часть в чистую посуду, в которой ее доставляют в лабораторию, и обязательно указывают объем суточной мочи.
6. Порядок подготовки для проведения исследования на пробу Реберга (оценка секреторной и экскреторной функции почек):
1. Утром помочиться в туалет.
2. Выпить 300-400 мл жидкости.
3. Через 10-15 минут помочиться в туалет.
4. Лечь в постель и через 60 и через 120 минут помочиться в отдельную посуду (2раза)
5. Измерить объем мочи.
6. В промежутке между опорожнением мочевого пузыря взять кровь для исследования на креатинин.
Доставить в лабораторию и провести исследование в тот же день.
7. 3-стаканная проба. Используется для установления уровня гематурии и источника лейкоцитурии. Пробу проводят только в утренние часы без предварительного туалета наружных половых органов. Без перерывов в акте мочеиспускания больной собирает мочу в 2 сосуда, не опорожняя полностью мочевого пузыря. Затем после массажа простаты в 3-ий сосуд собирается 3-я порция мочи.
ВОПРОСЫ ДЛЯ ОБСУЖДЕНИЯ
2. Основные лабораторные методы исследования 3. Структура и оснащение современных лабораторий 4. Диагностическая специфичность тестаСАМОСТОЯТЕЛЬНАЯ РАБОТА СТУДЕНТОВ
2. Записать способы взятия и подготовки мочи для общеклинических и биохимических исследований. Дать заключение с внесением в протокол. 3. Записать основные принципы взятия и подготовки крови для биохимических… 4. Определить диагностическую чувствительность и специфичность тестов в клинических задачах.Тема занятия: Принципы клинической биохимии и КЛД. Организация контроля качества лабораторных исследований. Виды лабораторных исследований. Унификация биохимических методик. Стандартизация исследований.
Правильную диагностическую информацию с помощью лабораторных исследований можно получить, зная нормальные величины данного лабораторного теста, пределы внутри- и межиндивидуальных колебаний и влияние на них различных факторов.
Источниками вариабельности показателей КЛД являются такие биологические факторы, как возраст, пол, масса и поверхность тела (особенно важны при обследовании детей); околосуточные месячные и сезонные ритмы; этническое происхождение; условия, в которых производится забор материала для анализа (положение тела, физическое напряжение, прием жидкости, курение, прием лекарств, стресс и др.), а также климатогеографические условия и экологическая обстановка в районе проживания больного.
Истинно нормальными (референтными) считают величины лабораторных показателей, установленные в группах тщательно обследованных здоровых лиц в возрасте 20—30 лет, а нормальными для контингента, отличающегося по каким-либо признакам (по полу, возрасту, профессии, месту обитания и т.д.), — величины этих показателей у здоровых лиц данного контингента. При этом в оценке отклонений величины какого-либо показателя учитывают и так называемую индивидуальную норму — величину показателя у данного пациента, установленную ранее при профилактических и диспансерных обследованиях. Сравнивая обнаруживаемые у обследуемого результаты лабораторных исследований с нормальными для него и для соответствующего ему контингента, а также с референтными величинами, можно получить наиболее достоверное суждение о характере обнаруженного отклонения. Для оценки результатов единичного анализа необходимо знание пределов колебания показателей в норме с вычислением верхней и нижней границ с помощью статистических методов.
Цель занятия: Ознакомление с принципами клинической биохимии, организацией контроля качества лабораторных исследований. Знать понятия скрининговое, профилактическое и дифференциально-диагностическое исследования, экспресс-диагностика, унификация биохимических методик.
Знать:
- организацию контроля качества лабораторных исследований;
- понятие о скрининговом, профилактическом и дифференциально-диагностическом исследовании, экспресс-диагностике;
- понятие о стандартизации исследований.
Уметь:
- оценить правильность ведения контроля качества в лаборатории;
Выбрать адекватные средства и методы контроля качества.
Для выявления и оценки систематических и случайных погрешностей результатов измерений, производимых в лаборатории, осуществляют внутрилабораторный и… При этом используют ряд критериев качества: • Точность измерений – близость результатов к истинному значению измеряемой величины. Высокая точность соответствует…Клиническая молекулярная биология и диагностическая генетика
Исследует генетический материал – хромосомы, гены, нуклеиновые кислоты для выявления разных типов мутаций, лежащих в основе наследственных заболеваний и пороков развития. Современные методы ДНК-диагностики – гибридизационный анализ, амплификация геномов, полимеразная цепная реакция, ДНК-зонды и другие незаменимы в пренатальной диагностике, а также широко используются для определения вирусов и бактерий.
Клиническая токсикология
Обеспечивает лабораторную диагностику острых и хронических отравлений, вызванных органическими и неорганическими веществами, лекарственными препаратами и т.д. Высокая степень загрязнения окружающей среды, производства с вредными условиями, техногенные аварии и многие другие факторы определяют современную значимость этой области медицины.
Клинико-лабораторная паразитология
Выявляет и идентифицирует возбудителей паразитарных заболеваний – насекомых, гельминтов, простейших. Такие заболевания имеют определенные территориальные и социальные особенности распространения, но в связи с высокой миграционной активностью населения у людей появляются паразитарные заболевания, не характерные для мест постоянного проживания, поэтому лабораторная паразитология в настоящее время сохраняет высокую актуальность и значимость.
Лабораторный контроль (мониторинг) лекарственной терапии
Используя комплекс биохимических, физико-химических, цитологических и других методов осуществляет контроль за соотношением дозы и эффекта лекарственных препаратов, их индивидуальной фармакокинетикой. Такой лабораторный контроль распространен еще недостаточно широко, хотя необходим и эффективен при лекарственной терапии опухолей, неотложных состояний, длительных хронических заболеваниях и т.д. Современные автоматизированные системы регистрации обеспечивают высокую скорость и точность анализов.
Клинические анализы крови
Костный мозг является органом, в котором рождаются и созревают клетки крови. Через определенное время клетки поступают в кровеносное русло, в… Подсчет количества клеточных элементов, который может производиться, как в… Кроме того, определяя количество эритроцитов, лейкоцитов, тромбоцитов и других элементов, концентрацию гемоглобина и…Исследования свертывающей системы крови
Расстройства гемостаза могут быть причинами самостоятельных заболеваний, но чаще всего они играют очень серьезную роль в течении, а иногда и в…Исследования эндокринной системы
Продукция гормонов находится под контролем нервной системы, которая через гипоталамус осуществляет регуляцию синтеза гормонов в гипофизе. Гормоны… Получить информацию об активности эндокринной железы можно путем…Исследования функции почек
Пробы, используемые для изучения функции почек, в одних случаях позволяют оценивать их способность концентрировать мочу и выводить воду, в других –…Исследования функции печени
Печень участвует в синтезе белков, углеводов, жиров, в пигментном обмене, образовании мочевины, креатина и целого ряда других соединений. Велика…Маркеры опухолей
Опухолевые маркеры используются для контроля за течением заболевания и эффективности проводимой химиотерапии, хирургического и биологического… В соответствии с Государственным стандартом, во всех отраслях науки и техники,… Единицей количества вещества, содержащего столько же структурных элементов, сколько содержится атомов в нуклиде…ВОПРОСЫ ДЛЯ ОБСУЖДЕНИЯ
2. Референтные величины и средний показатель. 3. Скрининговое, профилактическое и дифференциально-диагностическое… 4. Основные единицы СИ в биохимии.САМОСТОЯТЕЛЬНАЯ РАБОТА СТУДЕНТОВ
2. Записать способы взятия и подготовки мочи для общеклинических и биохимических исследований. Дать заключение с внесением в протокол. 3. Записать основные принципы скринингового, профилактического и… 4. Записать основные единицы СИ в клинической биохимии.Тема занятия: Биохимические исследования при заболеваниях печени. Функции печени. Лабораторные тесты диагностики заболеваний печени. Клинические и биохимические синдромы. Гипоальбуминемия и гиперглобулинемия. Энзимодиагностика заболеваний печени.
Печень играет важную роль в обмене белков, углеводов, липидов. Клетки печени метаболизируют, детоксицируют и экскретируют экзо- и эндогенные вещества. Важной функцией печени является синтез белков плазмы. В печени также синтезируется желчные кислоты, необходимые для переваривания и всасывания жиров. Гликолиз, цикл Кребса, синтез и распад аминокислот, реакции окислительного фосфорилирования – все эти процессы представлены в гепатоцитах, богатых митохондриями. В печени представлены 2 основных типа клеток: гепатоциты или паренхиматозные клетки, составляющие около 60% всей клеточной массы, и Купферовы клетки, входящие в состав ретикуло-эндотелиальной системы и составляющие 30% от всех клеток печени.
Цель занятия: Освоить основные лабораторные методы диагностики заболеваний печени, изучить основные функции печени, клинические и биохимические синдромы поражения печени, диагностическое значение определения ферментов.
Знать:
- основные функции печени;
- клинические и биохимические синдромы поражения печени;
- методы лабораторной диагностики заболеваний печени.
Уметь:
- оценить правильность выбора лабораторного метода исследования функции печени;
Определять характер заболевания печени, основываясь на лабораторных данных.
Функции печени
Обмен углеводов.
Выход глюкозы из печени поддерживает уровень сахара кррови в промежутках между приемами пищи; основными источниками глюкозы при этом является гликоген (гликогенолиз и глюконеогенез). Печень также превращает в глюкозу галактозу и фруктозу.
Обмен аминокислот и белков.
Аминокислоты, получаемые из пищи и образующиеся при катаболизме белков тканей, поступают в печень. В печени некоторые из них дезаминируются или трансаминируются до кетокислот, другие метаболизируются до мочевины и аммиака. В печени также синтезируется большинство белков плазмы (за исключением иммуноглобулинов, синтезируемых лимфоидной тканью).
Обмен липидов.
Обмен желчных кислот.
Основными желчными кислотами являются холевая и хенодезоксихолевая кислоты, синтезируемые из холестерина только в печени. Они секретируются в желчь, и большая их часть вновь возвращается по кровотоку из кишечника в печень. Синтез новых желчных кислот регулируется количеством «реутилизированных» кислот. Кишечная микрофлора дегидроксилирует первичные желчные кислоты до вторичных кислот – дезоксихолевой и литохолевой.
Конъюгация и детоксикация.
Конъюгации и детоксикации подвергаются стероидные гормоны и лекарственные препараты.
Функции печени и методы их оценки
Лабораторные тесты диагностики заболеваний печени Под тестами оценки функций печени обычно подразумеваются измерения компонентов… · Обструкция билиарного трактаЩелочная фосфатаза.
Печень не является единственным источником активности ЩФ. Умеренные количества ЩФ представлены в костях, тонком кишечнике, плаценте, почках.Лактатдегидрогеназа.
Уровень ЛДГ часто возрастает при гепатоцеллюлярной дисфункции, хотя на практике определение активности этого фермента редко используют в диагностике заболеваний печени из-за низкой специфичности показателя (фермент широко распространен в организме).
Глутамилтранспептидаза.
Активность γ-глутамилтранспептидазы в плазме резко повышается (иногда более, чем в 50 раз) при холестазе и является показателем печеночной… Глутаматдегидрогеназакатализирует превращение глутаминовой кислоты в… Глутаматдегидрогеназа - один из органоспецифических ферментов, определяется в сыворотке крови при заболеваниях…ВОПРОСЫ ДЛЯ ОБСУЖДЕНИЯ
2. Лабораторные методы диагностики заболеваний печени. 3. Клинические и биохимические синдромы при заболеваниях печени. 4. Нарушение целостности гапатоцита: синдром цитолиза.САМОСТОЯТЕЛЬНАЯ РАБОТА СТУДЕНТОВ
2. Записать виды клинических и биохимических синдромов при заболеваниях печени. Дать характеристику каждому из синдромов с описанием основных… 3. Записать основные ферменты, использующиеся для лабораторной диагностики…Тема занятия: Биохимические исследования при заболеваниях печени. Типы желтух. Гипербилирубинемия и билирубинурия. Образование билирубина и его фракций в крови, печени, кишечнике, почках. Свободный (непрямой) и коньюгированный (прямой) билирубин, уробилиноген и стеркобилиноген, желчные пигменты. Токсичность билирубина. Желтуха новорождённых. Референтные значения, дифференциальная диагностика заболеваний печени. Фракции билирубина в крови, моче, кале.
Желтуха представляет собой желтое неестественное окрашивание кожи или склер. Это связано с присутствием в плазме билирубина в концентрациях, превышающих 40 мкмоль/л. В норме концентрация билирубина в плазме менее 22 мкмоль/л.
Имеются 3 основные причины повышения уровня билирубина в крови:
· Скорость синтеза билирубина повышена и превышает выделительную способность печени (гемолитическая, надпеченочная желтуха).
· Угнетение конъюгационных и/или выделительных механизмов в печени – снижается способность печени метаболизировать синтезируемый в нормальных количествах билирубин (печеночная, гепатоцеллюлярная желтуха).
· Обструкция билиарной системы, препятствующая оттоку желчи (холестатическая, подпеченочная, механическая, обструкционная желтуха).
Цель занятия: ознакомиться с основными типами желтух, механизмом образования билирубина и его фракций, изучить дифференциальную диагностику заболеваний печени.
Знать:
- основные типы желтух;
- дифференциальную диагностику заболеваний печени;
- основные фракции билирубина;
- механизм образования основных фракций билирубина.
Уметь:
- определять тип желтухи, основываясь на лабораторных данных;
Определять характер заболевания печени, основываясь на лабораторных данных.
Типы желтух
Надпеченочная (гемолитическая) желтуха.
Причины желтухи
Гепатоцеллюлярная желтуха.
Холестатическая желтуха.
Внутри- и внепеченочныйхолестаз могут быть отдифференцированы ультразвуковым исследованием или биопсией печени, но не оценочными пробами функции… Внутрипеченочныйхолестаз часто является результатом генерализованной… Внепеченочная обструкция часто является результатом опухолей главных желчевыводящих путей, опухоли головки…Дифференциальная диагностика желтух
Метаболизм билирубина.
Билирубин образуется при распаде гемоглобина в клетках ретикулоэндотелиальной системы (РЭС), особенно активно в…Гемолитическая болезнь новорожденного
Клиническая диагностика. Проявляется сонливостью, плохим сосанием, умственной отсталостью, ригидностью затылочных мышц, тоническими судорогами,… Лабораторная диагностика. В крови выявляются выраженная анемия, ретикулоцитоз,…Физиологическая (транзиторная) желтуха новорожденных
· относительное снижение активности УДФ-глюкуронилтрансферазы в первые дни жизни, связанное с повышенным распадом фетального гемоглобина, · абсолютное снижение активности УДФ-глюкуронилтрансферазы в первые дни… · дефицит лигандина,Желтуха недоношенных
· относительное снижение активности УДФ-глюкуронилтрансферазы в первые дни жизни, связанное с повышенным распадом фетального гемоглобина, · абсолютное снижение активности УДФ-глюкуронилтрансферазы в первые дни… · дефицит лигандина,Оценка синтетической функции печени
Протробиновое время (РТ). Этот показатель наиболее точно и главное быстро отражает синтетическую функцию печени т.к. все факторы свертывания (кроме… Мочевина и аммиак. Эти показатели не играют основной роли в лабораторной… 1. Увеличение его продукции (гастроинтестинальное кровотечение, большое количество белка в диете).Изменение лабораторных показателей при различных видах заболевания печени
Референтные значения печеночных проб
Дополнительные тесты: Тест Норма Общая лактатдегидрогеназа (ЛДГ) 0,8—4,0 ммоль/(ч·л) …Фракции билирубина в крови
· Общий билирубин
· Прямой (связанный) билирубин
· Непрямой (несвязанный)
Фракции билирубина в моче
В норме в сыворотке крови содержится в среднем 17 мкмоль/л общего билирубина, из которого только 10— 15 % входит в состав прямой фракции. Непрямой билирубин не может проходить через почечные тельца, и поэтому моча здорового человека не содержит этого пигмента. Появление в моче билирубина указывает на повышение в крови прямой его фракции и, как правило, является признаком нарушения экскреции желчных пигментов в кишки.
Фракции билирубина в кале
Стеркобилиноген образуется также из билирубин-глюкуронида, поступающего из печени в двенадцатиперстную кишку и попавшего в толстую кишку. Этот…ВОПРОСЫ ДЛЯ ОБСУЖДЕНИЯ
2. Гипербилирубинемия и билирубинурия. 3. Образование билирубина и его фракций в крови, печени, кишечнике, почках. … 4. Свободный (непрямой) и коньюгированный (прямой) билирубин, уробилиноген и стеркобилиноген, желчные пигменты.САМОСТОЯТЕЛЬНАЯ РАБОТА СТУДЕНТОВ
2. Записать механизм образования, его основные фракции, их роль в лабораторном исследовании при заболеваниях печени. 3. Записать особенности формирования желтухи у новорожденных. 4. Записать основные референтные значения, дифференциальную диагностику заболеваний печени.Тема занятия: Белки плазмы крови, функции. Синтез белков в печени, РЭС, клетках иммунной системы. Определение содержания общего белка в крови и моче. Характеристика белковых фракций. Белки острой фазы воспаления. Типы протеинограмм.
Белки представляют собой высокомолекулярные полипептиды, состоящие из более 20 видов α-аминокислот. Различают простые и сложные белки. Простые белки содержат только аминокислоты, а сложные – ещё и неаминокислотные компоненты: гемм, производные витаминов, липиды, или углеводы и др.
Поскольку при многих заболеваниях наблюдают изменения в содержании отдельных белков, исследование их концентрации в крови широко используют в диагностических целях. В биологических жидкостях определяют общий белок, фракции белков и индивидуальные белки.
Цель занятия:Знать белковый состав плазмы крови, методы определения общего белка в биологических жидкостях, научиться интерпретировать протеинограммы при различных патологических процессах.
Знать:
- белки плазмы крови и их функцию;
- синтез белков в печени, РЭС, клетках иммунной системы;
- методы определения содержания общего белка в крови и моче;
- белковые фракции плазмы крови и их характеристики;
- белки острой фазы воспаления, функции, критерии диагностики;
- нормальную протеинограмму, а также при различных патологических состояниях (при остром и хроническом воспалении, нарушении функций почечного фильтра, злокачественных новообразованиях, гепатитах, циррозах печени, механической желтухе).
Уметь:
- интерпретировать полученные результаты протеинограмм при различных патологических состояниях организма человека;
- оценить результат лечения воспалительного процесса по данным показателей белков острой фазы.
Плазма крови человека в норме содержит более 100 видов белков. Примерно 90% всего белка крови составляют альбумины, иммуноглобулины, липопротеины, фибриноген, трансферрин; другие белки присутствуют в плазме в небольших количествах.
Функции белков плазмы крови:
· поддерживают постоянство коллоидно-осмотического давления крови;
· определяют вязкость крови и сохраняют устойчивость эритроцитов и лейкоцитов в кровотоке, обеспечивают нормальный кровоток в капиллярах (реологические свойства крови);
· белковая буферная система участвует в регуляции кислотно-щелочного состояния;
· специализированные белки связывают и транспортируют углеводы, липиды, гормоны, лекарства, витамины, токсичные вещества;
· удерживают в связанном состоянии и транспортируют катионы кальция, магния, железа, меди и другие ионы, препятствуя их потере с мочой;
· специализированные белки участвуют в свертывании крови (фибриноген, протромбин, антигемофильный глобулин и др.);
· иммуноглобулины, факторы системы комплемента, трансферрин и пропердин (предупреждая инфекционный процесс и сохраняя резистентность организма) выполняют защитную функцию;
· являются резервом аминокислот.
Синтез белков плазмы крови осуществляют:
· печень– полностью синтезирует фибриноген и альбумины крови, большую часть α- и β-глобулинов;
· клетки ретикулоэндотелиальной системы (РЭС) костного мозга и лимфатических узлов – часть β-глобулинов и γ-глобулины (иммуноглобулины).
Состояние белкового обмена в организме оценивают, определяя содержание общего белка, белковых фракций и индивидуальных белков плазмы крови.
Методы определения общего белка
Среди методов определения концентрации общего белка можно выделить несколько основных групп, основанных на различных принципах:
· азотометрические;
· гравиметрические (весовые);
· «преципитационные»;
· спектрофотометрические;
· рефрактометрические;
· колориметрические;
· нефелометрические;
· поляриметрические.
Азотометрические методы
Недостатком азотометрических методов является длительность и сложность процедуры, даже при том, что аммиак, образующийся в реакции, можно определять…Гравиметрические методы
Гравиметрические (весовые) методы определения общего белка сыворотки основаны на высушивании белков до постоянной массы и взвешивании на аналитических весах. Методы трудоемки и в настоящее время практически не используются для определения общего белка сыворотки. Гравиметрический метод продолжает использоваться в некоторых лабораториях для определения фибриногена в плазме крови.
Преципитационные» методы
Результаты данной группы методов зависят от множества факторов: скорости смешивания реактивов, температуры реакционной смеси, значения рН среды,… Спектрофотометрические методы Спектрофотометрические методы заключаются в измерении степени cветопоглощения в ультрафиолетовой области при двух…Рефрактометрические методы
Колориметрические (фотометрические) методы
Среди колориметрических методов определения концентрации общего белка сыворотки наиболее распространенным считается биуретовый метод, основанный на… Колориметрические методы определения общего белка сыворотки крови достаточно…Общий вид электрофореза
Количество выделяемых фракций определяется условиями проведения электрофореза. При электрофорезе на бумаге и пленках ацетата целлюлозы в…Нормальная протеинограмма
Альбуминовая фракция включает в себя альбумин (основная часть) и преальбумин – ее доля составляет более 50% от всех белков плазмы. Глобулиновые фракции более разнородны. Фракция альфа1-глобулина включает в себя следующие белки:Типы протеинограмм
Тип протеинограммы Альбумины Фракции глобулинов Примеры заболеваний α1 α2 … Для интегральной оценки протеинограмм используется А/Г коэффициент…Классификация БОФпостепени увеличения их концентрации
В сыворотки крови
Данные белки запускают каскад реакций для отграничения воспалительного очага, от неповрежденных тканей, восстановление нарушенной структуры и… Синтез белков острой фазы активируется под действием провоспалительных… Особенностью большинства БОФ является их неспецифичность и высокая корреляция концентраций в крови с активностью…Тесты на БОФ используемые в клинической практике.
2. При сопутствующей бактериальной инфекции. При любых заболеваниях, либо после операции присоединение бактериальной инфекции, будь то местный… 3. При некрозе тканей. Некроз тканей вызывает острофазный ответ, аналогичный… 4. Для контроля эффективности лечения хронических заболеваний. Существует корреляция между активностью воспаления,…ВОПРОСЫ ДЛЯ ОБСУЖДЕНИЯ
2. Функции белков крови. 3. Синтез белков в печени, РЭС, клетках иммунной системы. 4. Общий белок в сыворотке крови, гипо- и гиперпротеинемия.САМОСТОЯТЕЛЬНАЯ РАБОТА СТУДЕНТОВ
2. Расшифровать протеинограммы при различных патологических состояниях организма человека. Дать заключение с внесением в протокол. 3. Записать тесты на белки острой фазы используемые в клинической практике.…Тема занятия: Биохимическая диагностика заболеваний поджелудочной железы. Активность ферментов в дуоденальном соке. Панкреатиты, диагностическое значение определения активности α-амилазы в крови и моче. Активность трипсина, α1- протеиназного ингибитора, α2-макроглобулина в крови.
Поджелудочная железа – орган продолговатой формы, расположенный в брюшной полости. Играет важную роль в преобразовании поглощаемой пищи в “топливо” для клеток. Поджелудочная железа выполняет две основные функции: экзокринную, которая отвечает за переваривание и эндокринной функции, которая регулирует уровень сахара в крови.
Анатомия: поджелудочная железа расположена позади брюшины и окружена другими органами, включая тонкую кишку, печень и селезенку. Длина органа – около 15 см и он имеет форму плоской груши. Поджелудочная железа имеет головку, которая обращена к центру брюшной полости, шею, тело и хвост.
Цель занятия: знать биохимическую диагностику заболеваний поджелудочной железы, диагностическое значение определения активности ферментов в крови и моче.
Знать:
- ферменты поджелудочной железы;
- диагностическое значение определения активности α-амилазы в крови и моче;
- диагностическое значение определения активности трипсина, α1- протеиназного ингибитора, α2-макроглобулина в крови.
Уметь:
- интерпретировать данные относительно содержания ферментов поджелудочной железы в крови и моче.
Функции поджелудочной железы:
1. Экзокринная функция. Поджелудочная железа содержит экзокринные железы, выделяющие пищеварительные ферменты. Когда пища попадает в желудок, эти панкреатические соки попадают в систему протоков, которые собираются в основной поджелудочный проток. Поджелудочный проток впадает в общий желчный проток, формируя Фатеров проток, который расположен в двенадцатиперстной кишке. Общий желчный проток берет начало в печени и желчном пузыре и продуцирует желчь. Панкреатические соки и желчь, которые попадают в двенадцатиперстную кишку, переваривают жиры, углеводы и белки.
2. Эндокринная функция. Эндокринный компонент поджелудочной железы состоит из островков клеток, которые продуцируют и выделяют важные гормоны, непосредственно в кровоток. Основные гормоны поджелудочной железы - инсулин, который понижает уровень сахара в крови, и глюкагон, который увеличивает уровень сахара в крови. Поддержание нормального уровня сахара в крови необходимо для функционирования ключевых органов, включая мозг, печень, и почки.
Воспаление поджелудочной железы называется панкреатитом. Эта болезнь имеет две формы: острую и хроническую. Каждая форма может привести к осложнениям. В тяжелых случаях, могут быть кровотечение, инфекция, и перманентное повреждение ткани. Обе формы панкреатита встречаются чаще у мужчин, чем у женщин.
Острый панкреатит - воспаление поджелудочной железы, которое происходит внезапно и обычно лечится за несколько дней. Острый панкреатит может быть опасной болезнью с серьезными осложнениями. Основная причина острого панкреатита – желчекаменная болезнь. Хроническое злоупотребление алкоголем - также частая причина. Острый панкреатит может возникнуть в течение от нескольких часов до 2 дней после употребления алкоголя. Другие причины острого панкреатита включают травмы брюшной полости, инфекции, опухоли и генетические отклонения поджелудочной железы.
Хронический панкреатит - воспаление поджелудочной железы. Данная форма панкреатита не вылечивается и не идет на поправку. Наоборот, со временем приводит к перманентному поражению железы. Хронический панкреатит, как и острый панкреатит, происходит, когда пищеварительные ферменты “атакуют” поджелудочную железу и соседние ткани, вызывая при этом приступы боли. Хронический панкреатит чаще развивается у людей в возрасте 30-40 лет.
Самая частая причина хронического панкреатита – злоупотребление алкоголем в течение продолжительного времени. Хроническая форма панкреатита может быть вызвана одной острой атакой, которая приводит к повреждению поджелудочного протока. Поврежденный поджелудочный проток приводит к воспалению железы.
Лабораторные тесты:
1) Сывороточная амилаза. Увеличение уровня амилазы обычно свидетельствует о панкреатите.
2) Сывороточная липаза. При остром панкреатите почти всегда увеличивается уровень липазы в сыворотке крови.
3) Подсчет лейкоцитарной формулы. Количество лейкоцитов увеличивается в период обострения панкреатита. Иногда происходит значительное увеличение.
4) Печеночные пробы. Увеличивается уровень печеночных ферментов, в частности, аланинаминотрансфераза и щелочная фосфотаза могут быть признаком острого панкреатита, вызванного желчекаменной болезнью.
5) Билирубин. Уровень билирубина в сыворотке крови может увеличиваться при закупорке общего желчного протока.
6) Трипсин. Это панкреатический фермент, который, наряду с печеночной желчью, переваривает жиры. Измерение концентрации трипсина в сыворотке – один из самых чувствительных тестов при панкреатите, в том числе, хроническом.
Другие тесты, которые могут быть использованы для оценки осложнений при остром панкреатите, включают:
-определение уровня глюкозы,
-определение уровня кальция,
-определения уровня магния,
-определение концентрации С-реактивного белка (маркер воспаления).
Другие тесты, которые могут быть использованы при постановке диагноза и оценке хронического панкреатита, включают:
-фекальный жир,
-фекальная панкреатическая эластаза,
-молекуляро-диагностические тесты для определения генетических мутаций, ассоциированных с фиброзом мочевого пузыря.
Альфа-амилаза– основной фермент, участвующий в гидролизе углеводов, а именно разложении крахмала и гликогена до декстринов, мальтозы и глюкозы. Места образования фермента – слюнные железы и поджелудочная железа. В сыворотке крови выделяют, таким образом, панкреатический (Р-тип) и слюнной (S-тип) α-амилазы. Определение активности α-амилазы в сыворотке и моче используется преимущественно в диагностике заболеваний поджелудочной железы. При остром панкреатите через 2 – 12 часов от начала приступа наблюдается преходящее увеличение активности α-амилазы сыворотки; уровень фермента возвращается к норме на 3-й или 4-й день. Обычно происходит 4 – 6-кратное увеличение уровня с максимумом в период 12 – 72 часа от начала приступа. Альфа-амилаза экскретируется почками, поэтому увеличение активности фермента в сыворотке крови приводит к повышению активности α-амилазы мочи.
Диагностическое значение анализа
Основная ценность определения Р-типа α-амилазы заключается в том, что увеличение ее активности высокоспецифично для заболеваний поджелудочной железы. Панкреатическая α-амилаза повышается при остром панкреатите. Активность общей амилазы в этом случае повышена за счет панкреатической фракции. Диагностическая чувствительность панкреатической фракции амилазы в сыворотке крови для острого панкреатита составляет 92%, специфичность – 85%.
Альфа-амилаза при панкреатите
Панкреатическая α-амилаза в моче повышается при остром панкреатите, причем составляет основную часть общей амилазы, так как выводится с мочой… Активность панкреатической фракции амилазы в отличие от общей не повышается… Повышение уровня α-амилазы сыворотки крови также встречается при:ВОПРОСЫ ДЛЯ ОБСУЖДЕНИЯ
2. Понятие и формы панкреатита. 3. Лабораторные тесты при остром и хроническом панкреатите. 4. Диагностическое значение определения α-амилазы при заболеваниях поджелудочной железы.САМОСТОЯТЕЛЬНАЯ РАБОТА СТУДЕНТОВ
2. Записать основные формы панкреатита и их характеристику. 3. Записать лабораторные тесты для диагностики заболеваний поджелудочной… 4. Записать диагностическое значение определения α-амилазы, α-1-антитрипсина и α-2-макроглобулина при…Тема занятия: Сахарный диабет. Определение, классификация и клинические признаки. Абсолютная и относительная недостаточность инсулина. Влияние инсулина на метаболизм. Содержание глюкозы в цельной крови и плазме. Диагностические критерии сахарного диабета I и II типов. Гипергликемия и глюкозурия. Нарушенная гликемия натощак, нарушенная толерантность к глюкозе, постпрандиальная гипергликемия
Сахарный диабет (СД) – хронический метаболический синдром, характеризующийся гипергликемией, глюкозурией и связанными с ними нарушениями обмена веществ. Развивается вследствие абсолютной или относительной (нарушение взаимодействия с клетками-мишенями) недостаточности гормона инсулина и приводит к нарушению углеводного, жирового и белкового обмена.
Цель занятия:изучить основные формы сахарного диабета, уметь их дифференцировать согласно основным симптомам и клиническим проявлениям, правильно оценивать результаты гликемического профиля, глюкозотолерантного теста.
Знать:
- классификацию сахарного диабета и его формы;
- основные симптомы и клинические проявления;
- отличие абсолютной и относительной инсулиновой недостаточности;
- разницу в содержании глюкозы в цельной крови и плазме;
- принцип глюкозотолерантного теста.
Уметь:
- интерпретировать полученные результаты глюкозотолерантного теста;
- оценивать результаты гликемического профиля
Основным симптомом, определяющим патогенез и клинику СД, является гипергликемия. В норме содержание глюкозы натощак колеблется в пределах 3,3 – 5,5 у детей до 14 лет, 3,8 – 5,8 ммоль/л у взрослых. В цельной крови концентрация глюкозы ниже по сравнению с плазмой. Причина этого несоответствия – меньшее содержание воды в цельной крови. Глюкоза крови подвергается полной ультрафильтрации в клубочках почек, а затем полностью реабсорбируется в почечных канальцах. Однако способность канальцевого эпителия к обратному всасыванию глюкозы имеет количественный предел (почечный порог глюкозы 8,9 – 10 ммоль/л). Поэтому, как только гликемия и содержание глюкозы в первичной моче превысит этот предел, появляется глюкозурия.
Классификация сахарного диабета:
В настоящее время предложена классификация сахарного диабета, использующая этиологический принцип.
Этиологическая классификация сахарного диабета (ВОЗ, 1999).
I. Сахарный диабет 1-го типа (деструкция бета-клеток, абсолютная инсулиновая недостаточность):
А. Аутоиммунный.
Б. Идиопатический.
II. Сахарный диабет 2-го типа (претерпевает развитие от преимущественной резистентности к инсулину с относительной инсулиновой недостаточностью до преимущественно секреторного дефекта инсулина в сочетании с периферической инсулинорезистентностью).
III. Другие специфические типы сахарного диабета.
A. Генетические дефекты бета-клеточной функции
B. Генетические дефекты в действии инсулина.
C. Болезни экзокринной части поджелудочной железы.
D. Эндокринопатии.
E. Сахарный диабет, индуцированный химикатами и лекарствами.
F. Инфекции (врожденная краснуха, цитомегаловирус, вирусы Коксаки).
G. Необычные формы иммуноопосредованного диабета.
Н. Другие генетические синдромы, иногда сочетающиеся с сахарным диабетом (синдром Дауна, синдром Кляйнфельтера, синдром Тернера и т.д.).
IV. Диабет беременных.
Сахарный диабет бывает двух типов.
В клинической картине сахарного диабета принято выделять 2 группы симптомов – основные, а также второстепенные.
Основные симптомы сахарного диабета следующие:
Полиурия, то есть усиленное выделение мочи, которое вызывается повышение ее осмотического давления из-за наличия в моче растворенной глюкозы (в норме глюкоза в моче человека присутствовать не должна). Проявляется обильным учащенным мочеиспусканием в дневное, а также в ночное время.
Полидипсия, то есть неутолимая постоянная жажда, обусловленная существенными потерями с мочой воды, а также увеличением осмотического давления крови. Больные выпивают за сутки 3 – 5 л и более жидкости.
Полифагия, то есть неутолимый постоянный голод. Данный симптом вызывается сопровождающим диабет нарушением обмена веществ, а точнее неспособностью клеток поглощать, а также перерабатывать глюкозу без инсулина.
Признаками диабета первого типа являются: жажда, частое мочеиспускание, большая потеря веса, сухость во рту, раздражительность, быстрая утомляемость, тошнота, иногда рвота. Второстепенными признаками диабета такого типа служат: боли в сердце, боли в икроножных мышцах и судороги в них, фурункулез, кожный зуд, головные боли, раздражительность и нарушения сна. Говоря о второстепенных признаках диабета 1-го типа у детей, следует отметить появление не наблюдавшегося ранее ночного недержания мочи и быстрое ухудшение состояния здоровья.
Для диабета второго типа характерно онемение и судороги ног, болевые ощущения в ногах, а также в руках, чувство постоянной жажды, зуд, помутнение в глазах, плохое заживление ран, наличие кожных инфекций, утомляемость, а также сонливость, снижение болевой чувствительности, частые инфекционные заболевания, постепенное увеличение веса, снижение у мужчин потенции и пр. Кроме этого, при диабете второго типа наблюдается выпадение растущих на ногах волос на фоне усиленного роста волос на лице, появление на теле небольших желтых наростов, именуемых ксантомами. Также к первым признакам диабета 2-го типа относится воспаление крайней плоти, связанное с частым мочеиспусканием.
Влияние инсулина на метаболизм
Практически во всех тканях организма инсулин влияет на обмен углеводов, жиров, белков и электролитов, увеличивая транспорт глюкозы, белка и других веществ через мембрану клетки.
Основное действие инсулина заключается в усилении транспорта глюкозы через мембрану клетки. Содержание глюкозы в сыворотке крови является отражением состояния двух постоянно меняющихся процессов, находящихся под постоянным контролем инсулина: утилизация глюкозы тканями и поступления глюкозы в кровоток.
Свое биологическое действие на уровне клетки инсулин осуществляет через соответствующий рецептор в тканях. Стимуляция инсулином приводит к увеличению скорости поступления глюкозы внутрь клетки в 20 – 40 раз. Транспорт глюкозы через мембрану клетки осуществляется белками-транспортерами. При стимуляции инсулином наблюдается увеличение в 5 – 10 раз содержания транспортных белков глюкозы в плазматических мембранах при одновременном уменьшении на 50 – 60% их содержания во внутриклеточном пуле. Стимуляция транспорта глюкозы увеличивает потребление энергии в 20 – 30 раз.
Большая часть инсулина метаболизируется в печени, за один пассаж в ней задерживается 40 – 60% гормона, поступающего из систем портальной вены. Инсулин после связывания с рецепторами гепатоцитов подвергается протеолизу, сопровождающегося инактивацией гормона. Около 40% инсулина инактивируется почками. Следует отметить, что при почечной недостаточности поглощение и инактивация инсулина почками уменьшаются до 9 – 10%, поэтому у больных сахарным диабетом при почечной недостаточности потребность в инсулине снижается (синдром Зуброды-Дана).
Абсолютная и относительная недостаточность инсулина
В основе болезни лежит абсолютная и относительная инсулиновая недостаточность.
Абсолютная недостаточностьобусловлена уменьшением выработки инсулина В-клетками островков Лангерганса поджелудочной железы в результате их дистрофических изменений или некроза под влиянием повреждающих факторов или нарушением синтеза инсулина, приводящим к инкреции гормона со сниженной биологической активностью.
Абсолютной инсулиновой недостаточности способствуют аутоиммунные процессы (нарушение системы иммуногенеза, приводящее к развитию процессов аутоиммуноагрессии с избирательным поражением В-клеток), вирусная инфекция, воспалительные заболевания, фиброз или кальциноз поджелудочной железы, циркуляторные изменения (атеросклероз), опухолевые процессы.
Абсолютная инсулиновая недостаточность является причиной развития сахарного диабета лишь у 10% больных. В большинстве случаев возникновение заболевания происходит при нормальной и даже повышенной концентрации эндогенного инсулина в крови. Причиной развития обменных нарушений в этих случаях является относительная инсулиновая недостаточность, в основе которой лежит снижение чувствительности инсулинозависимых тканей к действию эндогенного инсулина - тканевая инсулинорезистентность.
Гипергликемя и глюкозурия
Гипергликемия – клинический симптом, обозначающий повышенное содержание сахара (глюкозы) в сыворотке крови. Гипергликемия появляется преимущественно при сахарном диабете или других заболеваниях эндокринной системы.
Существует несколько условных степеней выраженности симптома:
- легкая гипергликемия (уровень сахара составляет 6 – 10 ммоль/л);
- гипергликемия средней тяжести (10 – 16 ммоль/л);
- тяжелая гипергликемия (более 16 ммоль/л).
У людей, болеющих сахарным диабетом, встречаются две разновидности гипергликемии:
- гипергликемия натощак (если человек не принимал пищи около 8 часов, уровень сахара в крови возрастает свыше 7,2 ммоль/л);
- гипергликемия постпрандиальная (после приема пищи уровень сахара в крови превышает 10 ммоль/л).
Критерии диагностики СД и других категорий гипергликемии (ВОЗ,1999)
| Тесты, ммоль/л | Концентрация глюкозы в ммоль/л | |||
| цельная кровь | плазма | |||
| Сахарный диабет | ||||
| Натощак | > 6,1 | > 6,1 | > 7,0 | > 7,0 |
| Через 2 ч после нагрузки глюкозой или оба показателя | > 10,0 | > 11,1 | > 11,1 | > 12,2 |
| Нарушенная толерантность к глюкозе | ||||
| Натощак (если определяется) | < 6,1 | < 6,1 | < 7,0 | < 7,0 |
| Через 2 ч после нагрузки глюкозой | > 6,7 и < 10,0 | > 7,8 и < 11,1 | > 7,8 и < 11,1 | > 8,9 и < 12,2 |
| Нарушенная гликемия натощак | ||||
| Натощак | >5,6 и < 6,1 | >5,6 и < 6,1 | >6,1 и < 7,0 | > 6,1 и 7,0 |
| Через 2 ч | < 6,7 | < 7,8 | < 7,8 | < 8,9 |
Глюкозурия – это выявление глюкозы в моче. В моче здорового человека глюкоза содержится в очень низкой концентрации (0,06 – 0,083 ммоль/л). Поэтому, а также из-за низкой чувствительности методов, она не выявляется при исследовании мочи в клинико-диагностических лабораториях.
Обнаружение глюкозы в моче свидетельствует о патологии.
Глюкозурия зависит от трех факторов:
· концентрации глюкозы в крови,
· количества фильтрата клубочков почки за 1 минуту,
· количества реабсорбированной в канальцах глюкозы в 1мл.
Глюкозурии чаще предшествует гипергликемия. Профильтровавшаяся в почечных клубочках глюкоза реабсорбируется в проксимальном отделе почечных канальцев.
При нормально функционирующих почках глюкозурия появляется только в том случае, когда уровень глюкозы в крови превышает 8,8 – 9,9 ммоль/ л, так называемый «почечный порог» или гломерулярный клиренс глюкозы. Понятие это относительное, так как «почечный порог» определяется ферментной системой почечного эпителия и, следовательно, в значительной степени индивидуален. У ребенка «почечный порог» выше (10,45 – 12,65 ммоль/л).
Объем клубочковой фильтрации также влияет на уровень глюкозурии. Его снижение даже при высоком уровне глюкозы крови может не вызвать глюкозурии. Поэтому при некоторых хронических заболеваниях почек порог глюкозы повышается. В случае нефропатии, сопровождающейся нарушением резорбции глюкозы (ренальный диабет), возможна глюкозурия и при нормальном или пониженном уровне глюкозы в крови.
Толерантности к глюкозе
Нарушение толерантности к глюкозе – это состояние, которое предшествует диабету. При этом состоянии уровень глюкозы крови пациента уже выше нормального, но ниже того, при котором ставится диагноз диабета.
Диагностические критерии оценки глюкозотолерантного теста
Диагностическая важность этого состояния в том, что на этой стадии уже можно… Поэтому проведение глюкозотолерантного теста позволяет выявить группы риска больных, которые в перспективе могут…Постпрандиальная гипергликемия
Результаты недавнего анализа, проведенного учеными, подтвердили, что улучшение гликемического контроля значительно снижает частоту встречаемости… В итоге достоверно признано, что постпрандиальная гипергликемия является… Таким образом, постпрандиальная гликемия вызывает серьезные осложнения, и ее необходимо контролировать.ВОПРОСЫ ДЛЯ ОБСУЖДЕНИЯ
2. Классификация сахарного диабета. 3. Основные формы сахарного диабета. 4. Диагностические критерии сахарного диабета I и II типов.САМОСТОЯТЕЛЬНАЯ РАБОТА СТУДЕНТОВ
1. Записать протокол практического занятия с указанием ее цели и задачи, форм сахарного диабета, основных клинических симптомов, нормы содержания глюкозы и отличие в ее содержании в цельной крови и плазме, принципа глюкозотолерентного теста, абсолютной и относительной инсулиновой недостаточности.
2. Интерпретировать результаты глюкозотолерентного теста. Дать заключение с внесением в протокол.
Тема занятия: Сахарный диабет. Методы определения содержания глюкозы. Ранняя диагностика сахарного диабета: определение антител к β-клеткам поджелудочной железы, проинсулина, С-пептида. Компенсация сахарного диабета. Эффективный контроль гипергликемии: определение гликозилированного гемоглобина, фруктозамина. Оценка степени сосудистого риска: HbA1C, глюкоза плазмы венозной крови натощак, глюкоза капиллярной крови перед едой, постпрандиальная гипергликемия, показатели липидного спектра. Гипогликемическая кома.
В настоящее время во всем мире накоплены доказательства того, что эффективный контроль сахарного диабета может свести к минимуму многие осложнения, связанные с ним. Так, улучшение контроля за уровнем глюкозы в крови может значительно уменьшить риск развития как микроангиопатии, так и макроангиопатии. На каждый процент снижения гликозилированного гемоглобина риск развития микрососудистых осложнений (ретинопатии, нефропатии) снижается на 35%.
Цель занятия:изучить основные методы определения содержания глюкозы, маркеры ранней диагностики сахарного диабета, уметь выявлять маркеры сосудистого риска.
Знать:
- методы определения содержания глюкозы;
- основные маркеры ранней диагностики сахарного диабета ;
- гликозилированный гемоглобин и фруктозамин – как эффективный котроль гипергликемии;
- оценку сосудистого риска при сахарном диабете;
- понятие о гипогликемической коме.
Уметь:
- интерпретировать полученные результаты содержания гликозилированного гемоглобина;
- оценивать показатели липидного спектра.
Методы определения содержания глюкозы
Определение концентрации глюкозы в крови – одно из наиболее часто выполняемых биохимических исследований в клинико-диагностической лаборатории. Причина исключительной популярности теста связана с высокой заболеваемостью сахарным диабетом. Данный тест выполняется как в условиях стационара, так и в поликлиниках. Больные сахарным диабетом вынуждены исследовать уровень глюкозы в крови в домашних условиях, поскольку без этой информации им трудно скорректировать свою диету, физические нагрузки, применение инсулина и других сахароснижающих препаратов. Исключительная важность теста и большие объемы выполняемых исследований стимулировали разработчиков к созданию различных типов приборов и методов определения концентрации глюкозы в крови.
В настоящее время существует достаточно много методов определения глюкозы. Их можно классифицировать следующим образом:
1. Редуктометрические. Почти не используются.
2. Колориметрические. Почти не используются.
3. Ферментативные:
а) Глюкозооксидазный.
- фотометрический по конечной точке,
- фотометрический кинетический,
- отражательная фотометрия – сухая химия,
- электрохимический,
б) Гексокиназный.
Глюкозооксидазный метод.
Глюкозооксидаза катализирует перенос двух водородных атомов с первого углеродного атома глюкозы на кислород,…Гексокиназный метод.
Зависимость уровня гликозилированного гемоглобина
От среднего показателя глюкозы крови
Гемоглобин HbAIc является самой важной подгруппой фракции гемоглобина НвА1, состоящей из 3 компонентов (HbA1а; HbA1b; HbA1c). Количественно… О состоянии гликемического контроля в течение длительного времени можно судить… Фруктозамин – продукт гликозилирования белков плазмы крови (соединение глюкозы с белками). Более 60% всех белков,…Критерии степени нарушений углеводного обмена и риска развития сосудистых осложнений (макро- и микроангиопатий) при сахарном диабете 2-го типа
Как известно, хроническая гипергликемияявляется причиной развития и прогрессирования осложнений заболевания, а макроангиопатические осложнения –… Результаты недавнего мета–анализа, проведенного Stettler и коллегами,… · с повышенным риском ретинопатии;К каким же целевым показателям постпрандиальной гликемии следует стремиться?
Гипогликемическая кома Очень опасно повышение сахара в крови, однако не меньшие последствия вызывает… В основе этого состояния лежит гипогликемия, то есть понижение сахара в крови. Болезнь возникает при содержании…Гипогликемическая кома - это тяжелейшее проявление гипогликемии.
Легкая гипогликемия - (вне зависимости от степени выраженности симптомов) когда больному самостоятельно удается купировать ее приемом углеводов.
Тяжелая гипогликемия - (с различной степенью нарушения сознания) для выведения из которой требуется помощь другого лица, в виде парентерального введения глюкозы или пероральной дачи углеводов пациенту
Основная причина гипогликемии
Провоцирующие факторы: · Непосредственно связанные с медикаментозной сахароснижающей терапией: o Передозировка инсулина, ПСМ или глинидов (новонорм, старлекс): ошибка больного, неисправность инсулиновой…Клиническая картина
· Вегетативные симптомы: сердцебиение, дрожь, бледность кожи, потливость, мидриаз, тошнота, сильный голод, беспокойство, тревога, агрессивность
· Нейрогликопенические симптомы: слабость, нарушение концентрации, головная боль, говокружение, сонливость, парастензии, нарушения зрения, растерянность, дезориентация, дизартрия, нарушение координации движений, спутанность сознания, кома, возможны судороги и другие неврологические симптомы.
Чем быстрее снижается уровень глюкозы в крови, тем обычно ярче проявляются симптомы.
Показатели липидного спектра при сахарном диабете
· увеличение концентрации триглицеридов, · снижение уровня холестерина липопротеинов высокой плотности (ЛПВП) и · преобладание в крови мелких плотных частиц липопротеинов низкой плотности (ЛПНП) фенотипа В при пограничных…ВОПРОСЫ ДЛЯ ОБСУЖДЕНИЯ
2. Методы определения содержания глюкозы в крови. 3. Принципы глюкозооксидазного и гексокиназного методов. 4. Способы ранней диагностики сахарного диабета.САМОСТОЯТЕЛЬНАЯ РАБОТА СТУДЕНТОВ
2. Интерпретировать результаты содержания гликозилированного гемоглобина. Дать заключение с внесением в протокол. 3. Записать основные сдвиги в показателях липидного спектра. Дать заключение с…Тема занятия: Заболевания сердечно-сосудистой системы. Атеросклероз, стадии развития. Нарушения липидного обмена. Диагностическое значение определения содержания холестерола и его фракций в составе липопротеинов крови. Гиперхолестеролемия. Основные показатели атеросклероза. Рекомендуемые и пограничные значения общего холестерола, умеренная и выраженная гиперхолестеролемия.
Следствием нарушения липидного обмена являются сердечно-сосудистые заболевания, поэтому важно уметь диагностировать дислипидемии.
Цель занятия: научиться оценивать показатели липидного обмена и высчитывать риск развития сердечнососудистых заболеваний (ССЗ).
Знать:
- структуру и функции разных классов липидов,
- особенности исследования липидного спектра,
- алгоритмы диагностики дислипидемий,
- правила взятия крови для исследований липидного обмена,
- механизм развития атеросклероза и основные его осложнения.
Уметь:
-интерпретировать полученные результаты исследования липидного спектра при различных патологических состояниях организма человека.
Липиды -органические соединения, нерастворимые в воде, но растворимые в органических растворителях (эфире, бензине, хлороформе).
Классификация липидов.
Существует несколько классификаций липидов. Наибольшее распространение получила классификация, основанная на структурных особенностях липидов. По этой классификации различают следующие основные классы липидов.
A. Простые липиды:сложные эфиры жирных кислот с различными спиртами.
1. Глицериды (ацилглицерины, или ацилглицеролы – по международной номенклатуре) представляют собой сложные эфиры трехатомного спирта глицерина и высших жирных кислот.
2. Воска: сложные эфиры высших жирных кислот и одноатомных или двухатомных спиртов.
Б. Сложные липиды:сложные эфиры жирных кислот со спиртами, дополнительно содержащие и другие группы.
1. Фосфолипиды: липиды, содержащие, помимо жирных кислот и спирта, остаток фосфорной кислоты. В их состав часто входят азотистые основания и другие компоненты:
а) глицерофосфолипиды (в роли спирта выступает глицерол);
б) сфинголипиды (в роли спирта – сфингозин).
2. Гликолипиды (гликосфинголипиды).
3. Стероиды (холестерин).
4. Другие сложные липиды: сульфолипиды, аминолипиды, липопротеины.
B. Предшественники и производные липидов:жирные кислоты, глицерол, стеролы и прочие спирты (помимо глицерола и стеролов), альдегиды жирных кислот, углеводороды, жирорастворимые витамины и гормоны.
Функции липидов
2. Энергетическая: при расщеплении 1г жира выделяется 38,9 кДж нергии. 3. Запасающая: накапливаясь, – резервный источник энергии (капля жира в… 4. Защитная:Холестерин
Суточное потребление холестерина находится в диапазоне от 0,2 до 0,5 г. В организме ежедневно синтезируется более 1 г. Все клетки организма содержат его в составе своих мембран и теоретически способны его синтезировать. Общее количество холестерина в теле человека огромно - более 300 г.
Холестерин в связанной с жирными кислотами форме содержится в надпочечниках, гонадах (83%), в плазме крови (70%). В остальных тканях – в основном в свободном виде.
Функции холестерина
· участвует в обеспечении барьерной функции мембран; · влияет на активность мембранных ферментов; · избыток холестерина в цитоплазматической мембране затрудняет работу кальциевых насосов;Характеристика липопротеинов
ТГ – триглицериды, ХС – холестерин, ФЛ – фосфолипиды.Общий ХС = ХС ЛПНП + ХС ЛПОНП + ХС ЛПВП
Расчет ХС ЛПОНП
В моль/л ХС ЛПОНП = ТГ / 2,2
В мг/дл ХС ЛПОНП= ТГ / 5
Расчет ХС ЛПНП
В ммоль/л ХС ЛПНП = ОХС – ТГ / 2,2 – ХС ЛПВП
В мг/дл ХС ЛПНП= ОХС – ТГ / 5 – ХС ЛПВП
nоn-HDL Сhol = ХС – ХС ЛПВП
ХС ЛПНП = ХС – (ХС ЛПВП + ТГ* / 2,2)
*если уровень ТГ не превышает 4,5 ммоль/л (Формула Фридвальда)
Исследование липидного обмена
Правила взятия крови для исследования липидного обмена
2. Перед взятием крови пациент в течение 2 недель должен придерживаться своей обычной диеты. 3. Вечером накануне взятия крови должен быть исключен прием алкоголя:… 4. Если исследования липидов проводятся у больного, перенесшего инфаркт миокарда, то кровь следует брать либо в…Интерпретация результатов анализа
Целевые уровни содержания липидов в крови согласно Европейским рекомендациям по профилактике ССЗ в клинической практике, 2003 г.
Маркёрами увеличения риска смерти от ССЗ являются также: - ХС ЛПВП < 1,0 ммоль/л у мужчин и < 1,2 ммоль/л у женщин, - ТГ > 1.7 ммоль/лХарактеристики гиперлипопротеинемий
Развитие ГЛП может быть обусловлено наследственной предрасположенностью и факторами среды (первичный ГЛП), а также такими заболеваниями, как…Клиническая классификация гиперлипопротеинемий
| Первичные гиперлипопротеинемии | Вторичные гиперлипопротеинемии |
| Полигенные гиперлипопротеинемии Моногенные гиперлипопротеинемии Семейная гиперхолестеринемия Семейная комбинированная гиперлипидемия Дисбеталипопротеинемия Семейная эндогенная гиперглицеридемия Семейная хиломикронемия | Сахарный диабет Хронический алкоголизм Гипотиреоз Обструктивные заболевания печени Нефротический синдром Применение бета-блокаторов, диуретиков |
Диагностика нарушений липидного обмена
· ИБС с нарушениями мозгового кровообращения и кровотока в крупных артериях; · семейную предрасположенность к раннему развитию ИБС (у лиц моложе 60… · другие факторы риска: сахарный диабет, артериальную гипертензию и др.; локальные липидные отложения (ксантомы,…Следствием нарушения липидного обмена являются сердечно-сосудистые заболевания.
Атеросклероз- хроническое прогрессирующее заболевание артерий,… Главные факторы риска развития атеросклероза:Основные теории атеросклероза
· Паренхиматозного воспаления (Вирхов, 1856). · Артериомаляции (Тома, 1883). · Инфильтрационно-комбинационная (Аничков Н.Н., Халатов С.С., 1946).Алгоритм оценки риска ИБС
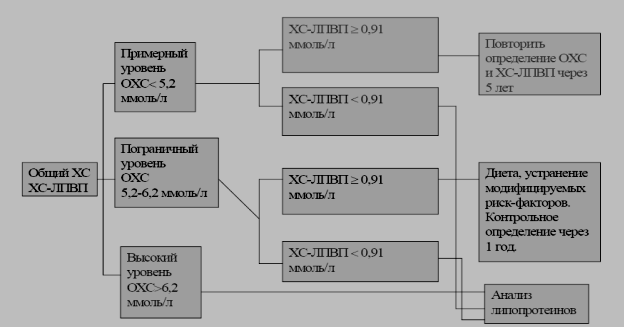
ВОПРОСЫ ДЛЯ ОБСУЖДЕНИЯ
2. Атерогенность липопротеинов, маркеры увеличения смертности от ССЗ. 3. Уровни холестерина (желаемый, погранично-высокий, высокий). 4. Правила взятия крови для проведения исследований липидного обмена.САМОСТОЯТЕЛЬНАЯ РАБОТА СТУДЕНТОВ
1. Записать протокол практического занятия с указанием его цели и задачи, классификации липидов, липопротеинов, таблицы интерпретации исследований липидного спектра.
2. Рассмотреть клинические случаи, связанные с нарушением обмена липидов. Дать заключение с внесением в протокол.
Тема занятия: Заболевания сердечно-сосудистой системы. Инфаркт миокарда. Нарушение снабжения сердца кислородом при ишемической болезни сердца. Основные метаболические нарушения при остром инфаркте миокарда. Условия обратимости изменений миокарда. Необратимые изменения сердечной мышцы. Маркерные ферменты миокарда. Энзимодиагностика инфаркта миокарда. Дифференциальная диагностика заболеваний сердца, ферментные констелляции. Неферментные маркеры инфаркта миокарда.
Сердечно-сосудистые заболевания (ССЗ) являются основной причиной смертности во всем мире. Диагностика возникновения и мониторинг лечения ССЗ занимает важное место в клинической лабораторной диагностике. Особое внимание уделяется экспресс-диагностике таких заболеваний как инфаркт миокарда.
Цель занятия:научиться использовать лабораторные данные в диагностике ССЗ.
Знать:
- биохимические маркеры инфаркта миокарда, сроки изменения их активности в крови;
- основные метаболические нарушения при остром инфаркте миокарда;
- основные и дополнительные исследования, проводимые при дифференциальной диагностике ССЗ.
Уметь:
- интерпретировать полученные результаты лабораторных исследований маркеров ССЗ.
Ишемическая болезнь сердца (ИБС) – это поражение миокарда, вызванное нарушением кровотока в коронарных артериях.
Факторы риска ИБС:
Биологические детерминанты или факторы:
· пожилой возраст;
· мужской пол;
· генетические факторы, способствующие возникновению дислипидемии, гипертензии, толерантности к глюкозе, сахарному диабету и ожирению.
Анатомические, физиологические и метаболические (биохимические) особенности:
· дислипидемия;
· артериальная гипертензия;
· ожирение и характер распределения жира в организме;
· сахарный диабет.
Поведенческие (бихевиоральные) факторы, которые могут привести к обострению ИБС:
· пищевые привычки;
· ожирение, как фактор развития ИБС;
· курение;
· недостаточная двигательная активность, или физические нагрузки, превышающие адаптационные возможности организма;
· потребление алкоголя.
Нарушение баланса между реальным кровоснабжением миокарда и потребностями его в кровоснабжении может произойти из-за следующих обстоятельств:
Внутрисосудистые причины:
· атеросклеротическое сужения просвета венечных артерий;
· тромбоз и тромбоэмболия венечных артерий;
· спазм венечных артерий.
Внесосудистые причины:
· тахикардия;
· гипертрофия миокарда;
· артериальная гипертензия.
Диагноз острого инфаркта миокарда (ОИМ), согласно рекомендациям ВОЗ, основывается на трех базисных постулатах:
1) клинической картине,
2) данных ЭКГ-исследований,
3) выявлении гиперферментемии (повышенной концентрации миокардиальных маркеров).
Диагноз ОИМ считается достоверным в случае, если два из трех названных диагностических критериев являются бесспорными и однозначно трактуемыми.
Развитие ишемии миокарда приводит к угнетению процессов окислительного фосфорилирования, активации гликолиза и гликогенолиза и ухудшению усвоения глюкозы неповрежденными отделами сердца.
В результате дефектов, возникающих в цитоплазматических мембранах миокардиоцитов, белки и ферменты, локализующиеся в цитоплазме, поступают в кровь больного ИМ со скоростью, зависящей в первую очередь от размера молекул. Изменение концентрации белков миокарда в сыворотке крови зависит также от скорости их элиминации из кровотока. Небольшие молекулы, например миоглобин, выводятся очень быстро, а большие, такие как лактатдегидрогеназа (ЛДГ), медленно. Поэтому содержание каждого белка при ОИМ имеет свою кинетику. Практическое применение методов определения общей креатинкиназы (КК), ЛДГ (включая изоформы), аспартатаминотрансферазы (АСТ) в качестве маркеров ИМ в настоящее время не рекомендуется вследствие их низкой специфичности.
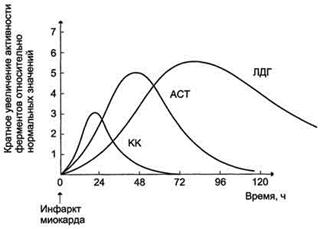
Аналогична ситуация с диагностикой нестабильной стенокардии. В последние годы в клинике все более широко используется определение в сыворотке (плазме) компонентов тропонинового комплекса миокардиоцитов – тропонинов I и Т, отвечающих критериям абсолютной миокардиальной специфичности при высокой диагностической чувствительности.
Чувствительность и специфичность маркеров ОИМ
Представлены средние показатели с указанием диапазонов отклонений от средних значений в пределах 95% доверительных интервалов (Eur. J. Cardiol.…Уровень кардиомаркеров в зависимости от времени после ОИМ
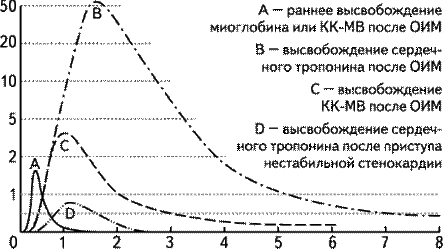
Современные требования к маркеру некроза миокарда
Маркеры ОИМ
Общая КК состоит из 3 изоферментов: ММ (мышечная), ВВ (мозговая), МВ. КК-МВ – димер, состоящий из двух субъединиц: М (мышечная) и В (мозговая). Повышение уровня КК-МВ в крови может свидетельствовать о таких патологиях, как:Миоглобин.
Повышение уровня миоглобина в крови может свидетельствовать о таких патологиях, как: · инфаркт миокарда; · синдром длительного сдавления;Тропонин I.
Анализ повышения тропонина крови применяется при: · диагностика ИМ; · оценка реперфузии после применения тромболитической терапии;Лактатдегидрогеназа (ЛДГ).
Изоферменты: ЛДГ 1 и 2 локализуются в сердце, ЛДГ 3 и 4 локализуются в легких, ЛДГ 5 локализуется в печени.
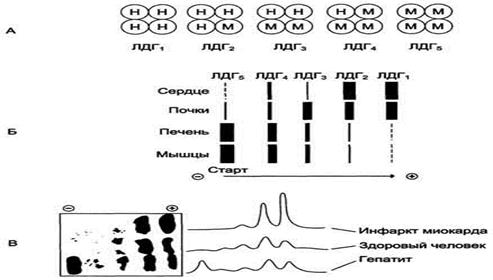
Повышение уровня ЛДГ в крови может свидетельствовать о патологиях:
· Сердечно-сосудистые заболевания.
· Заболевания печени.
· Анемии.
· Онкологические заболевания.
Диагностическая занчимость при ИМ:
При ОИМ уровень возрастает быстро на 2-4 сутки, и нормализуется только на 2 –3 неделе.
4. Аланинаминотрансфераза (АлАТ), аспартатаминотрансфераза (АсАТ).
Аминотрансферазы печени (АлАТ в большей степени), мышц, миокарда.
Уровень аминотрансфераз в крови повышается при повреждении печени и миокарда.
В норме соотношение активностей АСТ/АЛТ (коэффициент де Ритиса) равно 1,33±0,42. При остром ИМ это соотношение резко повышается.
Повышение АСТ в сыворотке крови наблюдается при ИМ через 6-12 часов от начала заболевания. Максимальное возрастание отмечается на 2-4 сутки, и на 5-7 сутки уровень фермента приходит к норме.
С-реактивный белок (СРБ).
Уровень СРБ в крови повышается при повреждении тканей (воспаление, травма). Концентрация CЗБ в сыворотке или плазме возрастает в течение 24-48 ч… Прочие маркеры: · Натрийуретические пептиды (мозговой, предсердный).Обязательные и дополнительные исследования при подозрении на заболевания сердечнососудистой системы
ВОПРОСЫ ДЛЯ ОБСУЖДЕНИЯ
2. Диагноз инфаркта миокарда, энзимодиагностика, маркеры высокой и низкой специфичности. 3. Креатинкиназа МВ, структура, диагностическая значимость при ОИМ. 4. Миоглобин, структура, диагностическая значимость при ОИМ.САМОСТОЯТЕЛЬНАЯ РАБОТА СТУДЕНТОВ
2. Рассмотреть клинические случаи. Дать заключение с внесением в протокол.Тема занятия: Заболевания почек. Фильтрационная, реабсорбционная и секреторная функция почек. Клинический и биохимический анализ мочи. Клиренс, транспортный максимум, почечный порог, функциональные показатели работы почек. Диурез и его нарушения. Физиологические и патологические компоненты мочи. Методы их определения. Гломерулярная, тубулярная, внепочечные протеинурии.
Заболевания почек и мочеполовой системы занимают важное место в структуре заболеваемости населения. По данным ВОЗ около 7-10% взрослого населения индустриально развитых стран имеют различную нефрологическую патологию. Среди многочисленных болезней почек широко распространены гломерулонефрит, пиелонефрит, поликистоз, гидронефроз, мочекаменная болезнь. В 2002 году Национальным почечным фондом США предложен термин – «Хроническая болезнь почек», объединяющий различные нозологические формы заболеваний почек. Хроническая болезнь почек – это повреждение почек либо снижение их функции в течение 3 месяцев и более. Существенное влияние на развитие и прогрессирование хронических заболеваний почек в той или иной популяции может оказать целый ряд факторов. К ним относятся распространенность некоторых инфекций, прием некоторых лекарственных препаратов, алкоголь и курение, состояние окружающей среды, климат, характер и традиции питания, генетические особенности популяции и др. Одновременно с этим артериальная гипертензия, сахарный диабет, аутоиммунные заболевания, дислипидемия, ожирение и метаболический синдром являются факторами, ассоциирующимися с развитием дисфункции почек.
Цель занятия:Знать основные заболевания почек: гломерулонефрит, пиелонефрит, почечная недостаточность, нефротический синдром, нефролитиаз. Иметь понятие о фильтрации, реабсорбции, секреции, физиологических и патологических компонентах мочи, нарушениях диуреза, клиническом и биохимическом анализе мочи.
Знать:
- основные заболевания почек: гломерулонефрит, пиелонефрит, почечная недостаточность, нефротический синдром, нефролитиаз;
- понятия о фильтрации, реабсорбции, клиренсе, почечном пороге;
- нарушения диуреза: полиурия, олигоурия, анурия, никтурия;
- нормальные уровни физиологических компонентов мочи: мочевина, кретинин, креатин, мочевая кислота;
- патологические компоненты мочи: глюкозурия, протеинурия и ее виды.
Уметь:
- провести оценку клинического и биохимического анализа мочи при основных заболеваниях почек;
- оценить нарушения диуреза;
- оценить содержание физиологических компонентов мочи;
- провести диагностическую оценку патологических компонентов мочи.
Правильная интерпретация результатов лабораторных тестов возможна в случае четкого представления о строении и функции почек, и процессе мочеобразования. Почки представляют собой парный паренхиматозный орган. Основной функциональной единицей почки является нефрон. Группы нефронов дают начало собирательным трубкам, которые открываются наружу в области верхушки почечного сосочка. Сосочек открывается в почечную чашечку, переходящую в почечную лоханку продолжением которой является мочеточник. Нефрон состоит из сосудистого клубочка, его капсулы (капсула Боумена-Шумлянского) и канальцевого аппарата (проксимального канальца, петли Генле, дистального канальца и собирательной трубки). Каждый отдел нефрона имеет высокую структурно-функциональную специализацию.
Клубочковая фильтрация представляет собой пассивный процесс перехода жидкой части плазмы крови из просвета капилляров клубочков в капсулу клубочка через почечный фильтр (эндотелий капилляров, базальная мембрана, эпителий капсулы). При этом вместе с плазмой крови фильтруются низкомолекулярные вещества. Скорость клубочковой фильтрации определяется: 1 – величиной почечного кровотока, 2 – внутриклубочковым гидростатическим давлением и 3 – площадью поверхности фильтрации. Следовательно, при повышении почечного кровотока, увеличении внутриклубочкового давления и при гипертрофии клубочков (увеличении площади поверхности фильтрации) скорость клубочковой фильтрации будет увеличиваться.
В клинической практике скорость клубочковой фильтации измеряется по методу Реберга-Тареева, основывающемся на определении клиренса эндогенного креатинина. Креатинин продукт метаболизма, в норме экскретируемый почками. Существует несколько вариантов пробы Реберга. Наиболее распространенные - это суточная и разовая. В суточной пробе Реберга определяется концентрация креатинина в сыворотке крови и в моче, собранной за сутки (24ч). Вычисляется минутный диурез: общее количество мочи за сутки (мл) разделить на 24 (ч) и на 60 (мин). Далее скорость клубочковой фильтрации рассчитывается по формуле:
СКФ = Креатинин мочи (моль/л) х минутный диурез (мл/мин) / Креатинин крови (моль/л)
Разовая проба Реберга проводиться утром до приема жидкости и после опоржнения мочевого пузыря. Далее обследуемый выпивает поллитра воды и через полчаса сдает кровь. Еще через полчаса собирает все мочу. Измеряется объем собранной мочи. Вычисляется минутный диурез: количество собранной мочи (мл) разделить на 60 (мин). СКФ вычисляется по ранее приведенной формуле.
Процесс реабсорбции протекает в проксимальных канальцах, петле Генли и в дистальных канальцах. Реабсорбция представляет собой способность клеток почечных канальцев к обратному всасыванию веществ из просвета канальцев в кровь. В просветах канальцев реабсорбируются все биологически важные органические вещества (глюкоза, аминокислоты, белок, мочевина), а также лактат, бикарбонат неорганический фосфор, хлор, калий, натрий. В петле Генли и дистальных канальцах реабсорбируются неорганические компоненты каналцевой жидкости: калий, натрий, магний, кальций.
Наряду с реабсорбцией в канальцах происходит секреция. Канальцевая секреция характеризуется способностью клеток почечных канальцев переносить из крови в просвет канальцев подлежащие выведению электролиты и различные вещества (органические, чужеродные, образованные в процессе метаболизма и синтезированные в клетках канальцев). В проксимальных канальцах осуществляется секреция органических кислот и оснований, конечных продуктов обмена чужеродных веществ. Секреция может быть пассивной и активной (с затратой энергии). В дистальном канальце осуществляется секреция ионов калия, водорода и аммиака. Способность почек к секреции ионов водорода и аммиака обеспечивает регуляцию кислотно-основного состояния, а способность секреции ионов калия – водно-солевой гомеостаз.
Изменение мочи являются важным признаком поражения почек и мочевыводящих путей, поэтому общий анализ мочи остается традиционным лабораторным исследованием состояния почек. Общий анализ мочи включает определение физико-химических свойств (цвет, прозрачность, реакция, относительная плотность, белок, глюкоза, кетоны, билирубин, уробилиноген) и микроскопию мочи. Физические параметры мочи во многом зависят от особенности диеты, водного режима, приема лекарственных препаратов, возраста и поэтому могут иметь диагностическое значение в совокупности с другими параметрами мочи.
Изменение цвета мочи признак, который побудит пациента, обратится к врачу. Следует помнить, что интенсивность окраски мочи зависит от концентрации урохромов (продуктов пигментного обмена). Прием пищи влияет на оттенки мочи. Свекла придает красный оттенок, а ревень – зеленый. Прием медикаментов может изменить цвет мочи. Аспирин придает розовый оттенок, амидопирин – красный, фурагин и 5 НОК – желто-коричневый, витамины – выраженную опалесценцию желтым цветом.
| Цвет мочи | Патологические состояния | Причина |
| Темно-желтый | Застойная почка, отеки, ожоги, понос, рвота | Повышенная концентрация красящих веществ |
| Бледный | Сахарный и несахарный диабет, ренальная глюкозурия, почечная недостаточность | Малая концентрация красящих веществ |
| Темно-бурый | Гемолитическая анемия | Уробилиногенурия |
| Темный (черный) | Острая гемолитическая почка, алкаптонурия, меланосаркома | Гемоглобинурия, меланин |
| Красный | Нефролитиаз, инфаркт почки, свинцовая анемия | Гематурия, уропорфиринурия |
| Вид «мясных помоев» | Острый и обострение хронического гломерулонефрита | Гематурия |
| Цвет пива, зеленовато-бурый | Паренхиматозная желтуха | Билирубинурия, уробилиногенурия |
| Зеленовато-желтый, коричневый | Механическая желтужа | Билирубинурия |
| Беловатый | Жировое перерождение | Липурия, гной, кристаллы фосфатов |
| Молочный | Лимфостаз почек | Хилурия |
Изменение цвета мочи часто зависит от наличия солей. Так мочевая кислота придает моче насыщенно-желтый цвет, ураты – кирпично-красный, фосфаты формируют белый осадок.
Количество мочи зависит от водного режима. Здоровые взрослые люди в течение суток выделяют с мочой от 0,6 до 2,0 л жидкости. При этом отношение дневного объема выводимой мочи к ночному соответствует 3-4:1. Увеличение ночного диуреза называется никтурия. Наблюдается при гипертрофии простаты, диабетенарушении сердечно-сосудистой системы, тяжелые поражения почек. Состояние, при котором суточный объем (диурез) мочи превышает 2 л, называется полиурией. Отмечается при обильном питье, сахарном и несахарном диабете, при нефросклерозе, эндокринных нарушениях мочеобразования.
При выделении за сутки менее 500 мл мочи констатируют олигурию. Олигурия подразделяется на преренальную, ренальную и постренальную. Преренальная олигурия обусловлена недостаточностью кровенаполнения почек (уменьшение объема циркулируещей крови, падение тонуса сосудов, кровотечение, стеноз почечных сосудов). Почечная олигурия обусловлена нарушением фильтрации мочи, вследствие воспалительных изменений в клубочках почек (гломерулонефрит, вирусные и бактериальные инфекции, тубулоинтерстициальный некроз). Постренальная олигурия связана с обтурацией мочевыделительной системы камнем, кровяным сгустком, опухолью.
Полное прекращение выделения мочи называется анурией (физиологическая у новорожденных в течение первых часов жизни). Наблюдается при тяжелом поражении почек, острой почечной недостаточности, пргрессирующем перитоните, отравлениях.
Дизурия расстройство мочеиспускания, может быть поллакиурия – частое мочеиспускание, оллакиурия – редкое мочеиспускание и энурез – недержание мочи.
Относительная плотность мочи зависит от концентрационной способности почек. Кроме того, плотность мочи зависит от глюкозурии и протеинурии. Диапазон относительной плотности в течение суток должен быть от 1,003 до 1,028. Причину нарушений концентрационной функции почек лучше анализировать в динамическом наблюдении. Для этого используется проба Зимницкого. Суть пробы Зимницкого заключается в измерении относительной плотности моче в 8-ми отдельных порциях, собранных в течение суток через каждые три часа (6, 9, 12, 15, 18, 21, 0 и 3 часа). Чем больше разница между максимальным и минимальным значением относительной плотности, тем выше функциональная способность почек. В норме она должна быть не менее 0,007. В первую очередь эта проба более чувствительна к выявлению патологии канальцев. Гипостенурия – нарушение процесса концентрирования первичного ультрафильтрата при сохранении разведения мочи.
Реакция мочи в норме является показателем характера питания. При смешанном питании характерно преобладание кислых продуктов в пище, поэтому рН мочи 5,5-6,5. Для вегетарианцев характерна нейтральная или щелочная реакция. При смешанном питании щелочная моча может быть признаком инфицирования мочевых путей, поскольку микрофлора преобразует мочевину (компонент мочи) в аммоний, защелачивая мочу. В клинической практике определение рН важно в связи с тем, что одни препараты, используемые в нефрологии, эффективно действуют в кислой среде, другие - в щелочной среде.
Глюкозурия расценивается как явление патологическое. Глюкоза свободно фильтрауется почечными клубочками и в норме полностью реабсорбируется клетками проксимальных канальцев. Перенос глюкозы из просвета канальца через мембрану щеточной каемки происходит с помощью переносчика. Максимальное количество молекул глюкозы, реабсорбируемых из канальцевой жидкости в кровь, зависит от числа переносчиков глюкозы. Если количество реабсорбируемой глюкозы превышает возможности переносчиков, то глюкоза появляется в моче. Максимальная концентрация глюкозы в крови, при которой не наблюдается глюкозурии, называется почечным порогом. В норме почечный порог составляет 10 ммоль/л глюкозы в крови. С возрастом почечный порог для глюкозы повышается. Количество переносчиков глюкозы снижается при хронических заболеваниях почек, при гипертонической болезни, при диабетической нефропатии. Это означает, что при этих заболеваниях глюкозурия может появляться при концентрации глюкозы в крови менее пороговой (<10 ммоль/л).
Кетонурия – обнаружение ацетона, ацетоуксусной, бета-оксимасляной кислоты в моче. Свидетельствует о нарушении обмена углеводов, белков и жиров, которое приводит к увелечению кетогенеза (сахарный диабет, голодание, лихорадка при инфекционном процессе, отравленияалкогольная интоксикация, повышенный катаболизм). Кетонурия не является непосредственным поражением почек.
Протеинурия (обнаружение белка в моче) является важным и практически значимым симптомом поражения почек и мочевыводящих путей. Проникновение белка через почечный фильтр в просвет канальцев почек зависит от состояния базальной мембраны капсулы клубочка, формы и размеров белковой молекулы, количества белка в плазме. В норме через почечный фильтр проходят белки с молекулярной массой до 70 кД (альбумин, легкие цепи иммуноглобулинов, многие ферменты). В норме концентрация белка в разовой порции не должна превышать 0,033 г/л. В суточной допускается до 0,15 г/сутки. В моче здоровых людей обнаружено более двухсот белков, имеющих различное происхождение. Одни фильтруются из плазмы крови, другие имеют почечное происхождение или секретируются эпителием мочевого тракта.
Протенурия может быть функциональной и органической. Функциональная протеинурия связана с гемодинамическим стрессом и может наблюдаться на фоне лихорадки, эмоциональном стрессе, после физической нагрузки или охлаждения. Увеличение экскреции белка с мочой при смене положения тела (из горизонтального в вертикальное), наблюдаемое чаще у подростков, называется ортостатической протеинурией.
Органическая (патологическая) протеинурия может быть преренальной, ренальной и постренальной. Преренальная (перегрузочная) не связана с поражением почек. Она возникает в результате заболеваний, сопровождающихся повышенным синтезом низкомолекулярных белков (миеломная болезнь). Ренальная протеинурия обусловлена поражением клубочков и канальцев почек. При этом страдает процесс фильтрации (гломерулярный тип протеинурии) или нарушается реабсорбция белков в проксимальных канальцах (тубулярный тип протеинурии). При повреждении клубочкового барьера (гломерулярный тип протеинурии) выделяют высокоселективную, селективную и неселективную протеинурию. При высокоселективном типе в моче обнаруживаются низкомолекулярные белки до 70 кД (альбумины). При селективной протеинурии в моче выявляют белки до 150 кД. При неселективной протеинурии в моче обнаруживаются белки с высокой молекулярной массой 830-930 кД (иммуноглобулины). Постренальная протеинурия обусловлена попаданием воспалительного экссудата, богатого белком, в мочу (цистит, простатит).
При микроскопическом исследовании мочевого осадка различают органическую и неорганическую часть.
Органическая часть представлена эритроцитами, лейкоцитами, цилиндрами и эпителием. Эритроцитурия – патологический мочевой синдром.
Причины эритроцитурии
Лейкоцитурия. У здоровогочеловека при микроскопии осадка мочи обнаруживаются единичные лейкоциты в каждом поле зрения. Лейкоцитурия бывает, как… Цилиндрурия – цилиндры в моче. Цилиндры представляют собой слепки почечных… В целях диагностики латентных форм воспалительных заболеваний почек и мочевых путей в нефрологической практике широко…ВОПРОСЫ ДЛЯ ОБСУЖДЕНИЯ
1. Фильтрация, реабсорбция, клиренс, почечный порог. 2. Нормальные уровни физиологических компонентов мочи: мочевина, кретинин,… 3. Основные заболевания почек:САМОСТОЯТЕЛЬНАЯ РАБОТА СТУДЕНТОВ
2. Расшифровать общий анализ мочи при различных патологических состояниях организма человека. Дать заключение с внесением в протокол. 3. Записать тесты на определение функции почек используемые в клинической…Тема занятия: Обмен жидкостей в организме. Отеки. Обмен натрия. Гипо- и гипернатриемия. Методы диагностики водно-электролитного баланса.
Цель занятия:Изучитьосновы водно-солевого обмена. Иметь понятие о положительном и отрицательном водном балансе. Освоить механизмы развития отеков… Знать: - положительный и отрицательный водный баланс;Показатели осмолярности в норме
Определение осмолярности является сложным лабораторным исследованием. Оно позволяет вовремя выявить симптомы таких нарушений, как гипоосмолярность,… Гиперосмолярность вызывается повышением осмолярности плазмы крови выше 350… Кроме того, определение осмолярности помогает выявлять и целенаправленно лечить гиперосмолярные коматозные состояния и…Системы регуляции водно-солевого обмена обеспечивают поддержание общей концентрации электролитов (натрия, калия, кальция и др.) и ионного состава внутриклеточной и внеклеточной жидкости на одном и том же уровне. В плазме крови человека концентрация ионов поддерживается с высокой степенью постоянства и составляет (в ммоль/л): натрия – 136–145, калия – 3,5–5,1, кальция – 2,3–2,75 (в т.ч. ионизированного, не связанного с белками – 1,12–1,32). По сравнению с плазмой крови и межклеточной жидкостью клетки отличаются более высоким содержанием ионов калия и низкой концентрацией ионов натрия.
Натрий - основной ион внеклеточной жидкости, в ней содержится 96 % от общего количества натрия в организме (90–100 г). Нормальная концентрация Na в плазме крови – 136–145 ммоль/л; она поддерживается с высокой точностью, поскольку определяет осмолярность плазмы и водный обмен. Обычное потребление человеком NaCl составляет 8–15 г/сут, хотя реальная потребность организма в натрии несколько меньше. Избыток Na выводится через почки и потовые железы; потеря натрия через кишечник может наблюдаться при диареях.
Важнейшие биологические функции натрия:
1. Главная роль в поддержании осмолярности плазмы крови и внеклеточной жидкости в целом.
2. Участие (совместно с калием) в возникновении электрохимического потенциала на плазматических мембранах клеток, обеспечение их возбудимости и мембранного транспорта.
3. Стабилизация молекул белков и ферментов, обеспечение протекания ряда ферментативных реакций
Определение концентрации натрия в плазме является первостепенной задачей при диагностике нарушений водного баланса в организме. Осмолярность плазмы напрямую связана с уровнем натрия, поскольку натрий и связанные с ним ионы (обычно хлор) представляют около 90% веществ, растворенных во внеклеточной жидкости. Поэтому натрий справедливо считается индикатором осмолярности при различных состояниях. Снижение его концентрации в плазме всего на несколько миллиэквивалентов (ниже 142 мэкв/л) свидетельствует о таком нарушении, как гипонатриемия. Превышение нормальных показателей называют гипернатриемией.
Гипонатриемия – уменьшение концентрации натрия ниже 134 ммоль/л. Характеризуется проявлением аппатиии, потерей аппетита, тошнотой, рвотой, нарушением рефлексов, тахикардией, анурией, гипотензией с потерей сознания, психозами. Снижение концентрации натрия в плазме может возникать по двум причинам: потери натрия из внеклеточной жидкости или избытка воды во внеклеточной жидкости.
Абсолютная гипонатриемиявозникает при уменьшенном поступлении натрия в организм (например, у больных с сердечной недостаточностью, вынужденных соблюдать бессолевую диету) и потере натрия через ЖКТ, с мочой, кровью, большим количеством удаляемой асцитрической и отечной жидкости, злоупотребление диуретиками, первичный и вторичный гипокортицизм, хроническая сердечная недостаточность, цирроз печени, печеночная недостаточность, нефротический синдром, нарушение питания. Потеря натрия обычно связана с гипоосмолярной дегидратацией вследствие снижения объема внеклеточной жидкости, что встречается при диарее и рвоте. Злоупотребление диуретиками, которые снижают натрий-сберегающую способность почек, а также болезнь Аддисона, при которой вследствие снижения выработки гормона альдостерона нарушается способность почек реабсорбировать натрий, могут также приводить к умеренной гипонатриемии.
Относительная гипонатриемиясвязана с избыточной задержкой или поступлением жидкости в организме, что приводит к разбавлению внеклеточной жидкости и снижению концентрации натрия. Гипонатриемия чаще всего формируется при введении в организм жидкостей, не содержащих электролиты (например, при инфузии изотонического раствора глюкозы), что способствует разведению плазмы. К ней приводит и избыточная продукция антидиуретического гормона, которая способствует реабсорбции большего количества воды в собирательных трубочках почки, приводя к гипергидратации и гипонатриемии. Синдром неадекватной секреции антидиуретического гормона отмечается не только при поражении ЦНС, но также у больных раком легкого, поджелудочной железы, воспалительными заболеваниями легких.
Гипернатриемия– увеличение концентрации ионов натрия выше 145 ммоль/л. Сопровождается тяжелым общим состоянием больных, повышением температуры тела, тахикардией.Увеличение концентрации натрия в плазме, что увеличивает ее осмолярность, может возникать либо в результате потери внеклеточной жидкостью воды, либо при попадании в нее избытка ионов Na+.
Абсолютная гипернатриемия – может быть обусловлена задержкой ионов электролита в плазме больных с повышенной фукцией коры надпочечников (при гиперальдостеронизме, синдроме или болезни Иценко-Кушинга), усилением выделения натрия из тканей в плазму в процессе активации метаболизма у лиц, стадающих гнойно-септическими заболеваниями, судорогами, лихорадкой; при избыточной терапии солевыми растворами.Гипернатриемия может также возникать при увеличении поступления натрия во внеклеточную жидкость. Это часто приводит к гиперосмолярной дегидратации, т.к. избыточное содержание NaCl во внеклеточной жидкости обычно приводит к небольшой задержке воды почками. Например, гиперсекреция гормона альдостерона, вызывающего задержку натрия, может вызвать умеренную гипернатриемию и гипергидратацию. Умеренность гипернатриемии объясняется тем, что увеличение продукции альдостерона приводит к усиленной реабсорбции не только натрия, но и воды в почках.
Относительная гипернатриемия– вызывается повышенной потерей воды через кожу (профузный пот), легкие (длительная гипервентиляция), ЖКТ (тяжелая рвота или понос различной этиологии), почки (полиуретические состояния, характерные для несахарного диабета, диабетического ацидоза).
Когда первопричиной является потеря воды, возникает гиперосмолярная дегидратация. Такое состояние встречается при невозможности организма секретировать антидиуретический гормон (АДГ), который необходим почкам для реабсорбции воды. Снижение продукции АДГ способствует выделению большого количества разбавленной мочи (несахарному диабету), что, в свою очередь, приводит к обезвоживанию и возрастанию концентрации NaCl во внеклеточной жидкости. При некоторых заболеваниях почки становятся невосприимчивыми к АДГ, что приводит к нефрогенному варианту несахарного диабета. Более частой причиной гипернатриемии, связанной с уменьшением объема внеклеточной жидкости, является дегидратация (обезвоживание), когда потери воды превышают ее поступление. Примером подобного состояния может служить значительное потоотделение при тяжелых физических нагрузках.
Таким образом, при анализе содержания натрия в плазме и выборе правильного лечения нарушений в первую очередь следует установить причину: вызваны ли данные нарушения потерей (избытком) натрия или потерей (избытком) воды в организме.
Специализированные системы регуляции водно-минерального обмена:
-нервная регуляция через центральную нервную систему;
-органная регуляция через изменение функционирования почек, в которых активно идут процессы фильтрации и реабсорбции воды и ионов, а также кишечника, слюнных желез, легких и кожи с потовыми железами;
-гормональная регуляция.
Водно-солевой обмен регулируется антидиуретической и антинатрийуретической системами, поддерживающими, соответственно уровень воды и солей, прежде всего ионов натрия, в организме. Эфферентное звено этих систем представлено расположенными в сосудистой сети осмо- и волюморецепторами, большинство из которых размещено в предсердиях, устьях легочных вен и некоторых артериях.
Центральными органами регуляции являются нейросекреторные супраоптические и паравентрикулярные ядра гипоталамуса, контролирующие синтез антидиуретического гормона (вазопрессина).
Гормон через усиление реабсорбции воды в почечных канальцах снижает диурез. С вазопрессином связано и чувство жажды, требующее приема новых порций жидкости. При избытке воды синтез гормона подавляется с усилением диуреза.
Задержка воды в организме осуществляется также за счет задержки натрия. Процесс регулируется альдостероном коркового вещества надпочечников, синтез которого находится под контролем соответствующих ядер гипоталамуса, передней части среднего мозга и эпифиза. Водно-солевой обмен со средой осуществляется не только через почки, но и кожу, легкие, желудочно-кишечный тракт.
Важнейшими гормонами, влияющими на обмен воды и натрия, являются:
-антидиуретический гормон гипофиза (АДГ, или вазопрессин) – повышает реабсорбцию воды в дистальных канальцах почек, "разбавляя" кровь, снижая ее осмолярность и увеличивая объем;
-альдостерон - гормон коры надпочечников - увеличивает почечную реабсорбцию натрия и вместе с ним воды; повышает осмолярность плазмы крови и увеличивает ее циркулирующий объем;
-предсердный и мозговой натрийуретический фактор (НУФ) – выделяется в ответ на растяжение предсердий и сосудов кровью; служит антагонистом альдостерона, увеличивая потери натрия и воды через почки и снижая циркулирующий объем крови.
Содержание натрия и организме регулируется в основном почками под контролем ц.н.с. через специфические натриорецепторы. реагирующие на изменение содержания натрия в жидкостях тела, а также волюморецепторы и осморецепторы, реагирующие на изменение объема циркулирующей жидкости и осмотического давления внеклеточной жидкости соответственно. Натриевый баланс в организме контролируется и ренин-ангиотензинной системой, альдостероном, натрийуретическими факторами. При уменьшении содержания воды в организме и повышении осмотического давления крови усиливается секреция вазопрессина (антидиуретического гормона), который вызывает увеличение обратного всасывания воды в почечных канальцах. Увеличение задержки натрия почками вызывает альдостерон, а усиление выведения натрия – натрийуретические гормоны, или натрийуретические факторы. К ним относятся атриопептиды, синтезирующиеся в предсердиях и обладающие диуретическим, натрийуретическим действием, а также некоторые простагландины, уабаинподобное вещество, образующееся в головном мозге, и др.
Нарушения водно-солевого обмена влекут за собой нарушения в метаболических путях, что способствует снижению резервов компенсаторно-приспособительных процессов. Тем самым понижается уровень здоровья человека в целом, модифицируется и усложняется течение заболеваний.
ВОПРОСЫ ДЛЯ ОБСУЖДЕНИЯ
2. Отрицательный водный баланс. Положительный водный баланс. 3. Методы оценки водного баланса. 4. Осмотическое и онкотическое давление. Определение осмолярности.САМОСТОЯТЕЛЬНАЯ РАБОТА СТУДЕНТОВ
2. Расшифровать анализ водно-электролитного баланса при различных патологических состояниях организма человека. Дать заключение с внесением в… 3. Записать тесты на определение водно-солевого обмена, используемые в… Тема занятия: Биологическая роль калия, кальция, фосфора. Клиническое значение дисэлектролитемии. Методы определения…Гипер-и гипокалиемия, клинические проявления
Баланс калия в организме складывается из равновесия между его поступлением, депонированием и выведением. Поступление калия в клетку находится под… Почки являются неотъемлемой и важнейшей функциональной единицей в системе… Определение концентрации калия в плазме (сыворотке) крови позволяет оценить глубину расстройств калиевого обмена,…Причины гипокалиемии
Вследствие дефицита калия поражаются все мышцы: поперечнополосатые, гладкие и сердечная мышца, а также почки. Эти изменения определяют основную… Концентрация сывороточного калия малоинформативна, так как 98 % калия… Повышенный уровень ионов калия в плазме может иметь место, несмотря на дефицит его в клетке при компенсированном…Кальций, гипер- и гипокальциемия у детей и взрослых
Главная роль в метаболизме кальция в организме человека принадлежит костной ткани. В костях кальций представлен фосфатами – Са3(РО4)2 (85%),… Регуляция обмена кальция между вне- и внутриклеточной жидкостью осуществляется… В плазме крови содержатся фракции связанного с белком (недиффундирующего) кальция (0,9 ммоль/л) и диффундирующего:…Фосфор, кислоторастворимая и кислотонерастворимая фракции. Гипер и гипофосфатемия у детей и взрослых
1. Кислоторастворимый фосфор (остающийся в фильтрате после осаждения белков плазмы трихлоруксусной кислотой): а) неорганический фосфор (свободный); б) органические соединения фосфора (эфиросвязанный фосфор, пирофосфаты: АТФ, АДФ и др., гексозофосфаты, пентозофосфаты…Норма фосфора в крови
В организм человека фосфор поступает с растительной и животной пищей в виде фосфолипидов, фосфопротеинов и фосфатов. Всасывание 70–90% фосфора… В крови фосфор находится в виде четырех соединений: неорганического фосфата,… Концентрацию фосфора в сыворотке крови рекомендуется определять натощак: богатая фосфором пища повышает его, а…Гомеостаз кальция и фосфата
Методы определения показателей минерального обмена
Определение калия
Пламенная фотометрия представляет собой один из видов эмиссионного спектрального анализа, основанного на фотометрировании излучения элементов в… Ионоселективные анализаторы выгодно отличаются от пламенных фотометров…Определение кальция
Для измерения содержания ионизированного кальция крови используются ионоселективные анализаторы. Самым точными чувствительным методом измерения содержания общего кальция в биологических жидкостях считается атомнаяабсорбционная спектрофотометрия. Этот метод обладает высокой специфичностью и является одним из видов спектрального анализа.
Биохимические методы определения фосфора
Все колориметрические методы измерения концентрации неорганического фосфора основаны на образовании фосфорно-молибденовой кислоты, количество…ВОПРОСЫ ДЛЯ ОБСУЖДЕНИЯ
2. Гипер- и гипокалиемия, клинические проявления, диагностика. 3. Метаболизм кальция. Регуляция обмена кальция. 4. Гипер- и гипокальциемия у детей и взрослых.САМОСТОЯТЕЛЬНАЯ РАБОТА СТУДЕНТОВ
1. Записать протокол практического занятия с указанием ее цели и задачи, схемы и методики определения минерального обмена.
2. Расшифровать анализ электролитного состава крови и мочи при различных патологических состояниях организма человека. Дать заключение с внесением в протокол.
3. Записать тесты на определение минерального обмена, используемые в клинической практике. Дать заключение с внесением в протокол.
Тема занятия: Кислотно-щелочной баланс организма. Формы нарушения кислотно-щелочного баланса. Клинико-диагностическое значение изменений показателей КЩС. Диагностика неотложных состояний в анестезиологии и реаниматологии.
Одним из условий существования живого организма является постоянство его внутренней среды. Это постоянство выдерживается по целому ряду параметров, в том числе и по концентрации водородных ионов (рН). Кислотно-основное равновесие – это состояние, которое обеспечивается физиологическими и физико-химическими процессами, составляющими функционально единую систему стабилизации концентрации ионов Н+. Нормальные величины концентрации ионов Н+ около 40 нмоль/л, что в 106 раз меньше, чем концентрация многих других веществ (глюкоза, липиды, минеральные вещества). Для поддержания рН артериальной крови в нормальных границах (т. е. для стабилизации кислотно-основного состояния организма) служат буферные системы (бикарбонатная, фосфатная, гемоглобиновая и др.). Наиболее емкой системой является бикарбонатная, представляющая собой смесь слабой угольной кислоты (Н2СО3) и ее однозамещенных солей – бикарбонатов. Буферные системы обладают свойством противостоять изменениям рН при добавлении кислот или оснований. Снижение NaНСОз/Н2СО3 ведет к ацидозу, увеличение – к алкалозу. При этом рН остается в пределах нормальных значений (от 7,35 до 7,45). При снижении рН артериальной крови ниже 7,35 говорят об ацидемии, при увеличении свыше 7,45 – об алкалемии.
Цель занятия:Знать основы кислотно-щелочного баланса организма. Иметь понятие о роли буферных и физиологических систем в поддержании кислотно-щелочного равновесия. Знать формы нарушения КЩС. Иметь представление о методах диагностики нарушений кислотно-щелочного равновесия и неотложных состояний в реаниматологии и анестезиологии.
Знать:
- кислотно-щелочной баланс организма;
- механизм работы буферной системы гемоглобина;
- физиологические системы: роль легких, почек, печени в поддержании кислотно-щелочного равновесия;
- формы нарушения кислотно-щелочного баланса, алкалоз и ацидоз: респираторный, метаболический, компенсированный, декомпенсированный;
- клинико-диагностическое значение изменений показателей КЩС;
- неотложные состояния в анестезиологии и реаниматологии, общеклинические анализы, экспресс-диагностику.
Уметь:
- оценить нарушения кислотно-щелочного баланса организма;
- провести диагностическую оценку неотложных состояний.
Кислотно-основное равновесие – это состояние, которое обеспечивается физиологическими и физико-химическими процессами, составляющими функционально единую систему стабилизации концентрации ионов Н+. Метаболическая активность клеток, функция ферментов и стабильность мембран зависит от рН, который является главным показателем КОС. Большая часть ферментативных реакций в организме протекает в узком диапазоне pH (7,30 – 7,50). Сдвиги концентрации ионов Н+ приводят к изменению активности внутриклеточных ферментов даже в пределах физиологических значений. Например, ферменты глюконеогенеза более активны при закислении цитоплазмы, что актуально при голодании или мышечной нагрузке, ферменты гликолиза - при обычных рН.
При нормальном метаболизме за сутки в организме образуется примерно 15000 ммоль ионов водорода (15000000000 нмоль). При норме около 100 нмоль/л во внеклеточной жидкости.
КОС характеризуют концентрацией водородных ионов, которые обозначаются символом рН. Величина рН – это десятичный логарифм концентрации ионов водорода в растворе, взятый с обратным знаком.
Нормальные показатели кислотно-щелочного равновесия
При изменении концентрации ионов Н+ в крови активируется компенсационная деятельность двух крупных систем организма: 1. Система химической компенсации · действие внеклеточных и внутриклеточных буферных систем,Основные показатели КОС крови
Несостоятельность компенсаторных механизмов организма в предотвращении сдвигов концентрации водородных ионов приводит к различным нарушениям… Ацидоз – изменение КОС, при котором в крови появляется абсолютный или…Механизмы компенсации нарушений кислотно-основного равновесия
Изменения отношения ВНСО3 / Н2СО3 могут происходить как за счет числителя, так и за счет знаменателя. В первом случае сдвиги носят метаболический… Если ВНСОз первично увеличен, компенсация развивается по пути увеличения Н2СО3… Если метаболические процессы приводят к увеличению содержания кислых продуктов обмена в крови, развивается…ВОПРОСЫ ДЛЯ ОБСУЖДЕНИЯ
2. Механизм работы буферной системы гемоглобина. 3. Роль физиологических систем в поддержании кислотно-щелочного равновесия … a. легкие;САМОСТОЯТЕЛЬНАЯ РАБОТА СТУДЕНТОВ
1. Записать протокол практического занятия с указанием ее цели и задачи, схемы и методики определения кислотно-щелочного баланса организма.
2. Расшифровать анализ кислотно-щелочного баланса при различных патологических состояниях организма человека. Дать заключение с внесением в протокол.
3. Записать тесты на определение кислотно-щелочного баланса, используемые в клинической практике. Дать заключение с внесением в протокол.
– Конец работы –
Используемые теги: установления, чины, болезни, генетических, инфекционных, заболеваниях, отравлениях0.111
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Установления причины болезни при генетических, инфекционных заболеваниях, отравлениях
Что будем делать с полученным материалом:
Если этот материал оказался полезным для Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов