рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Химия
- /
- До семінарських занять з предмету: Хімія
Реферат Курсовая Конспект
До семінарських занять з предмету: Хімія
До семінарських занять з предмету: Хімія - раздел Химия, ...

МІНІСТЕРСТВО ОСВІТИ І НАУКИ, МОЛОДІ ТА СПОРТУ УКРАЇНИ
ОДЕСЬКИЙ ТЕХНІЧНИЙ КОЛЕДЖ
ОДЕСЬКОЇ НАЦІОНАЛЬНОЇ АКАДЕМІЇ ХАРЧОВИХ ТЕХНОЛОГІЙ
Методичні вказівки та запитання
Для підготовки студентів І курсу
до семінарських занять з предмету:
“Хімія”
М. Одеса - 2011
Автор: Дьякова Т.В., викладач коледжу
Відповідальний за випуск: Стрельнікова І.А., методист коледжу
Оператор: Кутіян К.Б.
МІНІСТЕРСТВО ОСВІТИ І НАУКИ, МОЛОДІ ТА СПОРТУ УКРАЇНИ
ОДЕСЬКИЙ ТЕХНІЧНИЙ КОЛЕДЖ ОНАХТ
ЗАТВЕРДЖУЮ
заст. директора з НР
____________ В.І.Уманська
"___" ___________20__ р.
Методичні вказівки та запитання
Для підготовки студентів І курсу
до семінарських занять з предмету:
“Хімія”
Викладач Дьякова Т.В.
РОЗГЛЯНУТО
предметною комісією
 протокол №
протокол №
від “ ___ ” ________ 20__ р.
Голова комісії Швець Л. І.

2011р.
ВСТУП
При вивченні хімії студенти І курсу зустрічаються з проблемою при підготовці до семінарських занятть в зв’язку з переходом до лекціонно-семінарського методу навчання. Семінарські заняття включають об’ємні теми, які частично вивчаються студентами самостійно.
Методичні вказівки містять основну інформацію з вивчаємих тем, що дає можливість студентам І курсу більш досконало підготуватися до семінарського заняття, а перелік питань дає можливість студентам перевірити свої знання з вивчаємої теми.
Методичні вказівки також містять ряд запитань для розвитку логічного мислення студентів та вміння розв’язувати проблемні питання.
Семінар № 1.
Тема: Найважливіші класи неорганічних сполук. Періодичний закон і періодична система Д.І.Менделеєва. Мета: Закріпити знання студентів про класифікацію неорганічних сполук.… Література: 1. М.В. Горский “Обученые основам общей химии” М. Просвещение 1991.Кислоти.Число атомів водню, які мають властивість заміщати метали з утворенням солей, визначають основність кислоти. Розрізняють кислоти одноосновні (наприклад НСІ), двухосновні (H2SO4), трьохосновні (H3PO4).
По хімічному складу кислоти поділяються на безкисневі (НСІ) і кисневмісні (H2SO4).
Більшість кислотних оксидів утворюють шляхом приєднання води. Кислотні оксиди називають ангидридами кислот. Молекули деяких ангидридів можуть приєднувати різні кількості молекул води. При цьому утворюються метакислоти, які містять найменшу кількість води, і ортокислоти, які містять найбільшу кількість води. Наприклад:
P2O5 + H2O = 2HPO3 – метафосфорна кислота
P2O5 + 2H2O = H4P2O7– пирофосфорна кислота
P2O5 + 3H2O = 2H3PO4 – ортофосфорна кислота
Основи.В залежності від числа гідроксильних груп основи бувають однокислотні (КОН, NaOH) і багатокислотні (Са(ОН)2). Основи, які розчиняюиться в воді, називаються лугами. До них відносяться основи, які утворені лужними або лужноземельними металами, і гідроксид амонія.
Амфотерні гідроксиди. Гідрати амфотерних оксидів, так як і самі оксиди, проявляють амфотерні властивості. З кислотами вони взаємодіють як основи:
Zn(OH)2 + H2SO4 = ZnSO4 + 2H2O
з основами – як кислоти: H2ZnO2 + 2NaOH = Na2ZnO2 + 2H2O
Солі.Солі поділяють на середні (наприклад, Na2SO4), кислі (NaHSO4) і основні (NiOHNO3).
По міжнародній номенклатурі назву середніх і кислих солей отримують від назви кислот і металів, які їх утворюють. Так: CuSO4 – сульфат міді, NaHSO3 – гідросульфіт натрія, NaH2PO4 – дигідрофосфат натрія.
Основні солі називають гідроксосолями, наприклад: NiOHNO3 – нітрат гідроксонікеля, AIOHSO4 - сульфат гідроксоалюмінія.
Електронна будова атомів. Атомні радіуси. Утворення іонів.
Ядро атомів складається із протонів і нетронів. Число протонів в ядрі атома дорівнює порядковому номеру елемента в періодичній системі і дорівнює числу електронів в атомі. Число нейтронів в ядрі атома дорівнює різниці між відносною атомною масою хімічного елемента і числом протонів. Так як заряд протона по абсолютній величині дорівнює заряду електрона, то атом кожного хімічного елемента зображує собою складну електронейтральну систему, яка складається із позитивно заряженого ядра і електронної оболочки з числом електронів, які дорівнюють числу протонів в ядрі.
Електрони в атомі володіють різною енергією і розміщаються на енергетичних рівнях і підрівнях в залежності з принципом Паулі, правилом Хунда і правилом Клечковського.
Принцип Паулі: в атомі не може бути двух електронів з однаковими значеннями всіх чотирьох квантових чисел. Квантові числа позначаються буквами: n, l, m, s, де n – головне квантове число, яке характеризує запас енергії певного електрона, розмір його електронної хмари; l – орбітальне квантове число, яке характеризує енергетичний стан електрона, форму електронної хмари; m – магнітне квантове число, визначає орієнтацію атомних орбіталів просторі відносно зовнішнього магнітного або електричного поля (m залежить від – l, змінюється від – l до l; кожному заченню l відповідає 2l + 1стану електрона); s – спине квантове число, яке вказує напрям руху електрона біля його осі (приймають рівним +1/2 і –1/2).
Число електронів на зовнішньому енергетичному рівні в атомі будь-якого елемента не перевищує вісім. В межах підрівня електрони заповняють максимальне число орбіталей – правило Хунда.
Періодична система складається із семи періодів і восьми груп.
Запитання до семінару
2. Які оксиди називаються основними, кислотними? 3. Які оксиди називаються амфотерними? Наведіть приклади амфотерних… 4. Як, користуючись періодичною системою елементів, визначити характер оксида, гідроксида?Запитання до семінару
2. Напишіть формулу калій пероксиду. 3. Яке має співвідношення водень з киснем у суміші “гримучий газ”? 4. Назві та напишіть тип кристалічної гратки кисню.Запитання до семінару
2. Які елементи належать до металів? Що характерне для їх електронних конфігурацій? Метали у періодичній системі. 3. Які у металів спільні характерні ознаки (фізичні властивості) та чим вони… 4. Що таке сплави? Як вони утворюються та як їх вивчають?Запитання до семінару
2. Назвіть основні положення теорії хімічної будови Бутлерова. 3. Поняття про яке явище виходить із положень теорії хімічної будови… 4. Чим пояснюється настільки велика кількість різноманітних вуглеводнів?Запитання до семінару
2. Наведіть емперичні та умовно структурні формули і назви можливих ізомерів: а)пентину; б)пентену; в)пентадієну. 3. Складіть структурну формулу та визначте масу 1 м3 вуглеводню ряду СnH2n,… 4. Як можна відрізнити один від одного гази: бутан, бутен і бутадієн? Наведіть хід міркувань та рівняння реакцій.Спирти і феноли - це органічні речовини, молекули яких містять гідроксильні групи —ОН, сполучені з вуглеводневими радикалами. Загальна назва спиртів і фенолів - гідроксильні сполуки.
Залежно від числа гідроксильних груп, що містяться в молекулі, розрізняють одноатомні, двохатомні, трьохатомні спирти :

Спирти поділяють також на первинні, в яких гідроксильна група сполучена з первинним вуглецевим атомом, вторинні- група —ОН приєднана до вторинного атома вуглецю і третинні - група —ОН знаходиться біля третинного атому вуглецю. Приклади таких спиртів:

До насичених одноатомних спиртів належать аліфатичні спирти, молекули яких містять одну гідроксильну групу, сполучену з алкільним радикалом.
Члени гомологічного ряду насичених одноатомних спиртів мають загальну формулу СnН2n+1ОН, де n = 1, 2, 3, 4. Першими членами цього ряду є СН3ОН — метанол, С2Н5ОH — етанол, С3Н7ОН — пропанол, С4Н9ОН — бутанол.
Хімічні властивості спиртів зумовлені переважно наявністю гідроксильної групи в молекулі.
Метанол, або метиловий спирт, СН3ОН - безбарвна рідина з характерним запахом спиртів. Дуже отруйний.
Метанол — це важливий продукт хімічної промисловості. У великих кількостях його переробляють на формальдегід. З нього добувають і інші органічні речовини, наприклад ефіри кислот.
Етанол, або етиловий спирт, С2Н5ОН - безбарвна рідина з характерним запахом. Тривіальна назва етанолу - винний спирт.
Етанол утворюється під час бродіння продуктів, що містять крохмаль і цукристі речовини (зерна, фруктів, овочів). Бродіння - складний процес. Сумарну реакцію, яка відбувається під час бродіння поширеної цукристої речовини — глюкози С6Н12O6, можна виразити рівнянням:
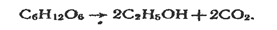
Багатоатомні спирти містять у молекулі кілька гідроксильних груп.
Хімічні властивості багатоатомних спиртів багато в чому подібні до властивостей одноатомних спиртів. При цьому в реакціях може брати участь як одна, так і дві, і більше гідроксильних груп.
Ф е н о л и — це гідроксильні сполуки, в яких гідроксильна група сполучена безпосередньо з атомом вуглецю бензольного ядра. Найпростішим представником фенолів є гідроксибензол, або фенол, який має одну гідроксильну групу в бензольному ядрі:
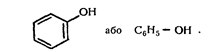
Фенол - це безбарвна кристалічна речовина з характерним запахом, температура плавлення становить 40,9°С. На повітрі фенол частково окислюється, внаслідок чого набуває рожевого забарвлення. При потраплянні на шкіру викликає подразнення. Тривіальна назва фенолу - карболова кислота.
Гліцерин.Єдиний практично важливий представник трьохатомного спирту. Сиропоподібна солодка рідина, без кольору, добре розчинна у воді. Водні розчини гліцерину замерзають при низькій температурі.
КсилітСН2ОН(СНОН)3СН2ОН та сорбітСН2ОН(СНОН)4СН2ОН. Добуваються відновленням відповідних моносахаридів: перший - ксилози, другий - глюкози. Сорбіт широко розповсюджений у природі, входить до складу багатьох плодів та ягід. Ксиліт та сорбіт вживають хворі на діабет замість цукру, для виготовлення кондитерських виробів, напоїв, зубних паст. Сорбіт - перший напівпродукт при виготовленні аскорбінової кислоти.
Запитання до семінару
2. Поясніть як при перекриванні відповідних електронних хмар утворюються хімічні зв’язки в молекулі води і гідроксильній групі спиртів. 3. Один із атомів водню в молекулах одноатомних спиртів більш рухомий.… 4. Які види ізомерії характерні для спиртів?Жири є різновидом класу природних органічних сполук, які називаються ліпідами. За хімічною будовою жири – складні ефіри гліцеріну і вищих карбонових кислот. Їх називають також тригліцеридами.
Тригліцериди насичених кислот за звичайних умов є твердими речовинами, ненасичених кислот – оліїстими рідинами. У воді розчиняються мало.
Важливою хімічною властивістю жирів є їх здатність гідролізуватися, тобто всупати в реакцію омилення. Омилення жирів відбувається необоротно при наявності лугів, при цьому утворюються гліцерин і сіль кислоти.
Жири широко поширені в природі, вони є складовою частиною рослинних і тваринних організмів. Тригліцериди можна добути за реакцією етерифікації, проте в промисловості їх виділяють переважно з природних речовин. У тваринних жирах переважають тригліцериди насичених кислот, тому ці жири за звичайних умов є твердими речовинами (наприклад, вершкове масло, сало). У рослинних жирах переважають тригліцериди ненасичених кислот, ці жири є рідинами (соняшникова олія, маслинова олія). Такі жири називаються оліями. У промисловості рідкі рослинні олії часто переробляють на тверді жири, які за властивостями нагадують тваринні.
Запитання до семінару
2. Написати класифікацію карбонових кислот. 3. Які дві кислоти мають спільну молекулярну формулу С4Н8О2? Назвіть їх. 4. Напишіть рівняння реакцій, за допомогою яких можна добути карбонові кислоти: а) взаємодію солей карбонових кислот…Олігосахариди – це продукти, побудовані з двох або кількох (до десяти) моносахаридів. Серед них найбільше значення мають дисахариди.
Сахароза – це безбарвна кристалічна речовина, розчинна у воді. Характерною властивістю сахарози (і взагалі всіх олігосахаридів) є здатність…Запитання до семінару
2. Як класифікують вуглеводи і чому? 3. Як можна експериментально довести, що в молекулі глюкози є 5 гідроксильних… 4. Зобразіть структурну формулу глюкози.– Конец работы –
Используемые теги: семінарських, занять, предмету, ХІМІЯ0.07
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: До семінарських занять з предмету: Хімія
Что будем делать с полученным материалом:
Если этот материал оказался полезным для Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов