рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Электроника
- /
- Лекція 3 ТОКСИКОЛОГІЧНІ АСПЕКТИ ОРГАНІЧНИХ РОЗЧИННИКІВ ТА ІНШИХ ЛЕТКИХ ОТРУТ
Реферат Курсовая Конспект
Лекція 3 ТОКСИКОЛОГІЧНІ АСПЕКТИ ОРГАНІЧНИХ РОЗЧИННИКІВ ТА ІНШИХ ЛЕТКИХ ОТРУТ
Лекція 3 ТОКСИКОЛОГІЧНІ АСПЕКТИ ОРГАНІЧНИХ РОЗЧИННИКІВ ТА ІНШИХ ЛЕТКИХ ОТРУТ - раздел Электроника, Лекція 3 Токсикологічні Аспекти Органічних Розчинників Та Інших Летк...
Лекція 3
ТОКСИКОЛОГІЧНІ АСПЕКТИ ОРГАНІЧНИХ РОЗЧИННИКІВ ТА ІНШИХ ЛЕТКИХ ОТРУТ
1.Загальна характеристика деяких органічних розчинників та їх токсикологічне значення
«Леткі» отрути – це токсичні речовини, що ізолюються з біологічного матеріалу дистиляцією (прегонкою) з водяною парою та іншими методами і характеризуються леткістю.

До цієї групи належать представники різних класів хімічних сполук;синильна кислота, деякі спирти аліфатичного ряду, альдегіди, кетони, карбонові кислоти, галогенопохідні вуглеводнів аліфатичного ряду, бензол, феноли, аміно- і нітропохідні ароматичного ряду та деякі інші речовини. Оволодіння практичними та теоретичними основами перегонки з водяною парою необхідне студентам для ізолювання з біологічного матеріалу великої групи “летких” сполук, які мають в наш час велике токсикологічне значення.
Летальні дози для деяких «летких отрут»:
НСN- 0,05-0,1 г
СН3OH-25-100 г 7-8 г-сліпота
СНС13 — 50-70 г,
СН3СООН-15г.
Зазначені речовини є високо токсичними, вони доступні, так як. широко використовуються в промисловості, сільському господарстві, медицині. Наприклад, у медицині застосовуються хлороформ, етанол, фенол, ефір; у сільському господарстві — циклони В і С для боротьби зі шкідниками; на заводах і фабриках — бензол, ацетон і інші органічні розчинники.
Загальні властивості «летких отрут» — здатність переганятися з водяною парою незалежно від змішуваності з водою. Цей метод дозволяє створити більш мякі умови для виділення зазначених речовин з біологічного матеріалу, тому що деякі речовини можуть осмолятися, розкладатися при високих температурах.
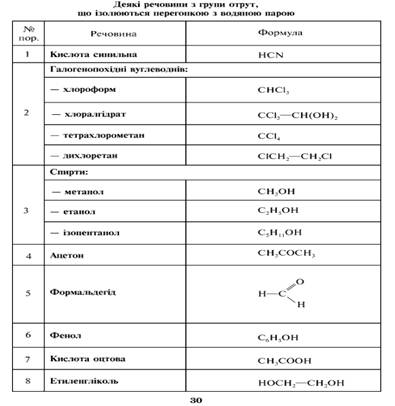

2. Органічні розчинники з групи спиртів, які використовуються у приготуванні готових лікарських засобів
Найбільше хіміко-токсикологічне значення мають перші п’ять представників гомологічного ряду насичених спиртів, а також етиленгліколь.
Спирт етиловий (С2Н5ОН) являє собою прозору, безбарвну рухливу рідину з характерним запахом і пекучим смаком, кипить при 78 °С.
Для фармацевтичних цілей застосовується етанол, одержуваний шляхом зброджування сировини, що містить полісахариди, в основному картоплі і зерна. Етанол іншого походження для готування лікарських форм не використовується у зв'язку з присутністю недопустимих домішок (спирту метилового та інших сполук).
Спирт етиловий можна віднести до неводних розчинників з визначеною часткою умовності, тому що застосовують не абсолютний етанол, а водно-спиртові розчини різної міцності. Концентрацію водно-спиртового розчину виражають в об'ємних відсотках, що показують кількість мілілітрів абсолютного етанолу в 100 мл розчину при 20 °С.
Етанол в одних випадках використовують як хороший розчинник для багатьох органічних і неорганічних сполук (органічні кислоти, ефірні та жирні олії, камфора, ментол, йод, танін, левоміцетин, алкалоїди та ін), а в інших - як лікарський засіб у вигляді розчинів, що містять спирт. Розчиняюча здатність етанолу залежить від його концентрації. Так, наприклад, олія касторова легко розчиняється в безводному (абсолютному) спирті, 85% етанол розчиняє близько 10% олії касторової, 70% - тільки 1%, а 40% - практично її не розчиняє.
Спирт змішується у всіх співвідношеннях з водою, гліцерином, ефіром, хлороформом. Він нейтральний, не окисляється киснем повітря, має бактеріостатичну і бактерицидну дію в залежності від концентрації розчину. Найбільші антисептичні властивості має спирт 70%, тому що він легко проникає всередину клітини через оболонку мікроорганізмів і убиває протоплазму. У концентраціях вище 70% спирт викликає денатурацію білкової оболонки, що перешкоджає його проникненню всередину клітини до протоплазми, а тому бактерицидна властивість спиртів вищих концентрацій не проявляється.
До негативних властивостей спирту слід віднести його неіндиферентність, сп'яняючу дію - смертельна доза 96% спирту етилового близько 210-300 мл. Він сприяє зсаджуванню білків, ферментів, легко займається, має високу гігроскопічність, несумісність з окислювачами (наявність у молекулі гідроксильної групи): калію перманганатом, бромом, міцною азотною кислотою та ін. Займистість і леткість спирту прямо залежать від його міцності. З деякими солями (кальцію хлоридом, магнію нітратом) спирт етиловий дає кристалічні сполуки.
Якість етанолу регламентується ДФ X (Spiritus aethylicus 95%).
Зберігають спирт у добре закупорених бутлях темного скла в прохолодному місці, подалі від вогню.
Спирт етиловий, або етанол (С2Н5ОН), — речовина, що має загальний пригнічувальний вплив на центральну нервову систему (нагадує ефект засобів для наркозу).
Пререзорбтивна дія — подразнювальна, в'яжуча, припікаюча, анестезуюча, протимікробна. Механізм виникнення цих ефектів зумовлений згортанням білків і дегідратацією тканин. Протимікробна дія розвивається досить швидко: відбувається денатурація білків цитоплазми мікроорганізмів. Звикання до спирту етилового у мікробів не виникає. При застосуванні для дезінфекції рук спирт етиловий виявляє досить значний ефект. Протимікробна дія збільшується при підвищенні його концентрації від 10 до 70 %. У концентрації понад 70 % спирт етиловий утворює плівку на поверхні шкіри (дубильна дія), абсорбція його припиняється, протимікробна дія зменшується.
Фармакокінетика. При застосуванні всередину спирт етиловий швидко абсорбується вже слизовою оболонкою порожнини рота. Близько 20 % абсорбується у шлунку, 80 % у тонкій кишці. Спирт подразнює слизову оболонку шлунка. У осіб, які постійно і багато вживають алкогольні напої, блювотного рефлексу немає. Через 5 хв після вживання всередину спирт етиловий можна виявити у плазмі крові. У концентрації 10-20 % абсорбується краще, ніж 30-40 % (внаслідок дубильної дії та місцевого звуження судин). Теплі розчини і розчини, що містять С02, також абсорбуються краще. Розподіл спирту етилового відбувається прямо пропорційно гідратації тканин і обернено пропорційно вмісту ліпідів, продовжується протягом 1-1,5 год. Спирту етиловому властива органотропність, наприклад, у тканинах мозку його міститься більше, ніж у крові, він також концентрується в секреті передміхурової залози, яєчках, сім'яній рідині, добре проникає крізь плаценту. Біотрансформація спирту етилового здійснюється шляхом окиснення (90 %), 10 % виводиться у незміненому вигляді через легені, нирки, потові залози, 70-80 % окиснюється в печінці. Цей процес здійснюється трьома шляхами.
1. В гепатоцитах за допомогою алкогольдегідрогенази до ацетальдегіду (3/4 об'єму). Це основний шлях у здорових людей.
2. За допомогою мікросомних ферментів печінки без алкогольдегідрогенази за участю цитохрому Р-450. Ця система значно активізована у осіб, які зловживають алкогольними напоями.
3. За допомогою каталази, оксидаз і пероксидаз. Цим шляхом метаболізується 10-15 % спирту етилового, у хворих на алкоголізм — значно більше.
Звикання до алкоголю зумовлене підвищенням активності детоксикації. При тривалому вживанні спирту етилового відбувається індукція ферментів печінки, що викликає зростання інактивації алкоголю. Суперактивація ферментів нестійка, толерантність змінюється підвищеною чутливістю організму до спирту етилового.
Ацетальдегід, що утворився, окиснюється альдегіддегідрогеназами тканин за наявності кисню, НАД, КоА до ацетил-КоА. У осіб, які зловживають алкогольними напоями, цей процес уповільнений. Подальше перетворення ацетил-КоА: залучається до енергетичного обміну (затримується окиснення пірувату, розвивається лакта-цидемія, ацидоз), синтезу жирних кислот (жирова дистрофія печінки тощо), холестерину (розвиток атеросклерозу).
Ацетальдегід має прямий шкідливий вплив на організм. Він сприяє вивільненню катехоламінів із депо, накопиченню НАДН і НАДФН, що порушує обмін катехоламінів. Взаємодія ацетальдегіду з серотоніном викликає психічні порушення, галюцинації.
Кінцеві продукти окиснення спирту етилового — С02 і Н20.
Фармакодинаміка. Резорбтивна дія передусім поширюється на центральну нервову систему, потім на серцево-судинну, дихальну, травну, впливає на діурез, обмін речовин.
Щодо впливу спирту етилового па центральну нервову систему розрізняють три стадії:
I стадія — збудження. Відбувається ослаблення процесів гальмування, з'являються ейфорія, самовпевненість, знижена реакція на навколишнє середовище, неможливість виконувати точні дії, зменшення витривалості.
II стадія — пригнічення, зменшується відчуття страху, помірна анальгезія, снодійний ефект, наркотична дія. Спирт етиловий не використовують як засіб для наркозу через малу наркотичну широту і тривалий період збудження.
III стадія — агональна. Вплив на автономну нервову систему зумовлений вивільненням катехоламінів з надниркових залоз і симпатичних нервк.
У І стадії вивільнення катехоламінів під впливом спирту етилового викликає підвищення артеріального тиску, тахікардію, підвищення потреби міокарда в кисні, напади стенокардії.
У II стадії артеріальний тиск знижується. Спостерігається специфічна зміна периферичних судин (параліч судин лиця, кон'юнктиви). Пригнічення судинорухового центру викликає параліч судин шкіри. Збільшується тепловіддача.
Спирт етиловий у малих дозах збуджує дихання, в більших — пригнічує, при тяжкій інтоксикації настає параліч дихального центру.
У концентрації до 4 % спирт етиловий підвищує ферментативну здатність шлункового соку, 20 % і вище — пригнічує секрецію, понад 50 % — значною мірою подразнює, припікає слизову оболонку, пригнічує рухову здатність.
Спирт етиловий є протиплазматичною отрутою, негативно впливає на клітини печінки (викликає алкогольний цироз). Збільшує діурез. Негативно впливає на статеві органи, на репродуктивну функцію. У хворих на алкоголізм діти народжуються з психічними і фізичними вадами. Ступінь інтоксикації спиртом етиловим зумовлена вмістом його у крові людини: 1-2 г/л — сп'яніння; 3-4 г/л — інтоксикація; 5-8 г/л є смертельною концентрацією.
При гострому отруєнні спиртом етиловим розвивається стан коми: шкіра стає холодною, липкою, червоніє лице, кон'юнктива, знижується температура тіла, неодноразове блювання, мимовільне виділення сечі та випорожнення. Хронічна інтоксикація (алкоголізм) розвивається у випадках регулярного вживання спирту етилового. Розвивається психічна і фізична залежність з абстинентним синдромом. Порушується психічна діяльність, знижується інтелект, розумові здібності, вражаються периферичні нерви. Відбувається руйнівний вплив на внутрішні органи (гастрит, цироз печінки, жирова дегенерація міокарда, нирок). Розвивається психічна і фізична деградація особи.
Лікування при гострому отруєнні. Негайне промивання шлунка кілька разів (алкоголь може виділятись слизовою оболонкою шлунка), очисна клізма. Введення сорбентів, гіпертонічного розчину глюкози з інсуліном, 4 % розчину натрію гідрогенкарбонату. Стимуляція дихання, кровообігу, зігрівання тіла. Симптоматичні засоби.
При хронічному отруєнні застосовують і тетурам (дисульфірам), що блокує окиснення спирту і затримує процес метаболізму на стадії утворення ацетальдегіду. При цьому у хворого розвивається відраза до алкоголю. Ефект нетривкий. Тетурам пролонгованої дії (еспераль) підшивають під шкіру живота. Тривалість ефекту 4-6 місяців. Інколи для вироблення негативного умовного рефлексу використовують блювотні засоби (наприклад, апоморфін) одночасно з призначенням спирту етилового. Для комплексного лікування хворих на і алкоголізм можна використовувати метод психотерапії. Сьогодні ефективних засобів для лікування хворих на алкоголізм немає.
Показання до застосування спирту етилового — дезінфекція шкіри, інструментарію, лікування при опіках, обтирання, компреси. Застосовують для інгаляцій під час набряку легень (як піногасник). Для резорбтивної дії також використовують у випадках гангрени, абсцесу легень, як антидот при отруєнні спиртом метиловим (внутрішньовенно).
Метиловий спирт (метанол) - безбарвна рідина (т. кіп. 64,5 ° С, густина 0,79), змішується у всіх співвідношеннях з водою і багатьма органічними розчинниками. Метиловий спирт отруйний, він горить блідо-блакитним коптить полум'ям. Метиловий спирт за запахом і смаком майже не відрізняється від етилового. Відомі випадки отруєння метиловим спиртом, помилково прийнятим замість етилового. У природі метиловий спирт у вільному стані майже не зустрічається. Поширені його похідні - ефірні масла, складні ефіри й ін Раніше метиловий спирт отримували шляхом сухої перегонки дерева. Тому й досі неочищений метиловий спирт, отриманий сухий перегонкою деревини, називають деревним спиртом. В даний час використовується кілька промислових синтетичних способів отримання метилового спирту.
Застосування. Дія на організм. Метиловий спирт широко використовується в промисловості як розчинник лаків, фарб, як вихідна речовина для отримання хлористого метилу, діметілсульфата, формальдегіду і ряду інших хімічних сполук. Він застосовується для денатурації спирту етилового, входить до складу антифризу. Метиловий спирт може надходити в організм через харчовий канал, а також з повітрям, що містить пари цього спирту. У незначних кількостях метиловий спирт може проникати в організм і через шкіру. Токсичність метилового спирту залежить від обставин отруєння та індивідуальної сприйнятливості. Під впливом метилового спирту відбувається ураження сітківки ока та зорового нерва, а іноді настає невиліковна сліпота. Поява сліпоти ряд авторів пояснюють не дією метилового спирту, а дією його метаболітів (формальдегіду і мурашиної кислоти). Метиловий спирт порушує окислювальні процеси і кислотно-лужну рівновагу в клітинах і тканинах. Внаслідок цього настає ацидоз. Отруєння метиловим спиртом в ряді випадків закінчується смертю. Небезпека появи сліпоти виникає вже після прийому 4-15 мл метилового спирту. Токсичними вважають дози від 30 мл. На токсичність впливає одномоментний прийом етанолу, при цьому токсична доза може зростати багаторазово. Смертельна доза прийнятого внутрішньо метилового спирту становить 30-100 мл. Смерть настає в результаті зупинки дихання, набряку головного мозку і легень, колапсу чи уремії. Місцева дія метилового спирту на слизові оболонки проявляється сильніше, а наркотичну дію - слабкіше, ніж у етилового спирту. Одночасне надходження метилового та етилового спиртів в організм зменшує токсичність метилового спирту. Це пояснюється тим, що етиловий спирт зменшує швидкість окислення метилового спирту майже на 50%, а отже, і зменшує його токсичність. Метаболізм. Метиловий спирт, що надійшов в організм, розподіляється між органами і тканинами. Найбільша кількість його накопичується в печінці, а потім у нирках. Менші кількості цього спирту накопичуються в м'язах, жирі і головному мозку. Метаболітом метилового спирту є формальдегід, який окислюється до мурашиної кислоти. Частина цієї кислоти розкладається на оксид вуглецю (IV) і воду. Метанол в організмі людини метаболізується тими ж ферментами, що і етанол: алкогольдегідрогенази до формальдегіду, а останній альдегіддегідрогенази до мурашиної кислоти. При цьому розвиваються пригнічення ЦНС, виражений метаболічний ацидоз, токсичні ураженнязорового нерва і сітківки ока, сліпота. Вважається, що метаболічний ацидоз обумовлений дією мурашиної кислоти, а сліпота - переважно токсичною дією формальдегіду на орган зору. Метаболізм метанолу відбувається значно повільніше, ніж етанолу.Деяка кількість метилового спирту, не піддалося метаболізму, виділяється з повітрям, що видихається. Він може виділятися з сечею у вигляді глюкуроніду. Однак з сечею можуть виділятися і невеликі кількості незміненого метилового спирту. Метиловий спирт окислюється в організмі повільніше, ніж етиловий спирт. При укладенні про отруєння метиловим спиртом слід мати на увазі, що в організмі (в нормі) може міститися 0,01-0,3 мг% метилового спирту і близько 0,4 мг% мурашиної кислоти. Виявлення метилового спирту. Враховуючи летючість метилового спирту при ізолювання його з біологічного матеріалу шляхом перегонки з водяною парою, приймач для дистиляту необхідно охолоджувати холодною водою або льодом. Окислення метилового спирту. Більшість реакцій виявлення метилового спирту грунтується на окислюванні його до формальдегіду і визначенні останнього за допомогою реакцій фарбування.
Симптоми отруєння. У початковий період інтоксикації клінічна картина нагадує таку при алкогольної інтоксикації. Але через 1 - 40 год (в залежності від прийнятої дози) розвиваються характерні симптоми отруєння метанолом: з боку травного каналу - нудота, блювота, пронос, біль в животі; ЦНС - різного ступеня пригнічення свідомості аж до коматозного стану, судоми і центральні розлади дихання ; органу зору - від «миготіння мушок», появи «сітки» перед очима, іноді диплопії до стійкого прогресивного зниження гостроти зору, помірний мідріаз, пригнічення фотореакцій; серцево-судинної системи - тахікардія, коливання рівня артеріального тиску, погіршення гемодинаміки при важкій інтоксикації. Шкірні покриви і видимі слизові оболонки сухі, спостерігається тотальний ціаноз.
Гострі отруєння метанолом поділяють на швидко перебігаючу (блискавичну) і сповільнену форми інтоксикації.Блискавична форма наступає після прийому всередину масивної дози отрути(200-300 мл). У потерпілого швидко розвиваються сопор, потім кома, колапс. Смерть може наступити вже в перші 2-3 години.
При сповільненій формі виділяють наступні періоди:
— сп’яніння (тривалістю 6-8 год.),
— відносного благополуччя (тривалістю від 1-2 годин до 2-3 діб),
— виражених симптомів отруєння,
— зворотного розвитку (при сприятливому перебігу).
Сповільнену форму, в залежності від клінічного перебігу, можна поділити
на три форми: легку, середньої важкості (офтальмічну) і важку
(генералізовану).
Діагностика. Діагноз встановлюють на підставі характерної клінічної картини, наявності ураження сітківки та зорового нерва, виявлення метанолу в біологічних середовищах організму.
Лікування. У першу чергу необхідно нормалізувати функції дихальної та серцево-судинної систем, купірувати судоми, якщо вони є. Для зняття явищ метаболічного ацидозу вводять натрію гідрокарбонат. Промивають шлунок, вводять ентеросорбент, проносне.
Етиленгліколь (СН2ОН)2 — безбарвна, сиропоподібна рідина, солодка на смак, без запаху. Температура кипіння + 197,2° С, добре змішується з водою і спиртом. Температура замерзання - 40° С.
Фізико-хімічні властивості. Етиленгліколь входить в склад різно-манітних рецептур гальмівних рідин та антифризів — незамерзаючих рідин в радіаторах двигунів внутрішнього згорання.
Шляхи поступання в організм і токсичність. Отруєння етиленгліколем переважно пов’язані з вживанням його з метою викликати стан сп’яніння.
Мінімально токсичною дозою для людини є 30-50 мл всередину, смертельною — від 100 мл і вище.
Механізм дії етиленгліколю пояснюється двома факторами. Спочатку він, як двохатомний спирт, діє наркотично і може викликати смерть в результаті значного пригнічення центральної нервової системи, в яку він легко проникає і сорбується на клітинних мембранах.
Потім з етиленгліколя в печінці та нирках при участі фермента алкоголь-дегідрогенази утворюються гліколева та щавелева кислоти. Остання зв’язує іонізований кальцій і переходить в оксалати:
Щавелева кислота викликає ацидоз і гіпоксію. Щавелевокислий кальцій, як нерозчинна у воді сполука, викликає некронефроз, закупорку ниркових канальців і анурію.
Зменшення вмісту кальцію в крові та тканинній рідині може привести до ослаблення серцевих скорочень, виникнення гіпотензії, рухових порушень і навіть розвитку судом (синдром тетанії).
Клінічна картина отруєння.
При отруєннях легкого ступеня порушення обмежуються вегетативними розладами, диспептичними явищами та загальною слабістю, посиленим виділенням оксалатів з сечею.
При отруєннях середнього ступеня відмічаються запаморочення, головний біль, нудота, блювота, болі в животі та попереку, порушення їх сечовидільної функції.
В клінічній картині важкого отруєння розрізняють три стадії: початкових явищ, мозкових проявів і ниркову. Слід відмітити, що вони не завжди чітко розмежовані і не у всіх проявляються в однаковій мірі.
Стадія початкових проявів. Відчуття сп’яніння, що з’являється після прийому етиленгліколю, швидко проходить і наступає безсимптомний пері-од, що може тривати від 2 до 24 год. Потім розвиваються ейфорія, атаксія, запаморочення, головні болі, нудота, блювота, болі в животі, в ділянці попереку. Подібний стан триває від 4 до 15 годин.
Стадія мозкових проявів. Даний період при важких отруєннях явно виражений. Ейфорія швидко змінюється депресією, загальмованістю, станом, подібним до наркотичного, що є передвісником коми. Потерпілі можуть ска-ржитись на головний біль, болі в поперековій ділянці, онімінння пальців, неприємні відчуття в грудях. Відмічається атаксія, зіниці розширені, з в’ялою реакцією на світло.
Із симптомів ураження центральної нервової системи найчастіше зустріча-ється різний ступінь порушення свідомості — від оглушення до коматозного стану. Психопатологічні прояви інтоксикації зводяться до порушення пам’яті, слабого орієнтування в довкіллі, різного роду галюцинацій.
Порівняно швидко наступають зміни з боку крові — збільшується кіль-кість еритроцитів, підвищується вміст гемоглобіну, відмічається виражений нейтрофільний лейкоцитоз.
Розвиток інтоксикації етиленгліколем завжди супроводжується ацидозом, вираженість якого прямо пропорційно залежить від важкості отруєння. Знижується резервна лужність крові, з’являються ацетонемія та ацетонурія.
Стадія ниркових проявів. При подальшому перебігу інтоксикації на 2-3 добу різко знижується діурез. Внаслідок розвитку токсичного нефрозо-нефриту порушення сечовидільної функції нирок супроводжується значним погіршенням загального стану.
В цей період хворі скаржаться на запаморочення, поганий сон, спрагу, болі в попереку та животі, болючий сечопуск. У них відмічається оліго- та анурія, сеча набуває кольору м’ясних помиїв. В подальшому розвиваються азотемія, уремія, гіпертонія. Отруєні гинуть при явищах уремічної коми, як правило, на 8-14 добу.
Діагностика гострих отруєнь етиленгліколем базується на врахуванні наступних ознак:
— визначенні в сечі значної кількості оксалатів кальцію;
— періодичності перебігу та клінічних особливостях інтоксикації;
— визначенні етиленгліколю в біосередовищах.
Лікування. Патогенетична терапія при отруєнні етиленгліколем повинна бути спрямована на:
— попередження утворення токсичних метаболітів етиленгліколю;
— відновлення порушеної іонної рівноваги;
— зниження рівня оксалатів.
При наданні першої медичної допомоги необхідно проводити наступні заходи:
— видалити етиленгліколь із шлунку (дати випити 400-500 мл 1-2% р-ну гідрокарбонату натрію і викликати блювоту — повторити 2-3 рази);
— зондовим методом промити шлунок 2 % р-ном гідрокарбонату натрію — кожні 2 години;
— призначити сольове проносне, енетеросорбенти і рясне пиття;
— для боротьби з ацидозом довенно крапельно вводити ізотонічний роз-чин гідрокарбонату натрію (5% - 500мл);
— довенне введення 50 мл 40% р-ну глюкози і 5 мл 5% р-ну аскорбінової кислоти.
Антидотом при отруєнні є етиловий спирт, який вступає в конкурентні відносини з етиленгліколем за зв’язок з ферментами, окислюючими спирти (алкогольдегідрогеназою та ін.). Це приводить до зменшення утворення ща-велевої кислоти та інших токсичних продуктів метаболізму і сприяє виведенню етиленгліколю із організму в незміненому вигляді. Призначається в дозах і за методикою, як при отруєннях метанолом.
Для відновлення порушеної іонної рівноваги, пов’язаної з дефіцитом кальцію в крові, необхідно довенне введення препаратів кальцію (20-30 мл 10% р-ну глюконату кальцію, хлористого кальцію).
Сірчанокислий магній (25% р-н 5-20мл) вводять довенно повільно для зменшення утворення оксалатів. При взаємодії сірчанокислого магнію зі щавелевою кислотою утворюється щавелевокислий магній — добре розчинна у воді сіль, яка легко виводиться нирками. В результаті значно зменшується кількість щавелевокислого кальцію, який відіграє в патогенезі отруєння значну роль.
До розвитку олігоурії призначають форсований діурез з використанням великих доз лазиксу — до 1.0 г на добу та замісної інфузійної терапії лужними кристалоїдними розчинами.
Симптоматична терапія повинна бути спрямована на боротьбу з гіпоксією, порушеннями дихання, падінням серцевої діяльності, порушеннями судинного тонусу і пригніченням центральної нервової системи.
При прийомі всередину більше 200 мл отрути рекомендована операція замінного переливання крові. При можливості отруєний повинен бути якнайшвидше направлений на гемодіаліз або перитонеальний діаліз, які особливо ефективні в перші 6-12 годин після отруєння.
Дихлоретан – (хлористий етилен, етилендихлорид (СН2Сl — CН2Cl)) відноситься до хлорованих вуглеводнів. Це безбарвна рідина із специфічним запахом хлороформу. Погано розчинний у воді, добре — в спирті та ефірі. Дихлоретан добре розчиняє жири, стійкий до дії води, кислот і лугів, останніми гідролізується при високій температурі. Температура кипіння 83,7° С, замерзання —37° С. Пара в 3,5 разів важча за повітря. Застосовується як розчинник жирів, мастил, лаків, фарб, є сировиною для синтезу пластмас. Входить до складу дегазуючого розчину N 1.
Токсичність. Дихлоретан потрапляє в організм через травний та ди-хальний шляхи, а також через шкіру.
Летальна доза при прийомі всередину 20 - 50 мл, смертельна концентрація 0,3-0,6г/м3,гранично допустима концентрація —0,01 г/м3.
Механізм дії. Дихлоретан відноситься до групи наркотиків жирного ряду. При інгаляційному отруєнні він легко проникає з легенів в кров і швидко розчиняється в рідких середовищах організму.
Токсична дія дихлоретану зумовлена наркотичним впливом на центральну нервову систему, вираженою дією на серцево-судинну систему, ураженням паренхіматозних органів, здебільшого печінки. Попадаючи в кров, дихлоретан накопичується в тканинах, багатих ліпідами: центральній нервовій системі, сальнику, наднирниках, печінці, в результаті чого в них розвиваються дегенеративні процеси і жирове переродження.
Дихлоретан в ендоплазматичному ретикулумі печінки підлягає окис-лювальному дехлоруванню за участю оксидаз “змішаної функції” (цитохром Р-450 та інші). В результаті реакції утворюється стабільний дегалогенізований електрофільний радикал Cl—CH2—CH2—, який, руйнуючи внутрішньоклітинні структури гепатоцитів, здатний алкілувати нуклеопротеїди та інші біосубстрати. Внаслідок метаболізму утворюються високотоксичні речовини — хлоретанол і монохлороцтова кислота, які викликають пошкодження клітинних мембран, порушення внутрішньоклітинного обміну і цитоліз клітин.
Дихлоретан та його метаболіти вступають в реакцію кон’югації, що призводить до зниження детоксикуючої функції печінки за рахунок виснаження запасів відновленого глутатіону печінки, який нейтралізує отруту та її метаболіти.
В патогенезі ураження печінки не виключений вплив вільних перекисних радикалів, які діють на ліпіди мембран гепатоцитів. Також порушуються клі-тинні мембрани ендотелія судинної стінки. Це сприяє збільшенню їх проник-ливості і зменшенню маси циркулюючої крові, що призводить до гіповолемії і різкого ацидозу.
Виведення отрути здійснюється, в основному, через легені, нирки, кишеч-ник.
Клініка. При пероральному отруєнні дихлоретаном клініка отруєнь розвивається бурхливо. Виникає біль в животі, нудота, блювання, загальна слабість, адинамія або, навпаки, ейфорія, психічне збудження, слухові та зорові галюцинації, непритомність, судоми, коматозний стан. Смерть наступає в перші години після отруєння. Якщо протягом перших 2 діб хворий не гине, то розвиваються токсичний гепатит і нефропатія, шлунково-кишкові кровотечі, пневмонії. Смерть у віддаленому періоді наступає від гострої нирково-печінкової недостатності.
При інгаляційних отруєннях після прихованого періоду (від декількох хвилин при тяжких отруєннях і до 12 годин при легкому ступені) розвиваються неврологічні розлади, потім приєднуються порушення функцій шлунково-кишкового тракту, печінки і нирок. При дії високих концентрацій дихлоретану швидко розвивається кома. Смерть наступає від паралічу дихання або серцево-судинної недостатності.
Діагноз отруєнь дихлоретаном ставлять на підставі анамнезу, бурхливої картини інтоксикації, наявності запаху дихлоретану в блювотних масах, по-вітрі, що видихає потерпілий. Його можна підтвердити визначенням отрути в біосередовищах.
В аналізах периферійної крові в початковій стадії відмічаються неспецифічні зміни: нейтрофільний лейкоцитоз (із зсувом вліво), лімфоцитопенія. При важкій формі інтоксикації відмічається згущення крові, збільшення кількості еритроцитів, лейкоцитів, підвищується процент гемоглобіну і зменшується кількість лімфоцитів. Часто визначається білірубінемія.
Сеча у потерпілих солом’яно-жовтого кольору, мутна, кислої реакції. В сечі визначається білок, циліндри, еритроцити і багато уратів в осаді.
При ураженнях шкіри розвивається хімічний дерматит, який характеризується появою ерітеми і пухирців.
Перша допомога та лікування. При пероральному отруєнні дихлоретаном необхідно якомога швидше промити шлунок 2 % р-ном двовуглекислої соди, дати сольове проносне і довенно ввести 10 мл 10 % р-ну хлористого кальцію та 10-20 мл 40 % р-ну глюкози.
Специфічним антидотом дихлоретану є ацетилцистеїн. Його лікувальний ефект залежить від здатності взаємодіяти з хлоретанолом та іншими токсичними метаболітами з утворенням меркаптурових кислот. В першу добу антидот вводять довенно по 10,0 мл через кожні 3-4 години, в другу — з інтервалом 6-8 годин.
Важливу роль відіграє введення вазелінового масла, у якому розчиняється дихлоретан, що припиняє подальше всмоктування препарату в шлунково-кишковому тракті.
Потерпілому необхідно забезпечити тепло та рясне пиття. У важких випадках звертаються до кровопускання (300-400 мл) з наступним введенням глюкози з аскорбіновою кислотою.
За показаннями застосовують засоби, що збуджують нервову систему (кофеїн, камфору, кордіамін, коразол).
При інгаляційному отруєнні, після виведення (винесення) потерпілого із зони ураження, його необхідно зігріти, дати достатню кількість гарячого пиття. Призначають кисневі інгаляції.
На етапах кваліфікованої та спеціалізованої медичної допомоги рекомендується введення кровозамінників, проведення форсованого діурезу. В перші 6 годин з моменту отруєння показані гемодіаліз, гемосорбція, в пізніші терміни — перитонеальний діаліз.
Трихлоретилен
Застосовується як розчинник жирів і масел, засіб для очищення металевих деталей, в легкій промисловості, як наркотичний середник для інгаляційного… Наркотична отрута. Може потрапляти в організм всіма шляхами. Смертельна доза… Клінічна картина. Прояви отруєння виникають зразу ж після контакту з отрутою і характеризуються, насамперед,…Оцтова кислота
Патогенез отруєння оцтовою кислотою складається з наступних ланок:Окис вуглецю
Окис вуглецю ніколи не застосовувався як самостійна бойова отруйна речовина. Причина полягає у його великій леткості і неможливості створення… Проте, необхідно відмітити, що чадний газ має багато необхідних властивостей… Фізико-хімічні та токсичні властивості. Окис вуглецю — безбарвний, позбавлений запаху газ, з температурами кипіння…– Конец работы –
Используемые теги: Лекція, ТОКСИКОЛОГІЧНІ, аспекти, ОРГАНІЧНИХ, РОЗЧИННИКІВ, ТА, ІНШИХ, ЛЕТКИХ, ОТРУТ0.098
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Лекція 3 ТОКСИКОЛОГІЧНІ АСПЕКТИ ОРГАНІЧНИХ РОЗЧИННИКІВ ТА ІНШИХ ЛЕТКИХ ОТРУТ
Что будем делать с полученным материалом:
Если этот материал оказался полезным для Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов