рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Медицина
- /
- Конспекты по взрослой кардиохирургической патологии
Реферат Курсовая Конспект
Конспекты по взрослой кардиохирургической патологии
Конспекты по взрослой кардиохирургической патологии - раздел Медицина, Консп...
Конспекты по взрослой кардиохирургической патологии
(перевод СКОПЦА А.А.) Понимание природы сердечной патологии и процедуры принятия решения на операцию - бесценны при подготовке пациента к…Ишемическая болезнь сердца
A. Патофизиология. Ишемическая болезнь сердца (ИБС) развивается вследствие прогрессирующей обструкции коронарных артерий атеросклерозом.… B. Показания к операции.1C. Предоперационные вопросы
1. С целью уменьшения потребности в гомологичной трансфузии у пациентов с хронической стабильной стенокардией выполняется предоперационный забор… 2. Все антиангинальные лекарственные средства следует продолжать вплоть до утра операционного дня. Пациентов, которые…D. Вопросы анестезии
1. Факторы, увеличивающие миокардиальные кислородные потребности, такие как тахикардия и гипертензия, в предбайпассном периоде нужно предупреждать,… 2. Выявление и лечение ишемии является критически важным в предбайпассном периоде. Чреспищеводная эхокардиография…E. Хирургические операции
1. Стандартные коронарно-байпассные операции выполняются во время искусственного кровообращения (ИК). Защита миокарда обычно обеспечивается кардиоплегическим арестом, хотя некоторые хирурги используют альтернативные технологии, такие как перемежающийся ишемический арест и гипотермический фибрилляторный арест. Операции заключаются в шунтировании коронарного блока различными видами кондуитов. Левую внутреннюю маммарную (или грудную) артерию (ВМА) обычно используют как шунт на ножке для левой передней нисходящей артерии и дополняют венозными шунтами, размещаемыми между аортой и коронарными артериями (рисунок 1-1). Поскольку при использовании артериальных кондуитов была доказана безэпизодная выживаемость, расширенное применение ВМА (билатеральные ВМА и секвенциальные шунты) лучевой артерии стало обыкновенным. Внутривенное введение дилтиазема во время операции в дозе 0,1 мг/кг/ч (обычно 5-10 мг/ч) минимизирует кондуита из лучевой артерии.
2. Минимально инвазивные байпассные операции могут выполняться различными способами.
a. Наименее инвазивная техника называется «минимально инвазивным прямым коронарно-артериальным байпассом» или МИПКАБ. Она выполняется через небольшую левую переднюю торактомию путем создания анастомоза между левой внутренней маммарной артерией (ЛВМА) с левой передней нисходящей артерией (рисунок 1-2). Анастомоз ПКА с ПВМА может быть выполнен через правый торактомный разрез.
b. Одиночные, или мультисосудистые байпассы, выполняемые через срединную стернотомию, могут называться минимально инвазивными, поскольку позволяют эффективно избегать ИК.
c. Система HeartportTM, включающая ИК, осуществляется через бедренные сосуды в сочетании с баллонной окклюзией аорты и назначением кардиоплегии. Далее через небольшой левый торакотомный разрез выполняются одиночные или мультисосудистые байпассы. Такая минимальная инвазия позволяет ограничиваться небольшим разрезом, но не дает возможности исключить искусственное кровообращение.6
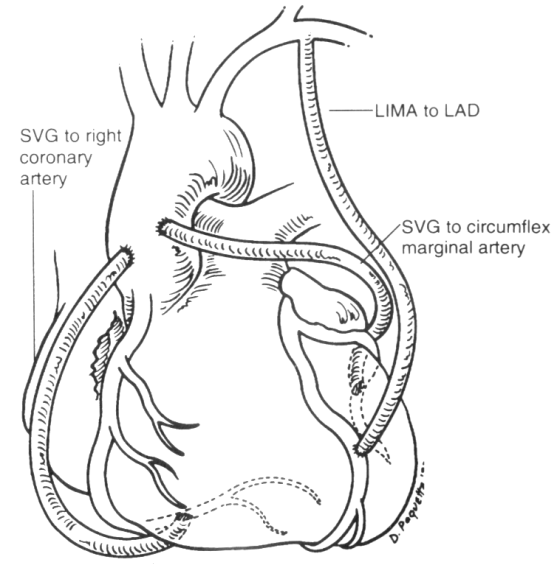
Рисунок 1.1. Шунтирование коронарных артерий. Внутренняя маммарная артерия подшивается к левой передней нисходящей артерии. Аортокоронарные шунты из v. saphena подшиты к правой и огибающей маргинальной артериям.
LIMA = Левая внутренняя маммарная артерия; LAD = Левая передняя нисходящая (артерия); SVG = Венозный шунт из v. saphena.
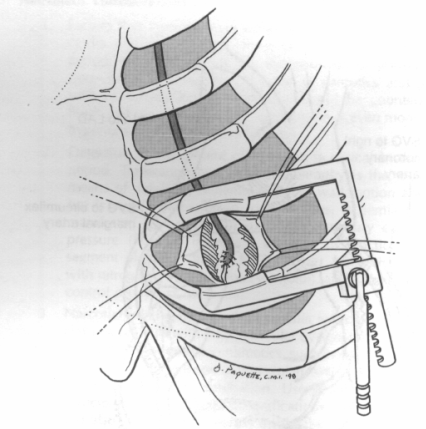
Рисунок 1.2. Процедура минимально инвазивного прямого коронарно-артериального обхода (MIDCAB). Левый передний торакотомный разрез делается в 4-ом межреберном промежутке. Внутренняя маммарная артерия располагающаяся у медиальной стороны разреза перемещается к первому межреберному промежутку. Перикард открывается и IMA. (внутренняя маммарная артерия) подшивается к левой передней нисходящей артерии на бьющемся сердце. Стабилизирующее устройство улучшает качество анастомоза.
II. Аневризма левого желудочка
A. Патофизиология
1. Левожелудочковая аневризма (ЛЖА, LVA) является следствием окклюзии крупной…C. Предоперационные вопросы
1. В присутствии левожелудочкового тромба пациенты должны находиться на гепарине. 2. Если доступно оборудование для интраоперационного картирования, следует… 3. Биплановая левожелудочковая вентрикулография является золотым стандартом при дифференциации аневризм от участков…D. Вопросы анестезии
1. Профилактика миокардиальной депрессии важна вследствие связи ЛЖА со значительной левожелудочковой дисфункцией. Для оптимизации преднагрузки и… 2. Трансэзофагеальная эхокардиография является наиболее чувствительным…III. Дефект межжелудочковой перегородки
A. Патофизиология. Обширное миокардиальное повреждение, вследствие окклюзии крупного коронарного сосуда, может приводить к септальному некрозу и… B. Показания к операции. Для предотвращения развития прогрессивной…C. Предоперационные вопросы
2. Инотропная поддержка и уменьшение постнагрузки, обычно с помощью ИАБП (IABP) показано всем пациентам со скомпрометированной желудочковой… 3. Сердечную катетеризацию с коронарной ангиографией следует выполнять для… D. Вопросы анестезии. Для предупреждения миокардиальной депрессии используется наркотическая анестезия. Системная…E. Хирургические операции
1. Традиционное хирургическое лечение заключается в вентрикулотомии через зону инфаркта, резекции области септального некроза, и закрытие заплатой из тефлонового фетра или перикарда перегородки и свободной стенки. Эта техника требует трансмуральных швов и подвержена рецидивам.
2. Циркулярная перикардиальная заплата вокруг края инфаркцированной желудочковой мышцы, исключающая участие инфаркцированной перегородки в закрытии шунта, уменьшает частоту рецидивов, поскольку швы накладываются через жизнеспособный миокард, минуя области некроза (рисунок 1-4).12
3. Следует выполнить коронарное шунтирование критически пораженных сосудов.10
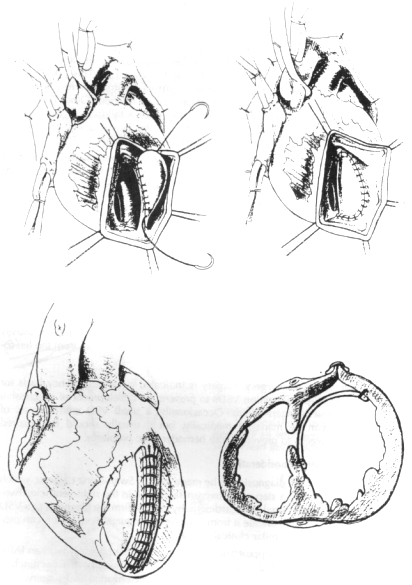
Рисунок 1.4. Коррекция переднего ДМЖП с помощью техники исключения зона инфаркта. Разрез производится через зону инфаркт и обнаруживается септальный дефект. 4-6 см перикардиальная заплата подшивается к нижней части неинфарктного септального эндокарда, а затем к неинфакртной части антелатеральной стенки. Затем с помощью полоски из фетра вентрикулотомия закрывается. (Перепечатано с разрешения David TE, Dale L, Sun Z.. Постинфарктный разрыв межжелудочковой перегородки: коррекция эндокардиальной заплатой с исключением зоны инфаркта.. J. Cardiovasc Surg 1995:110; 1315-22.)
IV. Аортальный стеноз
где: SEP = период/удар систолического изгнанияC. Предоперационные вопросы
1. Коронарная ангиография должна быть выполнена каждому пациенту старше 40 лет, и более молодым пациентам со стенокардией и положительными… 2. Ишемические синдромы у пациентов с АС требуют разумного лечения.… 3. Для уменьшения риска протезного клапанного эндокардита, до операции должна быть проведена санация зубов, если…D. Вопросы анестезии.
Индукция анестезии является критическим периодом для пациентов с АС. Наркотическая анестезия используется для минимизации гемодинамических изменений, таких как миокардиальная депрессия, вазодилятация, тахикардия, дисритмии, опасно снижающих сердечный выброс. Альфа-агенты, такие как фенилэфрин, или норадреналин, особенно полезны для поддержания системного сопротивления.
E. Хирургические операции
1. Традиционно операции на аортальном клапане выполняются через срединную стернотомию. Минимально инвазивный разрез становится все более рутинным, при этом наиболее часто используется верхняя стернотомия с “J” или “T” разрезом в третьем или четвертом межреберном промежутке. Кануляция для ИК выполняется или через основной доступ, или через бедренные сосуды.
2. Восстановительные операции, такие как комиссуротомия или debridement, играют малую роль влечение критического аортального стеноза. Однако debridement ценен у пациентов с умеренным аортальным стенозом, у которых клапанная патология не является настолько тяжелой, чтобы требовать клапанного замещения и декальцификация может отсрочить операцию на несколько лет.
3. Стандартным лечением является протезирование аортального клапана тканевым (каркасным или бескаркасным, stented or stentless) или механическим клапаном (рисунок 1-5). Гомографт следует предусмотреть у более молодых пациентов, особенно которым противопоказана антикоагуляционная терапия (возможность беременности), отсутствует желание, или присутствует эндокардит. Операция Ross, при которой собственный легочно-артериальный клапан пациента используется для замещения корня аорты (с замещением легочного клапана гомографтом) также ценна, но является технически более сложной процедурой, и обычно резервируется для молодых пациентов (< 50 лет).
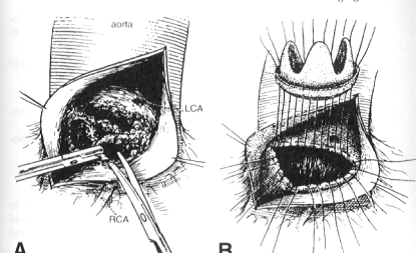
Рисунок 1.5. Протезирование аортального клапана. (A) Сделан аортотомный разрез, клапан удален ножницами и обнажено кольцо.(B) Горизонтальные матрацные швы (часто с прокладками) проводятся через кольцо и подшиваются к краю клапана. Клапан усаживается, узлы завязываются и аортотомный разрез закрывается. (Перепечатано с разрешения Cohn LN,. Протезирование аортального клапана In Cohn LH, ,ed..Современный методики хирургии: кардио/торакальная хирургия .Mt. Kisco, NY: Futura Publishing,, 1979:8-1-8-7.)
V. Аортальная регургитация
A. Патофизиология. Аортальная регургитация (АР, AR) является результатом поражения створок аортального клапана (поствоспалительной деформации;… B. Показания к операции.C. Предоперационные вопросы
1. Для уменьшения степени регургитации следует контролировать системную гипертензию с помощью вазодилятаторов. Однако избыточное снижение… 2. Β-блокаторов, для контроля ишемии, следует избегать, поскольку они,… 3. Размещение интрааортального баллона для контроля симптомов стенокардии – противопоказано.VI. Митральный стеноз
A. Патофизиология. Митральный стеноз (МС) практически всегда является…B. Показания к операции
1. Интервенциональные операции показаны при:
a. III-IV классах New York Heart Association (NYHA)
b. При II классе по NYHA, если присутствует критический митральный стеноз (MVA < 1 см2)
c. При наличии в анамнезе системной тромбоэмболии тромбами из левого предсердия
2. Чрескожная баллонная вальвулопластика (ЧБМВ, PBMV) является процедурой выбора.13,20 Эхокардиографическая оценка (echo score) выполняется для оценки клапанного утолщения, движения створок, комиссуральной кальцификации и подклапанного сращения. Echo score, кроме других факторов, таких как присутствие предсердного тромба, предсердной фибрилляции и митральной регургитации, может определить является ли эта процедура подходящей.
3. Операция показана, когда ЧБВВ противопоказана, или неосуществима.
C. Предоперационные вопросы
1. Многие пациенты с длительно существующим МС кахектичны и с высоким риском респираторной недостаточности. Энергичное предоперационное лечение… 2. Варфарин может быть использован при мерцательной аритмии или при наличии… 3. Дигоксин следует использовать при необходимости контроля желудочковых реакция на предсердную фибрилляцию. Обычно…E. Хирургические операции
1. Закрытая митральная комиссуротомия была вытеснена ЧБМВ (PBMV), которая имеет подобные результаты. Ее следует иметь в виду у беременных пациенток с критическим митральным стенозом, у которых ИК следует избегать.
2. Традиционно операции на митральном клапане выполняются через срединную стернотомию. Другие доступы, такие как верхняя стернотомия с верхним подходом к митральному клапану (между аортой и верхней полой веной), правый парастернальный разрез (биатриальный транссептальный доступ), правая переднебоковая торакотомия (задний доступ позади межпредсердной перегородки) становятся все более популярными и называются «минимально инвазивными» из-за маленького кожного разреза. ИК (CPB) может осуществляться через грудину, или бедренные сосуды.
3. Открытая митральная комиссуротомия выполняется, если ЧБМВ неосуществима, или имеются признаки левопредсердного тромбоза (рисунок 1.7).21
4. Протезирование митрального клапана (ПМК, MVR) показано, если клапанные створки или подклапанный аппарат находятся в рубцах и не подлежат открытой митральной комиссуротомии (рисунок 1-8).
5. Трикуспидальное клапанное кольцо следует предусматривать у пациентов с 3-4+ ТР (TR), особенно, если повышено ЛСС (PVR). Несмотря на то, что TR обычно улучшается после операции на левых отделах сердца, лучшие клинические результаты обычно достигаются, когда при значительной TR выполняется трикуспидальная аннулопластика.
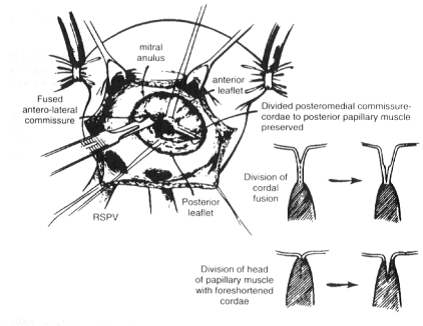
Рисунок 1.7 Открытая митральная комиссуротомия. Комиссуры отсекаются в приделах 2 мм от кольца. Область сращений клапнного аппарата иссекается. (Перепечатано с разрешения Olinger GN, Bonchek LI, Brooks HL, и др. Сердечная хирургическая техника и интраоперационные осложнения In: Bonchek Li, Brooks HL, и др. Функциональное лечение терапевтической и хирургической патологии сердца: краткое руководство для врачей. Boston: Little, Brown, 1981:285-304.)
VII. Митральная регургитация
A. Патофизиология. Митральная регургитация может быть результатом патологии кольца (дилятация), клапанных створок (миксоматозные изменения с… 1. Острая митральная регургитация обычно является результатом миокардиальной… 2. Хроническая МР характеризуется прогрессивным увеличением комплайнса левого предсердия и желудочка, с последующей…B. Показания к операции
1. Острая МР связана с застойной сердечной недостаточностью или кардиогенным шоком.
2. Острые эндокардиты с гемодинамическими нарушениями, стойкие бактериемии и сепсис, рецидивные системные эмболизации вегетациями, или угроза эмболизации крупными вегетациями.
3. Симптомы III-IV класса по NYHA.
4. I-II класс симптомов по NYHA с признаками нарушения ЛЖ (LV) функции:
a. Фракция выброса < 55%
b. Конечно-диастолические размеры, приближающиеся к 75 мм по данным эхокардиографии
c. Конечно-систолические размеры, приближающиеся к 45 мм по данным эхокардиографии
5. Для уменьшения риска развития мерцательной аритмии (и необходимости антикоагуляции) и легочной гипертензии, асимптоматичным пациентам и пациентам I-II классов по NYHA с 3-4+MR и нормальной желудочковой функцией рекомендуется ранняя операция.13
C. Предоперационные вопросы
1. Пациенты с острой МР чувствительны к отеку легких и мультисистемной органной недостаточности вследствие уменьшения антеградного сердечного… 2. Пациенты с хронической МР могут лечиться дигоксином, диуретиками и оральными разгружающими агентами, такими как…D. Вопросы анестезии
1. Для обеспечения антеградного потока в предбайпассном периоде должна поддерживаться адекватная преднагрузка. Брадикардии и системной гипертензии… 2. Для предупреждения миокардиальной депрессии, которая может уменьшать антеградный выброс, обычно используется…E. Хирургические операции
1. Реконструкция митрального клапана применима более, чем у 90% пациентов с дегенеративной МР. Техника заключается в аннулопластике кольца, коррекции створок и хордального перемещения, укорочения или замены (рисунок 1.9).22 Такие методики также применимы у пациентов с эндокардитами митрального клапана.23
2. Протезирование митрального клапана (ПМК, MVR) показано только тогда, когда удовлетворительная коррекция не может быть выполнена. Острая МР вследствие разрыва папиллярных мышц обычно требует ПМК. Сохранение хорды, по крайней мере, задней створки должно учитываться при всех случаях ПМК, выполняемых по поводу МР. Это улучшает желудочковую функцию и минимизирует риск разрыва ЛЖ.
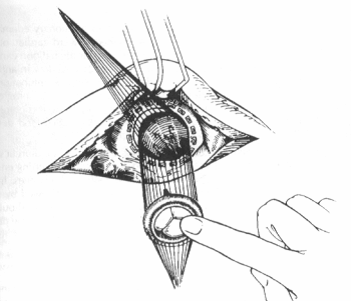
Рисунок 1.8 Протезирование митрального клапана. Экспозиция получена путем левой атриотомии, сделанной по межпредсердной борозде. Швы на прокладках проведены выше кольца и через кольцо клапанного протеза. Далее клапан усаживается на место, и швы завязываются. (Перепечатано с разрешения Cooley DA. Как делать это: имплантация клапана Ionescu-Shiley. Cardiovasc Dis 1981; 8:216-20.)
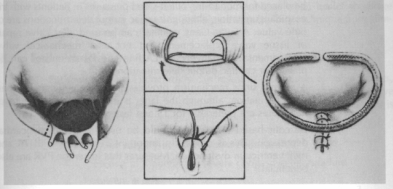
Рисунок 1.9 Коррекция митрального клапана при митральной регургитации, обусловленной разрывом хорды задней створки. Эта коррекция осуществляется путем четырехугольной резекции задней створки и повторным сближением ткани створки и имплантации кольца для аннулопластики. (Перепечатано с разрешения Carpentier A. Хирургия сердечных клапанов – «Французская коррекция». J Thorac Cardiovasc Surg 1983; 86:323-37.)
VIII. Патология трикуспидального клапана
A. Патофизиология. Изолированный трикуспидальный стеноз (ТС) очень редок, а трикуспидальная регургитация чаще всего наблюдается вследствие патологии митрального клапана, приводящей к легочной гипертензии и дилятации правого желудочка. Прогрессирование ТР продуцирует признаки правожелудочковой недостаточности – утомляемости, периферического отека и состояния низкого сердечного выброса.
B. Показания к операции.
1. Коррекция ТС показана при III-IV классах симптомов, таких как печеночный застой, асцит и периферический отек, рефрактерный к ограничению соли и диуретикам.
2. Коррекция ТР показана при тяжелых симптомах, или при наличии умеренно-тяжелой функциональной ТР во время левосторонней клапанной хирургии. Коррекция особенно важна, если ЛСС повышено.
C. Предоперационные вопросы
1. Пассивный застой печени часто приводит к коагуляционным нарушениям, которые следует энергично лечить перед и во время операции. Апротинин следует предусмотреть для минимизации кровопотери во время операции, также должны быть доступны компоненты крови. Часто эти пациенты перед операцией имеют некорригированное протромбиновое время.
2. Ограничение соли, дигоксин и диуретики могут улучшать функцию печени, но значительного улучшения функции печени не может быть без операции.
D. Вопросы анестезии
2. Нормальный синусовый механизм обеспечивает лучшую гемодинамику, чем мерцательная аритмия, хотя последняя часто присутствует. Более медленная… 3. Для предупреждения миокардиальной депрессии следует использовать…E. Хирургические операции
1. При ревматическом ТС может быть выполнена трикуспидальная комиссуротомия.
2. Трикуспидальная аннулопластика с кольцом (Carpentier) или шовная техника (DeVega или бикуспидизации) приемлемы для большинства пациентов с аннулярной дилятацией (рисунок 1.10).24
3. Трикуспидальное протезирование выполняется при деформации створок и плохой их коаптации, когда техника аннулопластики не может устранить ТР.
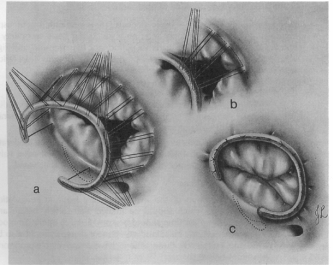
Рисунок 1.10 Трикуспидальная аннулопластика с помощью кольца Carpentier-Edwards. (a) Простые швы проводятся через кольцо, исключая область септальной створки для предупреждения повреждения проводящей системы. Редукция аннулярной дилятации наблюдается у основания передней и задней створок. (b) швы более широко распространяются на аннулярное кольцо, чем на протезное кольцо. (c) Завершение аннулопластики.. (Перепечатано с разрешения Sabiston DC Jr, Spencer FC, и др. Гиббоновская грудная хирургия 4-ое изд., Филадельфия: WB Saunders, 1983:1218.)
IX. Эндокардиты
A. Патофизиология. Эндокардиты могут приводить к разрушению клапанных створок, инвазии окружающей миокардиальной ткани, системной эмболизации клапанными вегетациями и персистентному системному сепсису. Трикуспидальный клапанный эндокардит обычно вызывается злоупотреблением внутривенных лекарств.
B. Показания к операции при первичном клапанном эндокардите
1. Присутствие умеренной и тяжелой застойно сердечной недостаточности.
2. Персистентный сепсис
3. Признаки локального расширения, вследствие аннулярного или миокардиального абсцессов, нарушения проводимости или интракардиальные фистулы.
4. Системная эмболизация
5. Распространенные вегетации с угрозой эмболизации
C. Показания к операции при протезных клапанных эндокардитах (ПКЭ, PVE)27,28
1. Все вышеперечисленное
2. Грибковая этиология
3. Клапанная обструкция
4. Нестабильный протез
5. Появление сердечного блока
6. Относительные показания: нестрептококковые организмы, перивальвулярная протечка, рецидив после завершения терапии, раннее появление ПКЭ (PVE), грам-отрицательный ПКЭ (PVE) со стойкой лихорадкой.
D. Предоперационные вопросы
1. Для уменьшения риска ПКЭ (PVE) перед операцией в идеале должен быть завершен 6-ти недельный курс антибиотикотерапии. Однако операция часто… 2. Перед операцией следует сделать попытки оптимизировать гемодинамику и… 3. Если в результате церебрального эмболизма пациент имеет неврологический дефицит, операция может быть безопасно…E. Вопросы анестезии
1. Управление анестезией определяется гемодинамическими расстройствами, связанными с особенностями вовлеченного клапана.
2. Пациенты с аортальным клапанным эндокардитом могут иметь признаки сердечного блока вследствие вовлечения проводящей системы перианнулярной инфекцией. Это может потребовать предоперационного размещения трансвенозного электрода для электрокардиостимуляции.
F. Хирургические операции
1. Операция предполагает иссечение всей инфецированной клапанной ткани, дренирование и дебридеминирование (debridement) полости абсцесса, и коррекция или протезирование пораженного клапана. При аортальном клапанном эндокардите гомографт является клапаном выбора вследствие его повышенной устойчивости к инфекции, несмотря на то, что имплантация корня гомографта более сложная процедура, чем тканевое или механическое протезирование. Последние имеют довольно сравнимый риск развития протезного клапанного эндокардита.
2. Митральные эндокардиты могут часто корригироваться, особенно, если перфорация створки является первичной патологией. Более поздние стадии эндокардитов обычно требуют клапанного протезирования.
3. Если коррекция трикуспидального клапана не может быть выполнена, трикуспидальная вальвулэктомия может быть осуществлена у пациентов без легочной гипертензии с немногочисленными неблагоприятными гемодинамическими последствиями.29 в противоположном случае клапан следует оставить. Клапан следует оберегать от злоупотребления внутривенными лекарствами, из-за значительного риска протезного клапанного эндокардита.
X. Гипертрофическая кардиомиопатия
A. Патофизиология. Асимметричная септальная гипертрофия и митральное септальное сорасположение, продуцирующие динамическую обструкцию выводному тракту, широко присутствуют у пациентов с гипертрофической кардиомиопатией (ГКМ, HCM). Диастолическая дисфункция также обычно присутствует. Эти изменения могут продуцировать клиническую картину миокардиальной ишемии , митральной регургитации, ЗСН и возможности внезапной смерти.
B. Показания к операции
1. Пиковый градиент > 50 мм Hg и стойкие симптомы несмотря на медикаментозную терапию β-блокаторами, блокаторами кальциевых каналов или DDD-стимуляцией. Операция может облегчить симптомы, хотя и оказывает малое влияние на естественное течение патологии и риск внезапной смерти.
2. Пиковый градиент > 80 мм Hg у асимптоматичных пациентов, у которых предполагается высокий риск внезапной смерти (семейный анамнез, возраст < 40 лет).
C. Вопросы предоперационной подготовки и анестезии
2. Использование β-блокаторов и блокаторов кальциевых каналов, уменьшающих частоту сердечных сокращений и контрактильность, является…D. Хирургические операции
1. Процедурой выбора является левожелудочковая миотомия-миэктомия (ЛЖММ, LVMM). Через аортотомный разрез ниже правой коронарной створки из перегородки вырезается клинообразный лоскут размерами 1,5х4 см (рисунок 1.11).
2. Митральное протезирование показано, если септальное утолщение менее 18 мм, если имеется атипичная септальная морфология, значительная митральная регургитация, или недостаточно процедуры ЛЖММ для снижения субаортального градиента.
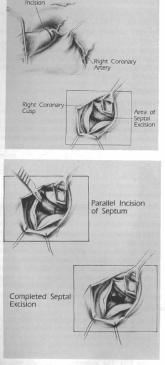
Рисунок 1.11 Левожелудочковая миотомия-миэктомия. (A) Производится поперечный аортотомный разрез и правая коронарная клапанная створка отводится назад. (B) Параллельные надрезы делаются перпендикулярно септум и септальная мышца иссекается. (Перепечатано с разрешения Doty DB. Сердечная хирургия. A looseleaf workbook and service. Chicago: Year Book Medical, 1985.)
XI. Диссекция аорты
A. Патофизиология. Диссекция аорты появляется вследствие разрыва интимы, предоставляющего путь для поступления крови в медию с формированием ложного…B. Показания к операции
1. Диссекция типа A: операция показана всем пациентам, если только этому не препятствует высокий риск, связанный с общей ослабленностью, обширными почечными, миокардиальными или кишечными инфарктами, или тяжелым инсультом.
2. Диссекция типа B: пациенты с неосложненной дисекцией типа B обычно лечатся медикаментозно, операция резервируется для осложненных диссекций (то есть, для пациентов со стойкой болью, неконтролируемой гипертензией, признаками дальнейшего распространения аневризмы и разрывом, висцеральными и почечными сосудистыми нарушениями, сосудистыми нарушениями в нижних конечностях).34 Центры с обширным опытом хирургии грудной аорты рутинно оперирующие кандидатов высокого риска с острой диссекцией типа B имеют низкую летальность и прекрасные отдаленные результаты.
C. Предоперационные вопросы
1. При подозрении диагноза всех пациентов следует лечить фармакологически с целью уменьшения кровяного давления (до 100 мм Hg систолического),… 2. Рекомендуемый антигипертензивный режим включает натрия нитропруссид с β-блокаторами (эсмолол или…D. Вопросы анестезии
1. Поддержание гемодинамической стабильности критически важно для профилактики разрыва аорты. Использование катетера Сван-Ганса является… 2. Большинство пациентов требуют экстренной операции и должны рассматриваться… 3. Трансэзофагеальная эхокардиография часто ценна для выявления места, а часто и степени диссекции. Из-за боязни…E. Хирургические операции
1. Диссекция типа A. Коррекция предполагает восстановление или протезирование аортального клапана (если присутствует аортальная регургитация), резекция интимального надрыва и вставочное протезирование графтом для восстановления целостности аортальной стенки (рисунок 1.12). Некоторые группы используют биологический клей, или при первичной коррекции, или для улучшения тканевой целостности графта.
2. Диссекция типа B. Коррекция предполагает резекцию интимального надрыва вставочное протезирование графтом для восстановления целостности аортальной стенки. Если имеются признаки висцерального артериального компромисса без разрыва, аортальная фенестрация может быть выполнена без шунтирования (grafting).35
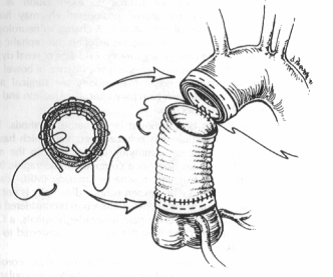
Рисунок 1.12. Коррекция диссекции аорты типа A. Аортальная стенка проксимально и дистально усиливается тефлоновыми фетровыми кольцами, располагаемыми под интимой и вокруг адвентиции. (Модифицировано с разрешения Cachera JP, Vouhe PR, Loisance DY и др. Хирургическое лечение острой аортальной диссекции, включающей восходящую аорту. Ранние и поздние результаты у 38 пациентов. J Thoracic Cardiovasc Surg 1981; 82:576-84; и из Crawford ES, Crawford JL. Патология аорты: атлас ангиографической патологии и хирургической техники. Балтимор: Williams & Wilkins, 1984:183. 1984, Williams & Wilkins Co., Baltimore.)
XII. Аневризмы грудной аорты
A. Патофизиология. Аневризмы восходящей аорты (ascending aortic, Aao) обычно возникают в результате дегенерации медии, тогда как аневризмы… B. Показания к опеарции36-38Аневризмы восходящей аорты (Aao)
a. Симптоматика, увеличение > 5,5 см в диаметре (синдрома Марфана или нет), или больше чем двойной размер нормальной аорты.
b. Аневризмы > 4,5 см, если операция показана вследствие аортальной регургитации (аннулоаортальная эктазия).
c. Все острые диссекции типа A (как отмечено выше)
d. Микотические аневризмы
Аневризмы поперечной дуги
a. Aao аневризмы, требующие протезирования, распространяющиеся на дугу аорты
b. Острая диссекция дуги с интимальным надрывом в дуге, или признаки распространения на дугу или разрыв.
c. Аневризмы > 6 см в диаметре
Аневризмы нисходящей грудной аорты (Dao)
a. Симптоматические аневризмы
b. Аневризмы > 6 см в диаметре
c. Осложненные диссекции типа B (неосложненными считаются те, которые представляют низкий риск для жизни пациента)
C. Предоперационные вопросы
1. Для операций по поводу аневризм восходящей аорты и проксимального отдела дуги требуется коронароангиография (при отсутствии острой диссекции).… 2. Стресс-сканирование (дипиридамол-талием или sestamibi) показано у… 3. Из-за высокого риска, связанного с циркуляторным аррестом (инсульт, судороги) пережатием аорты (параплегия), важна…D. Вопросы анестезии
Аневризмы восходящей аорты
a. Для коррекции аневризм AAo требуется ИК. Когда аневризма распространяется на дугу аорты, коррекция обычно сопровождается периодом циркуляторного… b. Адъюнктами, улучшающими церебральную защиту во время периода… c. Глубокая гипотермия и согревание связаны с коагулопатией. Для достижения гемостаза полезны тромбоциты,…Аневризмы нисходящей аорты
a. Для мониторинга проксимального и дистального давлений во время пережатия аорты артериальные мониторинговые линии вводятся в лучевую, а иногда и… b. Катетер Сван-Ганса важен для контроля давлений наполнения в период… c. Однолегочная вентиляция с использованием двухпросветной или однопросветной (Uni-Vent) трубки улучшает операционный…E. Хирургические операции
Аневризмы восходящей аорты
a. Супракоронарное интрапозиционное протезирование графтом выполняется, если аневризма не вовлекает синусы.
b. Клапанный кондуит (операция Bentall) размещается у пациентов с синдромом Марфана, если вовлечены синусы, или при аннулоаортальной эктазии (смотрите рисунок 1.6). Также может быть выполнена обширная резекция аорты с сохранением аортального клапана.41
Аневризмы дуги аорты
b. Расширенная коррекция предполагает размещение интерпозиционного графта и реимплантацию брахиоцефальной зоны в период циркуляторного арреста. Для… c. Коррекция дистальной дуги выполняется через левую торакотомию без… d. Если предполагается, что в будущем возможна коррекция нисходящей аорты, часть графтовского материала оставляют…Нисходящая грудная аорта
a. Интерпозиционное протезирование графтом. b. Следует рассмотреть вопрос об использовании адъювантов (лекарства, дренаж…XII. Желудочковые аритмии
A. Патофизиология
1. Поздняя (>48 часов) постинфарктная желудочковая тахикардия (VT) возникает вследствие гетерогенного миокардиального повреждения,… 2. Неишемическая желудочковая тахикардия может быть результатом… 3. Внегоспитальная остановка сердца часто не связана с миокардиальным инфарктом, хотя она обычно встречается у…B. Показания к операции
1. Картированная эндокардиальная резекция выполнялась в прошлом, когда антиаритмическая лекарственная терапия и абляционные технологии ЭФ лаборатории были не в состоянии контролировать аритмии. Поскольку оборудование для интраоперационного картирования коммерчески малодоступно, во время операции по поводу аневризмы левого желудочка могут быть выполнены слепая эндокардиальная резекция или криодеструкция. Поэтому, первичной хирургической процедурой для пациентов с рецидивирующими злокачественными аритмиями является размещение ICD устройства.
2. Таким образом, показаниями для ICD-устройства являются:
a. Желудочковая тахикардия, индуцируемая или нет, рецидивирующая, несмотря на медикаментозную терапию, абляции и/или хирургическое лечение.
b. Реанимацию после внегоспитальной остановки сердца без Q-позитивного миокардиального инфаркта.
c. Пациенты с VT, подвергнутые АКШ или эндокардиальной резекции, у которых предполагается высокая вероятность рецидива.
C. Предоперационные вопросы
1. Эндокардиальная резекция (по результатам картирования) a. Если доступна технология интраоперационного картирования, предоперационное картирование в лаборатории…D. Вопросы анестезии
1. Эндокардиальная резекция: для предупреждения неудач при интраоперационном электрофизиологическом тестировании, антиаритмическую лекарственную… 2. Имплантация ICDE. Хирургические операции
1. Маловероятно, что шунтирующая хирургия, сама по себе, предотвращает рецидивы желудочковой тахикардии, поэтому обычно требуется имплантация ICD. Некоторые пациенты с желудочковой фибрилляцией могут излечиваться байпасссными операциями, однако, в настоящее время не существует технологий, указывающих на то, у каких пациентов такие оперативные вмешательства будут эффективны.
2. Эндокардиальная резекция
a. Для подтверждения источника аритмий и прямой эндокардиальной резекции или адъюнктивной криоабляции, картирующая хирургия требует интраоперационного картирования. Аневризмы обычно закрывают с помощью техники эндоаневризмораффии (смотрите рисунок 1.3 и главу 1, раздел II). Затем, в условиях кардиоплегического арреста, осуществляется аортокоронарное шунтирование. В послеоперационном периоде проводится ЭФ-исследование. Если VT еще остается индуцируемой, то в условиях электрофизиологической лаборатории имплантируется ICD-устройство.
b. Стала возможной слепая субэндокардиальная резекция, выполняемая до картирующих операций. Несмотря на множество успешных случаев лечения, она не так эффективна, как картирующие процедуры. По этой причине, большинство пациентов сегодня чаще подвергается имплантации ICD, чем хирургическим операциям.
3. Имплантация ICD
a. Большинство имплантаций ICD осуществляется в ЭФ-лаборатории и предполагает трансвенозное размещение электродов, а иногда, для улучшения порога дефибрилляции, - применение подкожных электродов. Эти устройства имплантируются в предпекторальный карман. Далее выполняется тестирование электродов на чувствительность и определяется порог дефибрилляции (DFT, defibrillation thresholds). Затем генератор подключают к отведениям и система ретестируется.
b. До широкого распространения трансвенозных систем, имплантация ICD осуществлялась через левую торакотомию, срединную стернотомию, субкостальный и субксифоидальный доступы. Несмотря на то, что такие доступы редко используются сегодня, повторное размещение и удаление инфицированных отведений системы требует знания их имплантационных методов. Эти системы обычно состоят из 2-х частото-чувствительных отведений, размещаемых на эпикарде правого и левого желудочков, и двух титановых сетчатых электродов для дефибрилляции, интра- или экстраперикардиально размещаемых над желудочками.
XIV. Частичная левая вентрикулэктомия (операция Batista)
A. Патофизиология
1. Конечная стадия сердечной недостаточности характеризуется прогрессирующей дилятацией и ремоделированием левого желудочка. Дилятация приводит к… 2. У пациентов с терминальной стадией сердечной недостаточности прогноз…C. Предоперационные и анестезиологические вопросы
2. При окончании искусственного кровообращения для уменьшения кровотечения из линии швов левого желудочка рекомендуется умеренная гипотензия…D. Хирургическая операция
2. Большой сегмент левого желудочка резецируется между двумя папиллярными мышцами (рисунок 1.13). Пластика или протезирование митрального клапана…E. Результаты
2. Несмотря на то, что цитируемая смертность при этой процедуре составляет почти 10-20%, существенный процент пациентов выживает только при…XV. Перикардиальная патология
A. Патофизиология. Перикард может вовлекаться во множество системных патологических процессов, вызывающих, либо перикардиальный выпот, либо… 1. Большое количество выпота приводит к физиологии тампонады и прогрессирующему состоянию низкого выброса. Лучше…B. Показания к операции
1. Большое количество выпота, устойчивое к другим мерам (диализ при уремии, антибиотики при инфекции, облучение или химиотерапия при онкологической патологии) или рецидивы после повторных перикардиоцентезов следует лечить или субксифоидальным перикардиальным окном, или перикардэктомией.
2. Констрикцию, продуцирующую рефрактерное состояние низкого выброса, гепатомегалию или периферические отеки необходимо лечить перикардэктомией.
C. Предоперационные вопросы
1. Незначительные тампонады часто приводят к печеночной дисфункции и печеночному застою, но ни то, ни другое не улучшается до выполнения операции.
2. Предварительный перикардиоцентез при очень больших количествах выпота увеличивает безопасность индукции анестезии, которая может продуцировать вазодилятацию, падение давлений наполнения и глубокую гипотензию.
D. Вопросы анестезии
1. Сердечный выброс и кровяное давление зависят от адекватной преднагрузки, повышенного симпатического тонуса и повышенной частоты сердечных… 2. Мониторинг с помощью катетера Сван-Ганса полезен для поддержания…E. Хирургические операции
1. Перикардиоцентез должен быть первичной процедурой при больших количествах перикардиального выпота. При рецидивах следует рассмотреть вопрос об использовании склерозирующих агентов, инстиллируемых в перикард для предотвращения реаккумуляции жидкости (доксициклин, блеомицин, тиотепа).50,51
2. Субксифоидальное перикардиальное окно используется для дренирования перикардиального пространства, получения небольшого образца для биопсии и облитерации перикардиального пространства путем слипания. Несмотря на низкую частоту рецидивов, эту процедуру лучше резервировать для пациентов с терминальной стадией онкологической патологии.
3. Перикардэктомии через левый антелатеральный торакотомный доступ, или срединную стернотомию, очень эффективны в профилактике рецидивов выпота. Лучшим доступом при констриктивных перикардитах является срединная стернотомия в сочетании с готовым АИКом. Перикард удаляют между ножками диафрагмальных нервов или сбоку, или в той мерее насколько позволяет доступ. Для предотвращения отека легких, который встречается, когда правый желудочек освобождается, а левый остается констриктированным, декортикацию левого желудочка следует выполнять в первую очередь.
Ссылки
1. Favaloro RG. Critical analysis of coronary artery bypass graft surgery: a 30-year journey. J Am Coll Cardiol 1998;31(suppl B):1B-63B.
2. King SB III. The development of interventional cardiology. J Am Coll Cardiol 1998;31(suppl B):64B-88B.
3. Repine CJ, Holmes DR Jr. Coronary artery stents. J Am Coll Cardiol 1996;28:782-94.
4. Hall P, Nakamura S, Maiello L, et al. A randomized comparison of combined ticlopidine and aspirin therapy versus aspirin therapy alone after successful intravascularultrasound-guided stent implantation. Circulation 1996;93:215-22.
5. Rupprecht HJ, Darius H, Borkowski U, et al. Comparison of antiplatelet effects of aspirin, ticlopidine, or their combination after stent implantation. Circulation 1998;97:1046-52.
6. Calafiore AM, Angelini CD, Bergsland J, Salerno TA. Minimally invasive coronary artery bypass grafting. Ann Thorac Surg 1996;62:1 545-8.
7. Dietl CA, Benoit CH. Radial artery graft for coronary revascularization: technical considerations. Ann Thorac Surg 1995;60:102-10.
8. Ba'albaki HA, Clements SD Jr. Left ventricular aneurysm: a review. Clin Cardiol1989;12:5-13.
9. Dor V, ed. Ventricular aneurysm surgery. Sem Thorac Cardiovasc Surg 1997;9:112-55.
10. Muehrcke DD, Daggett WM Jr, Buckley MJ, Akins CW, Hilgenberg AD, Austen WC. Postinfarct ventricular septal defect repair: effect of coronary artery bypass grafting. Ann Thorac Surg 1992;54:876-83.
11. Heitmiller R, Jacobs ML, Daggett WM. Surgical management of postinfarction ventricular septal rupture. Ann Thorac Surg 1986;41:683-91.
12. David TE, Dale L, Sun Z. Postinfarction ventricular septal rupture: repair by endocardial patch with infarct exclusion. J Thorac Cardiovasc Surg 1995;110:1315-22.
13. Carabello BA, Crawford FA Jr. Valvular heart disease. N Engl J Med 1997; 337:32-41.
14. Lester SJ, Heilbron B, Gin K, Dodek A, Jue J. The natural history and rate of progression of aortic stenosis. Chest 1998;113:1109-14.
15. Otto CM, Burwash IG, Legget ME, et al. Prospective study of asymptomatic valvular aortic stenosis. Clinical, echocardiographic, and exercise predictors of outcome. Circulation 1997;95:2262-70.
16. Ross D. Replacement of the aortic valve with a pulmonary autograft: the "switch" operation. Ann Thorac Surg 1991 ;52:1 346-50.
17. Gaasch WH, Sundaram M, Meyer TE, Managing asymptomatic patients with chronic aortic regurgitation. Chest 1997;111:1 702-9.
18. Klodas E, Enriquez-Sarano M, Tajik AJ, Mullany CJ, Bailey KR, Seward JB. Optimizing timing of surgical correction in patients with severe aortic regurgitation: role of symptoms. J Am Coll Cardiol 1997;30:746-52.
19. Eraser CD, Cosgrove DM III. Surgical techniques for aortic valvuloplasty. Texas Heart Inst J 1994;21:305-9.
20. Turi ZG, Reyes VP, Raju BS, et al. Percutaneous balloon versus surgical closed commissurotomy for mitral stenosis. A prospective, randomized trial. Circulation1991 ;83:1179-85.
21. Farhet MB, Boussadia H, Gandjbakhch I, et al. Closed versus open mitral commissurotomy in pure noncalcific mitral stenosis: hemodynamic studies before and after operation. J Thorac Cardiovasc Surg 1990;99:639-44.
22. Cosgrove DM, ed. Mitral valve repair. Sem Thorac Cardiovasc Surg 1989;1:105-212.
23. Dreyfus G, Serraf A, Jebara VA, et al. Valve repair in acute endocarditis. Ann Thorac Surg 1990;49:706-13.
24. Rivera R, Duran E, Ajuria M. Carpentier's flexible ring versus De Vega's annuloplasty. A prospective randomized study. J Thorac Cardiovasc Surg 1985;89:196-203.
25. McGrath LB, Gonzalez-Lavin L, Bailey BM, Grunkemeier GL, Fernandez J, Laub GW. Tricuspid valve operations in 530 patients. Twenty-five-year assessment of early and late phase events. J Thorac Cardiovasc Surg 1990;99:124-33.
26. MacGregor JS, Cheitlin MD. Diagnosis and management of infective endocarditis. Texas Heart InstJ 1989;16:230-8.
27. Cowgill LD, Addonizio VP, Hopeman AR, Harken AH. A practical approach to prosthetic valve endocarditis. Ann Thorac Surg 1987;43:450-7.
28. Vlessis AA, Khaki A, Grunkemeier GL, Li HH, Starr A. Risk, diagnosis, and management of prosthetic valve endocarditis: a review. J Heart Valve Dis 1997;6:443-65.
29. Arbulu A, Holmes RJ, Asfaw I. Tricuspid valvulectomy without replacement. Twentyyears' experience. J Thorac Cardiovasc Surg 1991 ;102:91 7-22.
30. Spirito P, Seidman CE, McKenna WJ, Maron BJ. The management of hypertrophic cardiomyopathy. N Engl J Med 1997;336:775-85.
31. Mclntosh CL, Maron BJ. Current operative treatment of obstructive hypertrophic cardiomoyopathy. Circulation 1988;78:487-95.
32. Crawford ES. The diagnosis and management of aortic dissection. JAMA 1990;264: 2537-41.
33. Fann Jl, Smith JA, Miller DC, et al. Surgical management of aortic dissection during a 30-year period. Circulation 1995;92(suppl 2):ll-113-21.
34. Elefteriades JA, Hartleroad J, Gusberg RJ, et al. Long-term experience with descending aortic dissection: the complication-specific approach. Ann Thorac Surg 1992;53: 11-21.
35. Elefteriades JA, Hammond GL, Gusberg KJ, Kopf FS, Baldwin JC. Fenestration revisited. A safe and effective procedure for descending aortic dissection. Arch Surg 1990;1 25:786-90.
36. Kouchoukos NT, Dougenis D. Surgery of the thoracic aorta. N Engl J Med 1997;336:1876-88.
37. Pitt MPI, Bonser RS. The natural history of thoracic aortic aneurysm disease: an overview. J Cardiac Surg 1997;12:270-8.
38. Coady MA, Rizzo JA, Hammond GL, et al. What is the appropriate size criterion for resection of thoracic aortic aneurysms? J Thorac Cardiovasc Surg 1997;113:476- 91.
39. Sundt TM, Kouchoukos NT, Saffitz JE, Murphy SF, Wareing TH, Stahl DJ. Renal dys function and intravascular coagulation after use of aprotinin in thoracic aortic operations employing hypothermic cardiopulmonary bypass and circulatory arrest. Ann Thorac Surg 1993;55:1418-24.
40. Royston D. A case for aprotinin in patients having deep hypothermic circulatory arrest. J Card Surg 1997;12(suppl):215-21.
41. David TE, Feindel CM. An aortic-sparing operation for patients with aortic incompetence and aneurysms of the ascending aorta. J Thorac Cardiovasc Surg l992;103:617-22.
42. Brooks R, McGovern BA, Garan H, Ruskin JN. Current treatment of patients surviving out-of-hospital cardiac arrest. JAMA 1991 ;265:762-8
43. Gregoratos G, Cheitlin MD, Conill A, et al. ACC/AHA guidelines for implantation tf cardiac pacemakers and antiarrhythmia devices: executive summary. A report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Committee on pacemaker implantation). Circulation 1998;97:1325.
44. Batista RJV, Verde J, Nery P, et al. Partial left ventriculectomy to treat end-stage heart disease. Ann Thorac Surg 1997;64:634-8.
45. McCarthy PM, Starling TC, Wong J, et al. Early results with partial left ventriculectomy. J Thorac Cardiovasc Surg 1997;114:755-65.
46. Cadeville M, Insler S, Scalia CM, et al. Anesthetic considerations for the patient undergoing partial left ventriculectomy (Batista procedure). J Cardiothorac Vase Anesthesia 1998;12:101-10.
47. Moreira LFP, Stolf NAG, Bocchi EA, et al. Partial left ventriculectomy with mitral valve preservation in the treatment of patients with dilated cardiomyopathy. J Thorac
Cardiovasc Surg 1998;115:800-7.
48. Bocchi EA, Bellotti CM, de Moraes AV, et al. Clinical outcome after left ventricular surgical remodeling in patients with idiopathic dilated cardiomyopathy referred for heart transplantation. Short-term results. Circulation 1997;96(suppl ll):165-72.
49. DeValeria PA, Baumgartner WA, Casale AS, et al. Current indications, risks, and outcome after pericardiectomy. Ann Thorac Surg 1991 ;52:219-24.
50. Maher EA, Shepherd FA, Todd TJR. Pericardia! sclerosis as the primary management of malignant pericardia! effusion and cardiac tamponade. J Thorac Cardiovasc Surg 1996;112:637-43.
51. Girardi LN, Ginsberg RJ, Burt ME. Pericardiocentesis and intrapericardial sclerosis: effective therapy for malignant pericardia! effusions. Ann Thorac Surg 1997;64:1422-8.
– Конец работы –
Используемые теги: Конспекты, взрослой, кардиохирургической, патологии0.074
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Конспекты по взрослой кардиохирургической патологии
Что будем делать с полученным материалом:
Если этот материал оказался полезным для Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов