рефераты конспекты курсовые дипломные лекции шпоры
Реферат Курсовая Конспект
ИЗБРАННЫЕ ЛЕКЦИИ ПО ВНУТРЕННИМ БОЛЕЗНЯМ
ИЗБРАННЫЕ ЛЕКЦИИ ПО ВНУТРЕННИМ БОЛЕЗНЯМ - Лекция, раздел Медицина, Министерство Здравоохранения Республики Беларусь Минский Государстве...
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РЕСПУБЛИКИ БЕЛАРУСЬ
МИНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ ИНСТИТУТ
1-я КАФЕДРА ВНУТРЕННИХ БОЛЕЗНЕЙ
МакаревичАлександр Эдуардович
ИЗБРАННЫЕ ЛЕКЦИИПО ВНУТРЕННИМ БОЛЕЗНЯМ
Утверждено Научно-методическим советом института в качестве лекций 29.11.2000 г., протокол № 3Макаревич А.Э
ISBN 985-6603-73-0ХРОНИЧЕСКАЯ НЕДОСТАТОЧНОСТЬ КРОВООБРАЩЕНИЯ
Сердце ¾ небольшой мышечный орган весом около 300 г., сверхмощный и экономичный двигатель. За 1 час (ч) сердце способно прокачать около 300 л… Определение. ХНК ¾ это патологическое состояние, обусловленное… Эпидемиология.ХНК наиболее часто вызывается ишемической болезнью сердца (ИБС) и гипертонической болезнью (ГБ). Так, в…Рис. 1. Схема патогенеза ХНК
В начале развития ХНК при снижении насосной способности сердца в организме больного используются внутрикардиальные механизмы(механизм Франка-Старлинга, гипертрофия и ремоделирование миокарда, увеличение ЧСС) компенсации и поддержания МОК на определенном уровне. Так, при снижении сократительной способности миокарда уменьшается УОС и включается механизм Франка-Старлинга — УОС поддерживается за счет повышения преднагрузки (венозного возврата к сердцу). Сила сокращения сердца прямо пропорциональна его венозному возврату (растяжению сердца, объему наполнения) и сопротивлению, против которого идет выброс. Но возможности механизма Франка-Старлинга ограничены, по мере резкого повышения объема остаточной крови в ЛЖ (или в ПЖ) идет дилатация его полости. Дилатация и ГЛЖ ¾ это важные механизмы компенсации ХНК. При резкой дилатации ЛЖ или резком (более чем 20 мм. рт. ст.; в норме около 10 мм. рт. ст.) повышении конечно-диастолического давления (КДД) в ЛЖ, создаются условия для застоя крови в малом (или большом) круге кровообращения. УОС начинает падать и механизм Франка-Старлинга перестает действовать (УОС уже больше не растет). В норме ЛЖ сердце изгоняет 70% поступившей в него крови, а 30% крови остается. При ХНК, наоборот, ЛЖ изгоняет только 30% крови, а 70% ¾ остается. То есть, увеличивается остаточный объем в ЛЖ ® повышается диастолическое давление в ЛЖ, и ® позднее ретроградно повышаются давление в левом предсердии и венозное давление. То есть, возникает нарушение насосной функции сердца: кровь, поступающая в ЛЖ, выталкивается только частично, что повышает КДД ЛЖ и его размеры. По мере снижения УОС, развивается ретроградный застой крови: сначала в левом предсердии, а потом в легочных венах (пассивная легочная гипертензия — ЛГ). Клинически больной при этом ощущает чувство нехватки воздуха (или тягостную одышку).
Второй внутрисердечный механизм компенсации в ответ на повышение нагрузки — гипертрофия миокарда (ГЛЖ, ГПЖ), изменение его геометрии, что довольно длительное время позволяет поддерживать состояние компенсации. Взаимоотношения между гемодинамической нагрузкой и структурными изменениями в миокарде описываются уравнением Лапласа: T=PR/2H, где: Т ¾ напряжение стенки; P ¾ давление; R ¾ радиус желудочка; H ¾ толщина стенки миокарда. То есть, при росте постнагрузки на миокард для сохранения АД и поддержания МОК необходимо утолщение стенки миокарда. Возникающая ГЛЖ приводит к возврату исходных величин нагрузки на стенку желудочка.
Но ГЛЖ — неадекватный механизм компенсации ХНК, так как при этом повышается потребление кислорода (ПО2) миокардом, нарушается его архитектоника; накапливаются недоокисленные продукты обмена, и идут процессы ремоделирования (гипертрофия миокарда, рост фиброза и склеротических процессов в нем; повышается ригидность миокарда; удлинение и истончение миофибрил; выпячивание зоны инфаркта или распространение его на окружающий миокард). По мере гипертрофии миокарда ухудшается его кровообращение: развитие коллатералей отстает от роста массы миокарда; ухудшается диффузия газов в миокарде и функционирование митохондрий; новые кардиальные клетки, как результат компенсации, функционируют не нормально. Все вышеперечисленное приводит к ухудшению работоспособности миокарда и усилению его энергетических затрат при работе. Избыточно гипертрофированный миокард ЛЖ не способен работать в соответствии со своими метаболическими потребностями ("не в коня — корм"), снижается насосная функция ЛЖ, и начинают проявляться признаки ЛЖ недостаточности.
Два варианта гипертрофии желудочков (концентрическая и эксцентрическая) объясняют патогенез ХНК в зависимости от первоначального механизма развития. Так, при перегрузке давлением (повышение систолического давления) растет пик систолического напряжения, параллельно появляются новые миофибрилы, что способствует концентрическому утолщению стенки желудочка. При перегрузке давлением (при аортальном стенозе или повышении AД) сердце работает против повышенного сопротивления ® уменьшается УОС ® повышается внутрикардиальное напряжение ® гипертрофия миокарда (это ФК1 по NYHA). УOC не меняется, пока гипертрофированный желудочек справляется с увеличенным сопротивлением выбросу. Если желудочек слабеет, то начинают уменьшаться УOC и ФВЛЖ (около 70% объема крови остается в ЛЖ).
Третий важный механизм внутрисердечной компенсации системной гемодинамики (по мере истощения ГЛЖ) — повышение ЧСС, необходимое для поддержания адекватного МОК на фоне снижения УОС (снижение УОС + повышение ЧСС = постоянный МОК). Тахикардия обусловлена ростом давления в устье полых вен и рефлексом Бейн-Бриджа. Но возможности тахикардии ограничены, она весьма несовершенный механизм компенсации. При повышении ЧСС уменьшается время диастолы (и ресинтез макроэргов еще больше падает), увеличивается и потребление кислорода (ПО2) миокардом, что усиливает имеющуюся ишемию миокарда. Тахикардия является хорошим маркером тяжести имеющейся патологии сердца, и по мере улучшения состояния больного (в ходе лечения) тахикардия часто уменьшается.
Основные причины систолической дисфункции сердца:
· абсолютное уменьшение числа кардиомиоцитов в единице объема миокарда (ишемический, воспалительный, токсический некроз);
· относительное уменьшение числа кардиомиоцитов в единице объема миокарда, в основном вследствие диффузного кардиосклероза;
· уменьшение числа эффективно функционирующих кардиомиоцитов по причине ишемии (включаю гибернацию миокарда);
· миокардистрофия эндокринного, токсического, анемического генеза, а также перегрузка миокарда объемом, давлением.
При перегрузке объемом (например, при недостаточности аортального клапана) повышается диастолическое давление в камере ЛЖ (в него поступает много крови) ® вторичная перегрузка давлением левого предсердия ® рост давления в легочных венах ® появление новых саркомеров ® раннее увеличение размеров ЛЖ ® эксцентрическая гипертрофия ЛЖ.
Основные причины диастолической дисфункции ЛЖ:
· гипертрофирование и ремоделирование миокарда любой этиологии;
· ишемия (ИБС);
· кардиосклероз;
· миокардиодистрофия.
фиброз ® пассивная
клеточный "беспорядок" ® жесткость ® рост диастолического
гипертрофия ® камеры давления
асинхронность сокращений ® уменьшение
ненормальная нагрузка ® релаксации
ишемия ®
ненормальное вхождение ®
ионов кальция
Рис. 2. Факторы, ответственные за диастолическую дисфункцию и повышение диастолического давления в ЛЖ.
При первичном поражении сердца (более 30% его площади) важная роль отводится и ассинергии миокарда. Возникает гипокинезия пораженных участков (из-за кардиосклероза) и гиперкинезия интактных отделов сердца. При ОИМ, ишемии миокарда (стенокардии) быстро наступает гипокинезия пораженного ишемизированного участка. Быстрое ухудшение функции сердца возникает при ОИМ или аритмиях, а медленное ¾ отражает дисфункцию кардиомиоцитов и ремоделирование желудочков.
Со временем внутрикардиальных механизмов компенсации становится недостаточно: прогрессивно снижается УОС и перфузия органов, быстро присоединяются периферические изменения, опосредованные через нейро-эндокринную систему (внесердечный механизм компенсации). На начальных этапах ХНК активация симпато-адреналовой системы (САС) с повышением уровня катехоламинов (адреналина и норадреналина) в крови и ренин-ангиотензин-альдостероновой системы (РААС) играет защитную роль, приводит к мобилизации резервов сократимости миокарда. Активация САС и повышение выделения антидиуретического гормона (АДГ) обусловлены дисфункцией барорецепторов в области дуги аорты и каротидных синусов.
Но при далеко зашедшем поражении сердца нейрогуморальная стимуляция катехоламинами через САС не может улучшить гемодинамику, на стадии декомпенсации это повреждает миокард. Так, повышение тонуса САС и циркулирующих в крови катехоламинов увеличивает постнагрузку (механизм Анрепа) и УОС. Действие осуществляется через b-рецепторы, но возможности влиять через них снижаются со временем, по мере уменьшения чувствительности b-адре-норецепторов к симпатическим стимулам (вследствие снижения регуляции
b-адренорецепторов). Из-за повышения тонуса САС возрастает ЧСС и тонус артериол на периферии, что необходимо для поддержания нормального AД. Таким образом, за счет повышения ЧСС и уменьшения объема кровяного русла (из-за вазоконстрикции) сохраняется нормальное AД. Неблагоприятные последствия активации САС при ХНК состоят в:
· повышении постнагрузки вследствие системной вазоконстрикции;
· снижении систолической и диастолической функций сердца в результате ремоделирования миокарда под действием норадреналина;
· аритмогенном действии катехоламинов;
· повышении ПО2 на фоне увеличения ЧСС;
· изменении плотности b-адренорецепторов в миокарде.
На фоне уменьшения УOC идет перераспределение ("централизация") кровотока, особенно при ФН (а позже и в покое). Поддерживается нормальный кровоток только в жизненно важных органах (мозге, сердце) и понижается кровообращение в менее важных органах (скелетные мышцы, кожа, печень, почки). При снижении почечного кровотока (в норме 25% УOC идет в почки) активизируется РААС: повышается секреция ренина, ангиотензина-II (мощный периферический вазоконстриктор, вызывающий резкий спазм периферических сосудов) и выработка альдостерона надпочечниками, что стимулирует задержку натрия и жидкости. Ангиотензин-II поддерживает клубочковую фильтрацию за счет повышения ОПС и артериальной вазоконстрикции. Это повышает нагрузку на миокард, что еще больше понижает УOC. Рост активности РААС способствует: ГЛЖ, кардиосклерозу, фиброзу и диастолической жесткости миокарда; увеличению ОЦК и преднагрузки (повышается давление наполнения ЛЖ); задержке крови в легких и печени (кардиальный фиброз). Неблагоприятные последствия активации РААС при ХНК заключаются в:
· повышении постнагрузки вследствие вазоконстрикции на фоне увеличения ангиотензина-II в крови;
· снижении систолической и диастолической функций сердца в результате ремоделирования миокарда под воздействием ангиотензина-II;
· повышении преднагрузки вследствие увеличения ОЦК на фоне задержки натрия и воды;
· повышении чувствительности b-адренорецепторов резистивных сосудов к катехоламинам.
При ХНК нарушается баланс вазодилататорной (снижаются простогландин E2, эндотелий релаксирующий фактор и предсердный натрий-уретический пептид — ПНУП, вырабатываемый в правом предсердии в ответ на его расширение; ПНУП вызывает снижение преднагрузки благодаря диуретическому действию) и вазоконстрикторной систем (активируются САС, РААС, повышаются уровни вазопрессина и АДГ).
Таким образом, при ХНК все начинается со снижения УOC и доходит до венозного застоя (это основа ХНК). Ведущие факторы развития ХНК: снижение УOC, активация САС и РААС,и как следствие этого, констрикция артериол и венул (что усугубляет нарушение перфузии тканей). По мере прогрессирования ХНК, многие из компенсаторных механизмов, вначале играющих положительную роль (например, повышение преднагрузки или уровней катехоламинов и ангиотензина II), позднее начинают играть отрицательную роль. Так, чрезмерная активация нейроэндокринных механизмов становится неадекватно выраженной (на фоне сниженной насосной способности сердца), приобретает патологические свойства, и каждый из компенсаторных механизмов становится инструментом усугубления тяжести синдрома ХНК. Так, возникает и замыкается порочный круг патогенеза ХНК (дисфункции сердца), приводящий к нарушению механизмов компенсации, что вызывает дальнейшее структурное повреждение миокарда и его дисфункцию (прогрессирующее снижение УОС). РААС играет определяющую роль в ухудшении течения заболевания. Важную роль в механизмах ХНК играет увеличение синтеза АДГ, снижение уровня НПУП, задержка натрия, воды и повышение ОЦК. Задержка натрия и воды прямо пропорционально значительному повышению ОЦК и KДД в ЛЖ. Многие симптомы ХНК вторичны по отношению к задержке жидкости, но эта избыточная жидкость имеет и свой плюс — поддерживает МОК и перфузию жизненно важных органов.
По мере прогрессирования ХНК наступает истощение компенсаторных механизмов, повышаются пред- и постнагрузка на миокард, усиливается систолическая дисфункция миокарда. Изменение в сердце и сосудах вызывает появление симптомов ХНК (усталость, одышка) и периферических отеков (в том числе застой в легких) вследствие задержки натрия и жидкости. Прогрессирующий дефицит О2 приводит к нарушению окислительных процессов, идет накопление недоокисленных веществ — пировиноградной кислоты (ПВК) и молочной кислоты (МК); развивается ацидоз, что также стимулирует задержку жидкости.
Механизмы прогрессирования ХНК:
1. Продолжающее повреждение миокарда (хроническое злоупотребление алкоголем, рецидивирующая ишемия миокарда, активный миокардит, перегрузка давлением или объемом вследствие дисфункции клапанов сердца, чрезмерная нейрогормональная активация, анемия).
2. Ремоделирование миокарда.
3. Сопутствующие аритмии.
4. Лекарственные препараты (с отрицательным инотропным и миокардиотоксическим действием).
Условно эволюцию ХНК можно представить в четыре периода (Т):
Т1 — начальный ответ на повреждение миокарда. Началом, ведущим к появлению ХНК, служит потеря критической массы миокарда (например, вследствие обширного постинфарктного кардиосклероза). Компенсаторные механизмы поддержания УOC: механизм Франка-Старлинга (по мере увеличения размеров левого предсердия повышается синтез ПНУП, снижающий нагрузку на сердце) и активация САС (повышается сократимость неповрежденного миокарда). Таким образом, начальная ХНК ¾ это состояние, при котором сердце способно выполнить насосную функцию в покое и неспособно выполнить ее, когда метаболические потребности организма значительно повышаются (при ФН). Явная патология сердца может длительное время оставаться компенсированной.
Т2 — появление симптомов ХНК, вследствие истощения и потери эндогенных компенсаторных механизмов. Из-за повышения гидростатического давления и повышения проницаемости сосудов жидкая часть крови выходит за пределы сосудистого русла, и возникают отеки. САС становится постоянно активной; сердце теряет способность преодолевать постнагрузку (хотя в нормальных условиях миокард ЛЖ высоко резистентен к увеличенной постнагрузке); идет потеря чувствительности сердца к b-адренергическим стимулам, и повышается чувствительность к a-адреностимуляции периферических сосудов.
Т3 — усиление проявлений явной ХНК. Нарушена пропульсивная способность сердца. Перфузия периферических органов сохраняется за счет системной вазоконстрикции (активация САС, РААС) и задержки натрия и воды. При дальнейшем прогрессировании ХНК нарушаются и другие виды обмена (в том числе и белкового), что приводит к дистрофическим изменениям органов и тканей с последующим нарушением их функции.
Т4 — прогрессирования ХНК. Формируется вторичное повреждение миокарда из-за: дисфункции и некроза ранее неповрежденных сегментов миокарда, даже в отсутствие рецидивов заболеваний, их вызвавших. Воздействие повышенного давления на желудочки сердца вызывает их ремоделирование. Длительная активация САС и РААС усиливает их отрицательные эффекты на миокард. В конечной стадии может развиться тяжелая кахексия, иногда маскируемая отеками, гипопротеинемия, дистрофия органов и тканей с нарушением их функции и декомпенсацией.
В последние годы произошла смена акцентов в патогенезе ХНК. Так, ранее доминировала точка зрения о том, что, в первую очередь, ХНК — это недостаточность систолической функции сердца плюс задержка натрия и воды. Поэтому больных с симптоматикой ХНК лечили комплексно сердечными гликозидами (СГ) и мочегонными. Несколько позже стали придавать большую роль периферическому звену кровообращения в генезе ХНК, поэтому в лечении доминировали периферические вазодилятаторы. В настоящее время полагают, что в основе развития ХНК и прогрессирования ее клиники преобладают нейрогуморальные нарушения (иногда они даже опережают значимые нарушения насосной функции сердца), поэтому и назначаются рано ингибиторы ангиотензинпревращающего фермента (ИАПФ), как патогенетически обоснованное лечение.
Клиника ХНК.Она вариабельна, от легкой до тяжелой, когда работа сердца не способна поддерживать жизнь больного без посторонней медицинской помощи. В целом, клиника зависит от многих факторов, включая возраст больного, этиологию болезни, ТФН. Многие симптомы ХНК — это результат накопления избытка жидкости в одном из кругов кровообращения: жидкость скапливается "позади" пораженного отдела сердца. Симптомы ХНК мало специфичны для этиологического диагноза ХНК, но они являются хорошим индикатором тяжести ХНК, ее динамики в ходе проводимого лечения.
Главные клинические критерии ХНК (по Браунвальду): 1) пароксизмальная ночная одышка (или ортопноэ); 2) набухание вен шеи; 3) хрипы в легких; 4) кардиомегалия; 5) острый отек легких; 6) ритм галопа при аускультации сердца; 7) повышение венозного давления более 16 см Н2О ст.; 8) гепатоюгулярный рефлекс (положительный симптом Плеша).
Малые критерии: 1) отеки лодыжек; 2) ночной кашель;3) одышка при ФН; 4) гепатомегалия; 5) плевральный выпот (гидроторакс); 6) снижение ЖЕЛ на 1/3 от должного; 7) ЧСС больше 120 в мин; 8) потеря веса более 4,5 кг в течение 5 дней лечения.
Определенный диагноз ставится при наличии 2-х больших симптомов или 1 большого и 2 малых симптомов.
Таблица 1
Симптомы ЛЖ и ПЖ недостаточности
Как правило, ЛЖ недостаточность является частой причиной ПЖ недостаточности в последующем (они сочетаются). Реже, в чистом виде ПЖ недостаточность… Обычные жалобы больного с ХНК:ДИФФЕРЕНЦИАЛЬНЫЙ ДИАГНОЗ ХНК
ХНК по ЛЖ типу ¾ ею чаще дебитируют: митральные пороки (стеноз и недостаточность), ГБ и симптоматические АГ.
ХНК по ПЖ типу ¾ею чаще дебитируют: стеноз легочной артерии, стеноз и недостаточность трехстворчатого клапана, ХЛС на фоне ХОЗЛ, перикардиты.
ХНК бивентрикулярного типа ¾ ею дебитируют: миокардиды, ДКМП, алкогольная миокардиодистрофия (например, "пивное сердце").
Таблица 2
Отличие ХНК от сосудистой недостаточности
Тесты, полезные для исключения альтернативных диагнозов ХНК: · рентгенография грудной клетки и ФВД ® болезни легких; ТЭЛА (у этих больных… · биохимический анализ крови, общий анализ мочи ® ХПН;Алгоритм лечения больных ХНК с систолической дисфункцией ЛЖ и явными симптомами
Поддерживающая терапия — комбинация: петлевой диуретик (+) нитраты (+) ИАПФ;… При выраженной декомпенсации и рефракторности ХНКк проводимой терапии (максимальные дозы фуросемида+ИАПФ+СГ) временно…Комментарии к лечению ХНК
а) начинают лечение с тиазидовых мочегонных (гипотиазид) — тормозят всасывание натрия и хлора в дистальных канальцах. Их используют в малых дозах… Если диуретический эффект недостаточен, то прибегают к: · комбинированию петлевых диуретиков и тиазидовых;ИНФЕКЦИОННЫЙ ЭНДОКАРДИТ
Первое описание клиники инфекционного эндокардита (ИЭ) (ранее ¾ бактериальный или затяжной септический эндокардит) дали Крайзинт в 1815 г., а… ИЭ протекает по типу сепсиса с закономерно выявляемой циркуляцией в крови… Распространенность ИЭ. За последние 20 лет частота ИЭ увеличилась более чем в 3 раза (истинную частоту трудно…Ведущие возбудители ИЭ, в зависимости от ряда факторов
Золотистый стафилококк, нейсерия гонореи и менингита, гемофильная палочка обычно вызывают развитие острого ИЭ вследствие их высокой инвазивности.… В настоящее время довольно часто(в 50-70% случаев) определяются стерильные… · исследование крови в безлихорадочной (безмикробной) стадии ИЭ (нет повышения температуры и ознобов);Рис. 3. Схема патогенеза ИЭ.
Нормальный эндокард устойчив к прилипанию инфекции. Вторым моментом является наличие патологии сердца. Так, существенная роль в формировании ИЭ принадлежит предрасполагающим факторам (обнажающим поверхность эндотелия): порокам клапанов сердца (с регургитацией тока крови, увеличением скорости кровотока, наличием высоких градиентов давления (ток из камер сердца c увеличенным давлением в камеры с уменьшенным давлением), микротравм, нарушений гемодинамики внутри сердца и микроциркуляции. В результате макро- или микротравматизации эндокарда изменяется его поверхность ("оголяется" базальная мембрана или строма клапана). Травма эндокарда ¾ это главный механизм (тригер), индуцирующий ИЭ, это сигнал для отложения тромбоцитов и фибрина в зонах поражения (интерстициальный вальвулит) с образованием стерильных тромботических вегетаций. Возникает небактериальный, стерильный тромбоэндокардит. На них позднее лучше осаждаются микробы. Таким образом, для развития инфекционного очага в эндокарде недостаточно наличия бактериемии. Необходимо повреждение эндокарда (изменение реактивности эндотелия, дегенерация и десквамация его, образование вегетаций на клапанах и эндокарде, ¾ все то, что способствует проникновению инфекционных агентов) вследствие разницы давления, узости отверстия и изменения скорости кровотока. Они создают условия, благоприятствующие внедрению инфекционных агентов в эндокард с тромботическими вегетациями и образованием инфекционного очага (возникает ИЭ). Два фактора являются решающими в возникновении ИЭ ¾ бактериемия и повреждение эндотелия.
После внедрения микроба в ткань миокарда, в этой зоне дополнительно откладываются тромбоциты и фибрин в виде рыхлых и непрочных отложений (вегетаций), которые препятствует действию на микробы циркулирующих лейкоцитов, макрофагов и АБ. Эти отложения являются хорошей средой для роста микробов, формируя защитный слой, "одеяло". Вегетации плохо васкуляризированы, поэтому замещаются грануляционной тканью. Все это "закрывает" микроб от действия факторов внешней среды (терапии АБ) и позволяет ему выжить даже после многомесячного лечения АБ. В отсутствие лечения АБ, последовательные циклы отложений приводят к росту вегетаций, состоящих из тромбоцитов, фибрина и колоний микробов.
Вместе с тем, периодически микроб может проникать в периферическое русло, ткани и органы макроорганизма. Высокопатогенные микробы вызывают быструю (за несколько недель) деструкцию клапанов (язвенно-тромботические изменения и разрушения) с развитием их недостаточности. Менее патогенные микробы (чаще бывает при эндогенной инфекции) приводят к развитию затяжного ИЭ и вегетаций (полипозно-язвенные или бородавчато-язвенные изменения), что более характерно для вторичного ИЭ или уже леченного ИЭ. Клапаны сердца покрываются грязно-желтым налетом, грязно-зелеными, мягкими и рыхлыми массами. Затем идет их отторжение с образованием глубоких язв (язвенный эндокардит). На дне и по краям язв обильно выявляются тромботические отложения в виде полипозных разрастаний (полипозный эндокардит) с видом "цветной капусты" или "сифилитических кандилом". Эти вегетации (разрастания) со временем могут отрываться, образуя эмболы, которые в последующем вызывают тромбоэмболические осложнения, приводя к развитию септических инфарктов, абсцессов внутренних органов (легкие, сердце, почки, мозг, селезенка, печень). Например, если из левых камер ¾ появляются эмболии мозга, селезенки, почек, коронарных и мезентериальных артерий; если из правых камер ¾ инфаркт и абсцесс легких.
Формирование локальных очагов инфекции является пусковым механизмом генерализации процесса: формируется иммунокомплексная патология (макроорганизм вырабатывает антитела против Ig G и M) с вовлечением многих органов и сосудов: иммунные комплексы откладываются в определенных органах, что клинически проявляется как нефрит, васкулит, гепатит, миокардит и др. Дальнейшая эволюция ИЭ сопровождается присоединением дистрофических изменений внутренних органов.
Таким образом, можно выделить следующие патогенетически значимые процессы в организме при ИЭ:
· Постоянное поступление микроба в кровяное русло с развитием эпизодов бактериемии и появлением симптоматики: усталость, анемия, снижение массы тела и аппетита, лихорадка, появление метастатической инфекции и увеличение размеров селезенки (вследствие удаления микробов из крови ее ретикуло-эндотелиальной системой).
· Местное развитие микробных вегетаций (этому предшествует изменение ткани клапанов и формирование пристеночного эндокардита) и нарушение функционирования сердца (абсцессы фиброзного кольца клапана и его перфорация).
· Отрыв фрагментов микробных вегетаций (размер эмболов может быть различным) из правых или левых камер сердца с развитием эмболий и последующих септических инфарктов.
· Одновременное присутствие в системе кровотока антигенов микроба, фиксированных на клапанах сердца и антител к нему (при наличии длительной внутрисосудистой инфекции) приводит к стимуляции иммунной системы (клеточного и гуморального иммунитета): повышается титр антител к микробам, формируются циркулирующие иммунные комплексы (ЦИК ¾ содержащие Ig G, A, M и комплемент), которые откладываются в разных органах и тканях, повреждая их. Впоследствии формируются: нефрит, миокардит, васкулит, артрит. Только при поздней диагностике ИЭ и отсутствии адекватной терапии АБ выявляется клиника генерализованного сепсиса.
Различают 4 патогенетические фазы ИЭ в организме:
1. Доклиническая: имеется патогенная инфекция в организме, изменена реактивность эндокарда, формируется интерстициальный вальвулит и тромботические вегетации на клапанах.
2. Инфекционно-токсическая(чаще имеются лишь признаки неспецифической инфекции и изменения сердечно-сосудистой системы): бактериальное поражение клапанов с микробными тромботическими вегетациями (может появиться шум в сердце, если ранее не было порока сердца); эндокардит с бактериемией, лихорадкой, тромбоэмболиями, инфарктами, абсцессами внутренних органов. Нередко больные в эту фазу "лечат себя сами" от ОРЗ, гриппа или других болезней.
3. Иммунно-воспалительная (с развернутой клиникой ИЭ). Формируется иммунная генерализация процесса (развитие иммунокомплексной патологии) с экстракардиальными проявлениями: иммунокомплексный нефрит, миокардит, гепатит; поражения: легких (инфаркт с пневмонией), ЦНС (менингоэнцефалит), крови и костного мозга (панцитопения, лейкемоидные реакции).
4. Дистрофическая. Тяжелые, необратимые, дистрофические изменения во внутренних органах и формирование их функциональной недостаточности (например, прогрессирует ХНК на фоне сформировавшегося порока сердца или формируется ХПН).
Клинические симптомы ИЭ являются результатом:
· локального, внутрисердечного инфекционного процесса и его осложнений (перфорация клапанов, разрыв хорд, межжелудочковой перегородки, сосочковых мышц);
· тромбоэмболий (или септических эмболизаций) фрагментами вегетаций в разные органы;
· постоянной бактериемией с обсеменением периферических фокусов;
· формирования ЦИК и связанных с этим заболеваний.
В случае острого течения ИЭ (по типу острого сепсиса) и наличия очевидных входных ворот инфекции (например, операции, криминальный аборт), иммунно-патологические реакции не успевают развиться. Выражены лишь симптомы септикопиемии. В этом случае ИЭ можно считать синдромом сепсиса. Лишь позднее, при формировании в эндокарде инфекционного очага, он начинает оказывать решающее влияние (играет самостоятельную роль и поддерживает патологический процесс) на течение болезни как источник септицемии, сенсибилизации организма и многочисленных опосредованных органных проявлений.
Клиника ИЭ полиморфна и зависит от вирулентности микроба, состояния макроорганизма и варианта ИЭ (первичный или вторичный). В настоящее время терапевтическая симптоматика ИЭ заметно изменилась, больные с классическими симптомами ИЭ (лихорадка, спленомегалия, шум в сердце, периферическая эмболизация и позитивные посевы крови) стали редкими. Обычно (до появления явного шума в сердце) начальная диагностика ИЭ трудна, чаще всего больному ставят следующие диагнозы: "пневмония?, сепсис? или острая ревматическая лихорадка?".
В клинике ИЭ имеется три основных компонента болезни: интоксикация; нарушения гемодинамики (из-за поражения клапанов); специфические осложнения (тромбоэмболии, васкулиты). Симптоматика ИЭ обусловлена 4 ведущими патофизиологическими механизмами: инфекцией сердечных клапанов и окружающих их структур, метастатической инфекцией, отдаленной эмболизацией и ее последствиями, продукцией ненормальных Ig, ЦИК и их отложением в разных органах.
Варианты начала ИЭ могут быть следующие:
· по типу острого инфекционного заболевания;
· постепенное (типичное) начало;
· появление немотивированных тромбоэмболий (в мозг, почки, селезенку);
· появление симптомов диффузного гломерулонефрита (гематурия, протеинурия, отеки, повышение АД).
Развернутая клиническая картина ИЭ обычно возникает через 2 недели после бактериемии (средний период инкубации составляет около 1 недели) и включает сразу общие симптомы: лихорадку (или субфебрилитет), ознобы, потливость, кожные высыпания (сосудистые проявления). Затем, постепенно появляются поражения сердца (дефекты клапанов с шумами), почек, гиперспленизм, изменения крови (но они не всегда отчетливо выражены) и осложнения. Нередко ИЭ протекает атипично (нет полного набора классических симптомов). По основному клиническому синдрому ("маске") выделяют следующие формы ИЭ: спленомегалическую; гепатолиенальную; почечную (симптомы острого диффузного гломерулонефрита); тромбоэмболическую (чаще в мозг, селезенку, почки); ишемическую или с преобладанием ХНК; церебральную (резкая сонливость, нарушение сознания, психоз); сосудистую и др.
Ведущими классическими, клиническими синдромами ИЭявляются:
· инфекционно-токсический (лихорадка, кожные высыпания, изменения кожных покровов, общая слабость, снижение трудоспособности, артралгии, артриты);
· поражения сердца - повреждение эндокарда (формирование пороков) и миокарда;
· поражения сосудов (васкулиты, в том числе и тромбоэмболические поражения);
· поражения почек (инфаркт, диффузный нефрит);
· поражения селезенки и печени (гепатолиенальный);
· церебральный (от астено-вегетативных изменений до менингоэнцефалита);
· ишемический (или с доминированием сердечной недостаточности);
· кардиогепаторенальный;
· лабораторный (острофазовые сдвиги, положительная культура крови).
Лихорадкапри ИЭ - наиболее частый, ранний и важный симптом болезни, встречается почти у 90% больных (табл. 5). Характер и варианты повышения температуры тела больного могут быть различными (характерной температурной реакции при ИЭ нет). Нет и связи лихорадки с катаральными симптомами. Обычно лихорадка при остром ИЭ ¾ гектическая, при подостром ¾ неправильная, а при хроническом течении ИЭ ¾ субфебрильная. Можно выделить следующие частые варианты лихорадки:
· внезапное повышение температуры до 40оC по типу острого инфекционного заболевания (это характерно для стафилококкового ИЭ) с лихорадкой гектического типа (озноб, прострация, слабость, разбитость, артралгии, интенсивное потоотделение);
· субфебрильное повышение температуры с волнообразной лихорадкой (сопровождающейся неадекватными профузными потами после понижения температуры и выраженными ознобами при повышении температуры). Температура повышается на несколько дней (и даже часов). Это более характерно для вторичного ИЭ или стрептококкового ИЭ. На фоне повышения температуры прощупываются увеличенные печень и мягкая селезенка. В этот период чаще высеваются микробы из крови;
· нет повышения температуры, безлихорадочное течение ИЭ ¾ обычно отмечается у пожилых больных с тяжелой ХНК на фоне старых пороков сердца или "хроников-почечников" с выраженной ХПН.
Возможны и другие варианты лихорадки при ИЭ:
· 2-3 недели повышенная температура тела, потом 1-2 недели ¾ нормальная;
· "свечи" до 40оC на фоне постоянного субфебрилитета в течение 1-2 недель;
· повышение температуры до 39-40оC в течение 1-2 дней на фоне нормальной или субфебрильной температуры.
Таблица 5
Частота клинических данных при ИЭ
Могут поражаться все три слоя сердца. Клинические симптомы эндокардита зависят от варианта ИЭ: первичный (кардиальный шум отмечается в 99% случаев)… Лишь у 10% больных ИЭ изолированно поражается митральный клапан. Диагностика… При перфорации створок митрального и аортального клапанов появляются музыкальные систолические шумы в виде…Классификация ИЭ
| Этиология | Патогенети-ческая фаза | Вариант течения | Степень активности | Клинико-морфологи-ческая форма | Ведущая органная патология |
| Бактериальный, вирусный, грибковый | Инфекционно-токсическая, иммунно-воспалительная, дистрофическая | Острый (до 6 недель), под-острый (от 2 месяцев до 1 г), хронический рецидивирующий (от 1 до 7 лет) | Высокая (3 степень), умеренная (2 степень), минимальная (1 степень) | Первичный, вторичный | Сердце, почки, печень, легкие, сосуды, ЦНС, селезенка |
В настоящее время полагают, что деление ИЭ на острый и подострый достаточно условно, так как четкую границу между этими двумя полюсами клинического течения ИЭ провести довольно трудно (клиника ИЭ изменяется под действием лечения АБ). Так, больные с острым ИЭ могут переходить в подострый в ходе лечения, и, наоборот, у больных с подострым ИЭ может неожиданно развиться острый ИЭ с опасными для жизни осложнениями (перфорацией клапанов сердца и формированием тяжелой сердечной недостаточности). Поэтому многие клиницисты предлагают такое деление ИЭ отменить.
Острый ИЭ в типичных случаях протекает с клиникой острого сепсиса (с агрессивным течением). Это характерно для первичных форм (у ранее здоровых людей). Но так может проявляться и вторичный ИЭ на фоне ревматических пороков у молодых лиц. Острый ИЭ вызывается высоковирулентными микробами (например, золотистым стафилококком), их нередко обнаруживают при посеве крови. Острый ИЭ начинается резко с: выраженной интоксикации в 100% случаев (слабость, головная боль, миалгии); гектической лихорадки в 100% случаев (с перепадом температур более 2оC и с двумя пиками повышения температуры в течение дня), потрясающих ознобов и потливости; с острофазовых сдвигов в анализах крови (лейкоцитоз со сдвигом влево; повышение СОЭ).
На этом фоне часто развиваются: септические осложнения (абсцессы) вследствие гнойных метастатических инфекций (эмболический синдром); пневмония (40%), гепатит (40%), увеличение селезенки (30%), менингит (8%), поражение почек. Довольно часто поражается кожа рук (многочисленные петехии, узелки Ослера, пятна Лукина и Джейнуэя) и суставы (по типу полиартралгии, артритов). Острый ИЭ чаще вызывается золотистым стафилококком и пиогенным стрептококком. В более, чем 40% случаев выявляется положительная гемокультура. Деструкция клапанов сердца может осложниться разрывом хорд клапана или перфорацией створок клапана, приводя к быстрому развитию сердечной недостаточности.
Можно выделить два варианта острого ИЭ:
· начинается как острый сепсис различного генеза (чаще стафилококкового), лихорадка без лечения длится несколько дней (или недель). Этот сепсис на определенном этапе приводит к поражению клапанов (отмечаются более крупные вегетации на клапанах и, естественно, чаще осложнения);
· острый ИЭ, приближающийся по симптоматике и закономерностям к подострому ИЭ.
Вторая, более частая форма ¾ подострый ИЭ (с затяжным течением), который вызывают менее вирулентные микробы (зеленящий стрептококк). Преобладает (в 2/3 случаев) вторичный ИЭ у лиц с сопутствующим поражением сердца (ревмопороки ¾ в 40-60% случаев, реже ¾ врожденные пороки сердца). Для подострого ИЭ характерны: более длительное течение (от 2 до 9 месяцев без лечения), наличие мелких вегетаций (3 мм в диаметре и менее) и реже встречающиеся осложнения. Подострый ИЭ может протекать с типичной клиникой: симптомами интоксикации (в 66% случаев), лихорадкой (чаще, в 90% субфебрильная), повышенной потливостью (иногда с ознобами). Выявляются: узелки Ослера, петехиальная сыпь (малого размера, красного цвета на слизистой рта, конъюнктиве и передней поверхности грудной клетки), пятна Лукина, изменения ногтевых фаланг. Могут отмечаться боли в спине, суставах, плече. При развитии ИЭ вследствие в/в введения лекарств (наркотиков) часто появляются: плевральные боли, кашель, одышка из-за развития инфаркта легких (важный симптом ИЭ трехстворчатого клапана).
Подострый ИЭ обычно начинается постепенно, больные не могут точно назвать время появления симптоматики. У ряда больных ИЭ предшествуют: недавнее удаление зуба, вмешательства на уретре, тонзилэктомия или другие манипуляции. Частота септических осложнений при этом ИЭ сравнительно небольшая (могут быть параличи, боли в грудной клетке (из-за миокардита или инфаркта легкого), головные боли (из-за метастатических инфекций в мозг, оболочку); мозговые эмболии или разрывы микотической аневризмы могут проявляться клиникой инсульта.
Можно отметить: большую гематурию (из-за гломерулонефрита или эмболии почек), симптомы "острого живота"; жалобы на похолодание ног из-за эмболии крупных артерий. Эмболии могут поддерживать инфекционный процесс. При физикальном обследовании сердца можно выявить разные симптомы. Например, проявления ОИМ, как результат эмболизации коронарных артерий сердца, причем в ранний период ИЭ проявлений ОИМ вообще может и не быть. Положительный посев крови отмечается в 35% случаев (чаще выделяют зеленящий стрептококк и эпидермальный стафилококк). В целом, все клинико-лабораторные показатели менее выражены по сравнению с острым ИЭ.
Хронический, рецидивирующий ИЭ характеризуется нерезко выраженной клиникой. Могут быть субфебрильная температура, редкие познабливания, небольшая интоксикация (в 50% случаев). В большей степени выражена иммунокомплексная патология внутренних органов (нефрит ¾ в 30%; миокардит ¾ в 20%; артриты ¾ в 50% случаев), могут быть тяжелые осложнения (геморрагические инсульты, тромбоэмболии, разрывы микотических аневризм). Нередко отмечается атипичное течение данного ИЭ с моносиндромным поражением внутренних органов. Например, выраженный нефротический синдром или синдром поражения ЦНС, или синдром ХНК с или без лихорадки.
Лабораторные данные при ИЭзависят от фазы и остроты процесса.
1. Общий анализ крови:
· может быть умеренная гипохромная анемия (Нв менее 90 г/л) у 60-80% больных, которая усиливается по мере прогрессирования болезни (из-за наличия гемолитического фактора и почечной недостаточности, угнетающих кроветворение), появляются пойкилоцитоз, анизоцитоз, ретикулоцитоз и базофильная зернистость эритроцитов. Прогрессирование анемии связано с неблагоприятным течением болезни. При остром ИЭ анемия бывает редко.
· число лейкоцитов варьирует: может быть в норме, но со сдвигом влево, уменьшаться или увеличиваться (обычно в инфекционно-токсической фазе, почти всегда при остром ИЭ, или стафилококковом ИЭ или при развитии осложнений). Нередко лейкоцитоз сменяется лейкопенией (до 3×109 л).
· почти всегда повышается СОЭ (различной степени, иногда повышается до 80 мм/ч и более). СОЭ может оставаться высоким даже через несколько недель после успешной АБ терапии.
· может быть умеренная тромбоцитопения.
2. Биохимический анализ крови:
· у 1/4 больных выявляются диспротеинемия (уменьшение альбуминов и повышение глобулинов за счет повышения a2 и j фракций); положительные осадочные пробы (формоловая, тимоловая); могут повышаться билирубин (при остром стафилококковом ИЭ), ЦРБ, сиаловые кислоты.
· повышаются сывороточные Ig и титр ЦИК (у 80-90% больных), особенно при подостром ИЭ.
· могут определяться ложноположительная RW (из-за изменения белкового спектра сыворотки) и положительный ревматоидный фактор (у 30-50% больных с подострым ИЭ).
3. Наиболее значимым в верификации ИЭ является бактериологическое исследование крови до назначения АБ. У 40-60% больных можно выявить возбудитель и определить его чувствительность к АБ. Диагностичным для ИЭ считается положительная гемокультура в трех порциях (позитивный результат в одной из порций не имеет диагностического значения). Исследование на стерильность крови должно проводится несколько раз в стерильных условиях: на высоте лихорадки и пятикратно в течение суток, с 2-х часовым интервалом. Для ИЭ характерна бактериемия длительностью не менее 1 ч. Если у больного ИЭ высеян пневмококк, а пневмонии ¾ нет, то это с большой вероятностью указывает на ИЭ. Выявление в культуре крови коагулазо-негативного стафилококка при отсутствии в/в катетера также определенно указывает на ИЭ. Обычно при остром ИЭ взятие крови на гемокультуру проводят в течение 1 часа, после чего начинают терапию АБ. При подостром ИЭ нет необходимости в немедленном лечении АБ (болезнь протекает уже несколько месяцев), поэтому при отрицательной пробе на гемокультуру, лечение АБ временно (на 5-7 дней) прекращают и проводят повторные исследования крови. Культура крови может стать положительной через 24 ч ¾ 2 недели после отмены АБ (в зависимости от АБ и длительности АБ терапии). Поэтому, если АБ давали всего 2-3 дня, то после прекращения лечения культура крови может быстро стать положительной. Если лихорадящий больной ИЭ лечится АБ, то посев крови берут за 2-3 ч до введения АБ.
4.Анализ мочи. При ИЭ он чаще патологический. Можно выявить: микрогематурию (реже ¾ макрогематурию), небольшую протеинурию и цилиндурию.
5. При ЭхоКГу 50-80% больных обнаруживаются: обширные вегетации (но если их размер менее 2 мм, они не выявляются), кальцинаты различных участков эндокарда плюс симптомы деструкции клапанов. Вегетации обычно появляются через 2 недели при остром ИЭ и через 6-8 недель при хроническом ИЭ. Наличие вегетаций является симптомом высокого риска осложнений.
6. ЭКГвыявляет диффузные нарушения миокарда (неспецифические нарушения реполяризации); может быть ишемия миокарда (15%), вплоть до ОИМ (5%); нарушения ритма и проводимости.
Согласно Демина (1978) выделяют следующие диагностические критерии ИЭ:
· инфекционно-токсической фазы:
А. Клинические: лихорадка, озноб, кожные геморрагические и некротические высыпания, миалгии, церебро-васкулярные повреждения, появление шумов в сердце или их изменение (формирование порока), увеличение размеров селезенки.
Б. Лабораторные: положительный посев крови, рост СОЭ, и титра антител к бактериальному антигену.
· иммунно-воспалительной фазы:
А. Клинические: диффузный гломерулонефрит, гепатит, миокардит, спленомегалия, васкулиты, утолщение концевых фаланг пальцев, артриты и артралгии, снижение лихорадки после назначения ГКС.
Б. Лабораторные: ЦИК, иммунно-комплексные отложения в почках, миокарде, сосудах; тромботические вегетации; повышение уровня j-глобулинов, повышение фибриногена; симптомы анемии; появление противотканевых почечных антител (противопеченочных и кардиальных).
Диагностика ИЭ, согласно критериев Дюкского университета (США, 1994).
Определенный ИЭ:
· Патологические критерии: положительный посев крови (или гистологическое выявление микроба в вегетациях или во внутрисердечных абсцессах); патологические повреждения (вегетации или абсцессы внутри сердца, подтвержденные гистологически и указывающие на активный эндокардит).
· Клинические критерии:
Большие: в двух пробах, устойчивая позитивная культура крови (выявление типичных микробных возбудителей ИЭ ¾ зеленящий стрептококк; золотистый стафилококк; гемофильная палочка), доказательства поражения эндокарда (по ЭхоКГ).
Малые: наличие предрасполагающих факторов (патология сердца), лихорадка более 38оC, сосудистые (эмболии больших артерий, инфаркты, кровоизлияния, пятна) и иммунологические феномены (гломерулонефрит, пятна Ослера), ЭхоКГ и микробиологические доказательства позитивной культуры крови (микробы иные, чем выше названные).
В пользу ИЭ будут свидетельствовать: 2 больших критерия (чаще ¾ в 60%) или один большой и три малых (в 36%) или 5 малых критериев.
В целом диагноз ИЭ ясен, если имеются: положительный посев крови, характерные клинические изменения и данные ЭхоКГ (вегетации на клапанах). Средний срок постановки диагноза ИЭ колеблется от 1 до 2-х месяцев.
Осложнения ИЭ(чаще встречаются при остром варианте):
· инфекционно-токсический шок;
· ДВС-синдром;
· повреждения клапанов с формированием ОЛЖН или ХНК;
· абсцессы миокарда;
· нарушения ритма и проводимости сердца;
· микотические (септические) аневризмы сосудов (чаще, в 20% при подостром ИЭ);
· поражения почек с формированием ОПН или ХПН;
· тромбозы или эмболии (при остром ИЭ ¾ до 60%)
· рецидивирование ИЭ.
Дифференциальный диагноз. ИЭ является причиной многочисленных диагностических ошибок вследствие неспецифичности симптоматики. Так, на до госпитальном этапе частота ошибок составляет около 40%, причем только 30% больных направляются в стационар с правильным диагнозом и то, часто через 1 месяц и более от начала болезни. В поликлиниках ИЭ часто не диагностируют, больной с ИЭ долго лечится по поводу: "ОРЗ", "пневмонии" или "рецидивирующего гриппа". Причина ошибок отчасти кроется в плохом знании врачами современной диагностики ИЭ и его течения (в частности наличии "неполной" клинической картины), особенно на фоне ревматических пороков. Так, часто недооценивается первичная симптоматика после отрицательных посевов крови. Обычно такие симптомы, как повышение размеров селезенки, поражения сердца, мозговые и почечные эмболии появляются позже.
В последние годы клиника ИЭ изменилась: часто нет заметного повышения температуры или иногда при высокой и длительной лихорадке, долгое время (несколько месяцев) клинически не проявляется поражение клапанов сердца. Иногда в течение многих месяцев может быть поражение только одного органа (создавая "впечатление" нефрита, гепатита), то есть, нет системности поражения. Таким образом, ИЭ должен подозреваться у больного:
· со значительным шумом в сердце и повышением температуры в течение недели и больше;
· без шумов в сердце, но с постоянным повышением температуры, если ранее ему в/в вводились лекарства;
· леченного АБ с положительной динамикой симптомов (понижение температуры и недомогания), если после прекращения АБ терапии симптомы возобновляются;
· с появлением, усилением шума в сердце на фоне лечения АБ (или после окончания курса).
Очень много ошибок делается в дистрофической фазе ИЭ, когда необходимо правильно оценить причины, приведшие к ХНК, резистентной к терапии. Так, у больных вторичным ИЭ и с выраженной ХНК наличие симптомов выраженной активности патологического процесса и рефрактерность к проводимому лечению (наряду с другой симптоматикой) заставляют подозревать ИЭ. При 1-й фазе (инфекционно-токсической) дифференциальный диагноз проводят с рядом инфекционных заболеваний или злокачественных лимфом. Во 2-й фазе (иммунно-воспалительной), когда имеется развернутая клиника ИЭ, ошибки могут быть обусловлены:
· неумением найти системность поражения (повышение температуры плюс симптомы поражения сердца, почек, селезенки и др.), один из имеющихся симптомов рассматривается, как болезнь;
· плохой аускультацией сердца (не слышат формирование аортальной или митральной недостаточности), не обращают внимание на "необычный симптом" (васкулит, геморрагии, тромбоэмболии);
· неправильная оценка резистентности к терапии АБ у больных ревмопороками и ХНК;
· изменением клиники ИЭ под действием ГКС и АБ.
Чаще дифференциальный диагноз проводят с активным ревматизмом (острой ревматической лихорадкой), СКВ или узелковым панартериитом (УПА) и реже со злокачественными опухолями (раком толстой кишки и поджелудочной железы; гипернефромой, лимфогранулематозом), сопровождающимися высокой лихорадкой, а также с миеломной болезнью (табл. 7, 8).
Таблица 7
Критерии отличия ИЭ от активного ревматизма с пороками клапанов и СКВ
Таблица 8 Дифференциальные отличия подострого ИЭ и ревматического эндокардита (острой ревматической лихорадки) …СЕПСИС В КЛИНИКЕ ВНУТРЕННИХ БОЛЕЗНЕЙ
Сепсис (С) является актуальной общеклинической проблемой, которая всегда привлекала внимание врачей. Так, экономические затраты на лечение одного… Определение. С (от греческого "гниение") ¾ это… Таким образом, С можно охарактеризовать как системный ответ на инфекцию (имеет те же клинико-лабораторные признаки,…Классификация и терминология С
Условно можно выделить три клинико-патогенетические формы С:
· септицемия ¾безметастатический вариант С. Встречается у 1/4 больных. Это патологическое состояние характеризуется наличием и размножением микробов в крови. Из-за нечеткости формулировки этот термин в настоящее время не имеет широкого употребления. Тяжесть септицемии прямо пропорциональна масштабам гнойно-некротических процессов в первичном очаге, а также количеству и вирулентности микроба.
· септикопиемия(истинный С, встречается у 1/3 больных) характеризуется наличием гнойно-некротических метастатических очагов в разных органах (легкие, почки, селезенка, мозг и др.) на фоне имеющейся клинической симптоматики септицемии. Термин септикопиемия также не является четким и в настоящее время используется редко.
· септический эндокардит (острый или хронический) - классический пример "терапевтического С", при котором основной септический очаг находится в эндокарде (чаще на клапанах сердца). Термин "терапевтический С" указывает не на происхождение С, а на нуждаемость больного в консервативном лечении.
· тяжелый С характеризуется функциональными нарушениями со стороны органов (органная дисфункция) и тканей, гипотонией (снижением АД систолического менее 90 мм рт. ст. или АД более, чем на 40 мм рт. ст. от среднего АД, при отсутствии других причин для гипотонии). Возможны также наличие лактоацидоза, олигоурии и нарушение сознания;
· СШ ¾это осложнение, тяжелый С плюс наличие артериальной гипотонии. Этот шок развивается несмотря на проводимую перфузионную терапию. При этом состоянии отмечаются: лактоацидоз, гипоперфузия тканей, олигоурия, нарушение сознания, полиорганная недостаточность. Течение СШ молниеносное с высокой летальностью.
ПервичныйС развивается на фоне полного здоровья (когда микроб попадает в условия конкуренции с относительно сохранным иммунитетом макроорганизма, что обуславливает некоторую характерность симптоматики (несмотря на ее многообразие). С может быть вторичным, когда развивается на фоне тяжелой предшествующей патологии (декомпенсированный СД, цирроз печени, ХПН и др.). Большая часть С должна трактоваться как вторичный, как осложнение местных нагноительных процессов, при котором септический очаг развивается из обычного очага инфекции (как при гнойном отите, фурункулезе или ангине). Позднее появляется разница между тяжелым общим состоянием больного и умеренными изменениями в первичном очаге. При вторичном С микроб попадает в условия иммуносупрессии, что благоприятствует его размножению в высоком темпе.
С распределяется по месту "входных ворот" инфекции (в зависимости от локализации первичного септического очага) следующим образом:
· чрезкожный (в 30-60% случаев): постинфекционный из абсцесса ягодиц или мелких ран, фурункулов. Поэтому у пожилых лиц, с заведомо имеющимся вторичным иммунодефицитом (на фоне хронических заболеваний), в/м введение лекарств не по жизненным показаниям является ошибкой. Хотя, многие из этих больных любят лечиться "уколами и капельницами". Иногда наблюдается синус-тромбоз С, при котором инфекция попадает из мелких кожных гнойничков (при выдавливании прыщей) в кровь бассейна лицевой угловой артерии (соответствует области ниже бровей). При этом варианте С быстро развиваются: гнойный менингит, пневмония, отек век и экзофтальм с отеком половины носа на стороне поражения;
· оральный (тонзиллогенный ¾ ангина "ушла", а С "остался"). Частый вариант этого С ¾ одонтогенный, с выходом бактерий в кровоток из инфицированных зубов (кариес, хронический пульпит и перидонтит);
· отогенный (часто вызывает тромбоз сигмовидного синуса) с наличием первичного септического очага в ушах вследствие обострения хронического отита;
· генитальныйвследствие криминального аборта, родов, обострения хронических воспалительных процессов женской половой сферы;
· криптогенный (в 15-20% случаев) ¾ неуточненной этиологии (при жизни больного нельзя обнаружить первичный очаг С);
· ангиогенный, ятрогенный(в 1-2% случаев)¾частовозникает после катетеризаций подключичной, яремной вен, протезирования клапанов сердца.
· урогенный(около 1%)вследствие калькулезного хронического пиелонефрита с нарушением оттока мочи. Этот вид С обычно вызывается Гр(¾) флорой и плохо лечится;
· холангиогенный(около 1%) при котором входными воротами анаэробного С может быть желчный пузырь с симптомами умеренного воспаления;
· бронхолегочный(около 1%) вследствие наличия бронхоэктазов, пневмонии, абсцесса легких.
Терапевт чаще всего встречается с С, при котором вопрос о первичном очаге приходится решать на основании умозаключений или по результатам вскрытия больного. Как правило, поиск этого первичного очага С ("входных ворот") бывает безуспешным или же выявление этого очага является весьма сложной задачей. В целом "входные ворота" терапевтического С выявляются не более, чем у половины больных. Часто внедрение септической инфекции может быть эндогенным (например,микрофлора рта, носа, дыхательных и мочевых путей), при нарушении местных защитных механизмов, что и является причиной генерализации инфекции.
По течению С разделяют на:
· молниеносный(острейший) с полным развитием и смертью за несколько первых часов или суток. Этот вариант С протекает как септицемия (развивается из одного очага), метастатические очаги не успевают появиться. Клинические признаки молниеносного С: бурная лихорадка, раннее развитие сердечной недостаточности, страх смерти, деструктивная сыпь (геморрагическая, постулезная) с тенденцией к слиянию, раннее появление признаков деструкции органов и СШ;
· острый (удельный вес составляет 60-80%), который развивается в течение первых 2-х месяцев и характеризуется определенной этапностью течения: септицемия®септикопиемия. В классическом варианте у больного имеются: стойкая лихорадка, частая лимфоаденопатия, спленомегалия и деструктивная сыпь;
· подострый (затяжной), который длится от 2 до 6 месяцев. Обычно данный вариант С пролонгируется септицемией вследствие малой эффективности АБ. Последние, сдерживая развитие микроба, не могут ликвидировать септический очаг. Развивается эффект "подлечивания";
· хрониосепсис(удельный вес менее 10%) развивается после 6 месяцев. Эта форма С очень трудна для диагностики, но зато есть время врачу подумать над предполагаемым диагнозом С. Хрониосепсис, как исход острого, развивается у 1/4 больных, а у 3/4 ¾ он имеет первично-хроническое течение (с длительным субфебрилитетом и стойкой бактериемией) вследствие поражения внутренних органов (а не первичного очага). Обычно этот вариант С обусловлен генерализацией условно патогенной стафилококковой инфекции, при которой санация первичных очагов не приводит к выздоровлению больного. Как правило, у этих больных имеются в анамнезе наличие в разных органах гнойных очагов, которые не проявляют себя остро, но способны длительное время поддерживать воспалительные реакции.
Условно (четких временных стандартов течения С нет) можно выделить три периода острого С:
1. Ранний С (от 5 дней до 2 месяцев; чаще 6-15 дней), где ведущим патогенетическим звеном является микробная интоксикация. Самочувствие больного может быть обманчиво хорошим. В часы, когда нет лихорадки, интоксикация исчезает и больной может даже работать.
2. Запоздалый С ¾ к микробной интоксикации присоединяется тканевая. С точки зрения клиники отсутствуют периоды, когда температура тела бывает нормальная (повышена постоянно) и появляются значительные нарушения органов и систем.
3. Поздний С, когда на первый план выступает полиорганная недостаточность (обусловленная далеко зашедшим ДВС-синдромом) с наличием постоянных симптомов общей интоксикации.
Этиология С (возбудитель высевается не всегда).В РБ в генезе С преобладают Гр(+) стафилококки (в 80% случаев), из них золотистый ¾ в 60%, а эпидермальный ¾ в 20% случаев. На Гр(¾) С приходится до 30-40% случаев. В США, наоборот, С чаще вызывается Гр(¾) флорой (синегнойной и кишечной палочками или анаэробной). Большая часть Гр(¾) бактерий, вызывающих С, ¾ нормальные обитатели ЖКТ. Эти бактерии потом могут мигрировать из брюшной полости в мочевые ходы или желчный пузырь. Гр(¾) бактериемия следует после выхода инфекции из первичного фокуса (мочеполового тракта, желчных ходов, костей или суставов). Обычно бронхогенный и чрезкожный (после фурункула) С вызван стафилококком, урогенный (после катетеризаций) ¾ Гр(¾) флорой (кишечной палочкой), одонтогенный (после удаления зуба) ¾ зеленящим стрептококком. Так, по данным центра сепсиса в Грузии (проф. Бочарошвили) в зависимости от вида С, выделяли следующие микробы (%), вызвавшие его развитие.
Таблица 9
Этиология сепсиса
СШ вызывается в 60-70% случаев Гр(¾) бактериемией и в 20-40% случаев Гр(+) микробами (стафилококками и стрептококками). Патологическая анатомия С удручающе тяжелая, для нее характерны: · типичные изменения в селезенке: дряблая и увеличенная в размерах (септическая). При Гр(¾) флоре в ней…Рис. 4. Схема патогенеза сепсиса.
Цитокины являются БАВ, вызывающими системный ответ при поступлении в кровоток (рис. 4). К цитокинам относят: метаболиты арахидоновой кислоты, фактор активации тромбоцитов, противовоспалительные (ФНО, ИЛ-1,6, j-интерферрон) и контролирующие воспалительный ответ (ИЛ-2,10). Нарушение баланса двух последних групп цитокинов приводит к повреждающему и системному воспалительному ответу.
Поступающие в кровоток в нарастающем количестве агрессивные противовоспалительные молекулы "набрасываются на все без разбору", и локализованная воспалительная реакция превращаются в патологическую, системную (ССВО).
Синдром СШ чаще обусловлен Гр(¾) микрофлорой, массивным поступлением и размножением микроба в кровотоке и выбросом медиаторов. В формировании СШ равное участие принимают бактериальная токсемия и ДВС-синдром (генерализованный тромбоз сосудов под действием эндотоксина). Суть СШ заключается в нарушении кровотока в микроциркуляции, то есть в периферическом сосудистом коллапсе вследствие стимуляции бактериальным эндотоксином a-рецепторов в большей части органов. В последующем развивается спазм, дилатация артериол и венул, что приводит к тяжелым системным расстройствам; кровь неспособна выполнить свою функцию. Из-за неадекватности перфузии поражаются многие внутренние паренхиматозные органы. Вследствие снижения венозного притока, сердце недостаточно наполняется в диастолу (поэтому плохо растягивается), что способствует развитию сердечной недостаточности и гипотонии (снижении систолического АД на 40 мм рт. ст. и более от исходного уровня).
Очаг инфекции
¯
Инвазия в кровоток (бактериальная токсемия, ДВС-синдром)
¯
Высвобождение медиаторов
¯ ¯
Периферические Прямое угнетающее действие
сосудистые эффекты на миокард
¯ ¯
Нарушения микроциркуляции
¯
Резкое снижение Сильная дисфункция Тяжелое угнетение
ОПС внутренних органов миокарда
¯ ¯ ¯
Смерть от Смерть Смерть от падения
рефрактерной УОС
гипотензии
Рис. 5. Патогенез септического шока.
Клиника Сскладывается из: ацикличного течения, длительной лихорадки (вызванной инфекцией), очага (очагов) гнойной инфекции, ССВО и бактериальной верификации микроба. Клинические проявления С определяются его формой и возбудителем. Так, вторичный С может развиваться на фоне предшествующей тяжелой патологии (например, цирроз печени, рак, некомпенсированный СД, ХПН и др.). В данном случае микроб размножается в высоком темпе. Но С может развиться и на фоне полного здоровья (первичный С).
Для острейшего (молниеносного) Гр(¾) Схарактерно: бурное начало с тифоподобной лихорадкой (за 1-3 ч беспричинно повышается температура тела более 39оС) с ознобами и нарастающей интоксикацией; клиника яркая и простая (стремительное развитие симптомов); формируются ОРДС и СШ (обычно появляется за сыпью) со снижением систолического АД менее 70 мм рт. ст. уже в первые часы. В 80% случаев СШ и геморрагическая сыпь развиваются в первые сутки (в 15% ¾ во вторые и в 5% случаев ¾ на третьи сутки). Появления крупных подкожных кровоизлияний по типу "носков, перчаток" свидетельствуют о фатальном прогнозе.
Для молниеносного Гр(+) С характерно наличие триады симптомов: "взрывное начало", раннее развитие ОЛЖН (в первый же день вследствие кардиотропности золотистого стафилококка) и страх смерти. Больные не жалуются на головную боль на фоне имеющейся высокой лихорадки, но у них может развиться инфекционный психоз ("шизофренический синдром"), который может проявиться еще до начала лихорадки. В РБ острейший С почти всегда имеет менингококковую или стафилококковую природу.
Клиника острого С (составляющего более 40% от всех форм С) имеет менее яркую, но более сложную симптоматику. Характерными признаками данного С являются: лихорадка более 38оС или гипотермия (менее 36оС), тахипноэ (более 20 в мин), лейкоцитоз более 12×109/л (или лейкопения менее 4×109/л) с наличием незрелых форм более 10% и гипоксемия. В 80% случаев этот С начинается остро и течет как острое инфекционное заболевание. Высота лихорадки (вначале она появляется в вечерние часы) зависит от пирогенности микроба и реактивности макроорганизма.
Важнейшие ранние проявления С (микробной интоксикации):
1. Высокая лихорадка гектического характера с суточными колебаниями более 2оС (встречается только у 1/3 больных), сопровождаемая ознобами и недомоганием. Чаще эта лихорадка бывает постоянной, интермитирующей или волнообразной. Но возможно появление субфебрилитета с периодическими "свечами" разной продолжительности и безлихорадочными периодами в течение 5-10 дней. Иногда, в течение 1-3 недель, лихорадка может быть единственным проявлением С. У 15% пожилых больных с наличием тяжелых сопутствующих заболеваний нет повышения температуры (имеется гипотермия). Отсутствие температуры ¾ плохой прогностический признак. Нередко заполнение температурного листа больного позволяет уяснить динамику симптомов и эффективность проводимого лечения. В целом диагностическое значение температурной кривой не высоко. Например, гектическая лихорадка встречается как при С, так и опухолях или ДБСТ.
2. Неоднократные(несколько раз в сутки) ознобы (на фоне повышения температуры тела до 40оС) с последующей профузной потливостью через 2 ч. Утром у больного может остаться только легкое недомогание. Все последующие дни, когда температура не повышена, больной считает себя здоровым (анорексия может длиться несколько дней).
3. Головная боль, адинамия.
4. Бледность, боли в мышцах и суставах по типу септического бактериального артрита (сильная боль, припухание, ограничение подвижности), что часто мешает постановке диагноза С.
5. ЧД более 20 в мин.
6. Изменение умственного статуса (вначале симптоматика малоубедительна, а потом больной быстро входит в кому).
Симптомы 5 и 6 являются весьма опасными, так как часто возникают рано, еще до начала лихорадки и ознобов.
7. ЖКТ нарушения (в 1/3 случаев): тошнота, рвота, диарея. Все это также запутывает диагноз С, указывая на гастроэнтерит.
В ряде случаев симптоматика стафилококкового С облегчается: специфическими кожными проявлениями в области груди и живота (сухие, влажные некрозы вследствие инвазии микроба, гнойные высыпания после появления лихорадки). Сыпь может быть:
· продуктивной ("цветущие" розеолы, папулы, везикулы как "просяное зерно" с прозрачной жидкостью), что свидетельствует о достаточном иммунитете (о благоприятных реакциях макроорганизма на поступление микроба в кожу);
· деструктивной(геморрагии, пустулы, некрозы), что указывает на неблагоприятное течение процесса. Так, при синегнойном С могут появляться некротизирующие буллезные поражения кожи (быстро становящиеся геморрагическими) в подмышечной и мочеполовой областях.
С на фоне выраженного ДВС-синдрома проявляется акроцианозом и даже некрозом периферических тканей (кончик носа, пальцев или уха).
Клинические критерии острого С:
· несоответствие между местным воспалительным очагом (например, мелкая рана, фурункул) и сильной общей интоксикацией;
· отсутствие эффекта (не уменьшаются температура и интоксикация) от хирургической санации первичного очага;
· увеличение размеров селезенки в динамике.
В целом, для клиники острого С характерна этапность развития. Первый (начальный, септический) период возникает вследствие формирования септического очага и стойкой бактериемии (септицемии) и протекает кратковременно, субклинически. В этот период нет органных поражений, а течение С не тяжелое. Так, несмотря на лихорадку, самочувствие больного может быть удовлетворительным, даже головные боли бывают редко. Болезнь на этой стадии излечивается, если удается подавить микроб в септическом очаге. Обычно в начальный период нет подозрений на С, и врач или больной даже не думает об этой тяжелой патологии. Если применяемые АБ не эффективны, С прогрессирует и переходит во второй, септикопиемический период с формированием отдаленных гематогенных метастазов в виде воспалительно-деструктивных процессов на фоне резкого ухудшения общего состояния (роста интоксикации) и проявлений поражения многих органов (абсцессы, плеврит, геморрагическая сыпь). Во втором периоде "светлые промежутки" с нормальной температурой тела сокращаются, и характер температурной кривой обычно становится гектическим вследствие массивного выхода микроба и его токсинов из метастатических очагов ("бактериальные ливни"). В септикопиемическом периоде происходят следующие изменения во внутренних органах.
В легкихразвивается инфильтративно-деструктивная (в 20% случаев) или диссиминированая (множество мелких рентгенологических теней) двухсторонняя пневмония (в 80% случаев). Причем, у каждого пятого больного при стафилококковом С картина П может доминировать в клинике. Эта пневмония протекает особенно тяжело на фоне поражения других жизненно важных органов (почек, селезенки).
Довольно часто (в 30-40% случаев) при СШ развивается и ОРДСпо типу "шокового легкого" (токсического некардиогенного интерстициального и альвеолярного отека легких) с клиникой быстро нарастающей дыхательной недостаточности: тахипноэ, цианоз кожи и слизистых, гипоксемия (раО2 менее 50 мм рт. ст.). На рентгенографии легких выявляются двухсторонние, множественные и пятноподобные инфильтративные тени ("снежная буря"). По мере прогрессирования ОРДС инфильтраты сливаются. Нередко эту картину путают с метастатической пневмонией, вследствие чего назначают АБ, что еще больше усиливает токсемию (из-за распада микробов). Объективно при ОРДС выявляется скудость физикальных данных (например, может быть только ослабленное везикулярное дыхание или небольшое количество влажных хрипов), тахикардия, тахипноэ, выраженный цианоз и снижение легочного артериального давления заклинивания менее 12 мм рт. ст.
ОРДС часто возникает на фоне наличия его факторов риска: индуцирование патологии Гр(¾) микробами, появление клиники СШ или формирование метастатической пневмонии. Если при С формируется ОРДС на фоне сопутствующей вторичной пневмонии, то летальность превышает 90%.
Нарушения со стороны сердца включают: тахикардию, гипотонию, снижение УОС и ФВЛЖ (особенно при СШ, когда снижается ответ на введение инотропных средств), аритмии. Нередко развивается инфекционно-аллергический миокардит, сухой или гнойный перикардит (при стафилококковом С сердце поражается в 15% случаев).
При поражении почек (вследствие гипоперфузии) в анализах мочи появляются невысокие: протеинурия (у 15% больных), лейкоцитурия (у 10% больных), цилиндрурия и гематурия. В биохимическом анализе крови отмечается рост мочевины и креатинина. При стафилококковом С обычное явление ¾ мелкое метастатическое абсцедирование почек, которое обычно не диагностируется. Позднее осложнение ¾ острый тубулярный некроз.
Печень увеличивается в размерах в половине случаев, становится плотной и болезненной (в другой половине ¾ не прощупывается). Отмечается рост уровней АСТ и АЛТ в крови. Обычно Гр(¾) С дает желтушное окрашивание кожи и слизистых.
В случаях, когда селезенка пальпируется увеличенной, плотной и эластичной, то это ¾ клинический показатель хорошей реакции макроорганизма на генерализацию микроба. Если селезенка на ощупь дряблая, болезненная, это менее благоприятный показатель.
Лимфоаденопатия также часто отмечается у больных с С. Прогностически неблагоприятный фактор ¾ появление у больных на фоне лихорадки болезненных и мягких лимфоузлов. Это свидетельствует о том, что лимфоидные структуры (как часть системы иммунитета) некомпетентны и служат местом накопления микробов.
В мозге вследствие метастатических гнойных отсевов идет поражение мозговых оболочек (например, гнойный менингит), которое приводит к появлению нарушений сознания и сильных головных болей. Поражения мозга могут симулировать фебрильную шизофрению, вследствие чего больного с острым С направляют сразу в психиатрическую клинику, а уже потом ¾ в терапевтическое отделение (но время уже "ушло").
Ведущие синдромы острого С:
· легочной (в 50% случаев);
· токсическая нефропатия (в 60%);
· ДВС-синдром (практически у всех больных);
· множественной органной недостаточности (включает выраженную дисфункцию трех и более жизненно важных органов);
· гепатолиенальный (в 60%), причем при молниеносном С гепатомегалия и спленоменгалия не успевают сформироваться в достаточной степени;
· реактивности, включает комплекс симптомов, направленных на подавление инфекции (лихорадка, гепато- и спленомегалия, увеличение лимфоузлов, метастатическая сыпь);
· СШ (в 15%).
СШ имеет 2 фазы:
· компенсированную в первые сутки (стойкая гипотония; выраженная тахикардия более 120 в мин; снижение ОПС; появление аритмий; сознание сохранено, но есть тревога и беспокойство; диурез нормальный; на коже рук и ног появляется глубокая, красная сыпь; у женщин СШ часто развивается сразу после месячных);
· декомпенсированную(рефрактерный СШ, не поддающийся инфузионной терапии в течение часа, введение больших доз ГКС не эффективно), когда развиваются резкие тахикардия (более 140 в мин) и снижение АД до 60 мм рт.ст. и ниже; температура тела снижается до нормы; появляется олигоурия (вплоть до анурии); формируется полиорганная дисфункция ("шоковое легкое" ¾ ОРДС, "шоковая почка" ¾ ОПН) и тяжелый ДВС-синдром. Больные в эту фазу заторможены, безразличны; часто отмечаются кровоизлияния на слизистой ЖКТ и кожи. Позднее появляются одышка (частое собачье дыхание) и анурия, наступают потеря сознания, АД и смерть. Летальность при СШ связана с: рефрактерной гипотонией и постоянно низким ОПС; прогрессирующим лактатным ацидозом; полиорганной недостаточностью, несмотря на соответствующее лечение.
В отличие от молодых, С у пожилых может протекать без лихорадки, или могут быть отдельные пики повышения температуры до 38оС, совпадающие с познабливанием и миалгией. У этой категории больных С может не давать локальных симптомов (например, пневмония сопровождается лихорадкой, но нет кашля или других респираторных симптомов). Частый дебют С у пожилых ¾ это неожиданное и разительное утяжеление больного, которое не сопоставимо с небольшой лихорадкой на фоне отсутствия жалоб. Буквально за сутки состояние больного резко ухудшается (с ним что-то случилось): он тихо лежит в постели; нет аппетита, не может сам встать и ходить; плохо говорит. Применение в этом случае АБ в средне терапевтических дозах не препятствует прогрессированию С. Наличие у данных больных затянувшейся лихорадки заставляет врачей обычно искать опухоль, хотя на самом деле у больного имеется септикопиемия со свойственной ей патологией органов (чаще поражаются легкие по типу септической пневмонии с реактивным плевритом).
Изменения периферической крови при С. В большинстве случаев (без наличия иммунодефицита) отмечается лейкоцитоз (14-18×109/л у 70% больных), выраженность которого варьирует в зависимости от тяжести С и сдвиг формулы влево, может быть и токсическая зернистость нейтрофилов. Лейкопения (плохой прогностический признак) встречается очень редко, только при тяжелом С вследствие угнетения кроветворения. Рост СОЭ и анемия выявляются у 80% больных.
В ранний период С определяются КЩС нарушения ¾ респираторный алкалоз, а при появлении СШ ¾ метаболический ацидоз.
Подострый С(длительность 5-8 недель) не имеет принципиальных различий от острого С и представляет его затянувшийся вариант. Одна из частых причин этого ¾ недостаточная АБ терапия в период септицемии ("синдром подлечивания").
Дляхронического Схарактерно наличие длительно существующего септического очага, из-за чего болезнь приобретает хронический характер, формируются хронические воспалительно-деструктивные изменения в местах размножения микробов. Отмечается вялое и длительное размножение микробов в септическом очаге. Обычно после удаления очага первичной хронической инфекции (например, тонзиллэктомии) продолжается состояние неполного здоровья: отмечаются повышения температуры до 37,5оС, периодические снижения трудоспособности и возникновение одной и той же бактериемии. В целом хрониосепсис ¾ это хроническая, вялотекущая, генерализованная инфекция (постоянная или периодическая), при которой отсутствуют видимые очаги в органах и тканях, либо после ликвидации этих очагов не наступает полного выздоровления. Типичным примером хрониосепсиса является хронический ИЭ с длительным наличием септического очага на эндокарде клапанов, на фоне общего относительно удовлетворительного самочувствия больного вследствие достаточного уровня антител к токсинам возбудителя. Главную опасность при ИЭ представляет не тяжелая интоксикация (как при остром С), а местный патологический процесс на клапанах сердца с последующим развитием СН или отрыва вегетаций с эмболиями.
Причины гибели больных от С: прежде всего развернутый ДВС-синдром (обязательное проявление С), который распознается только у 10% больных; функциональная недостаточность жизненно важных органов (сердце, мозг, почки, легкие) или гепаторенальный синдром.
Диагностика С.Если найден первичный очаг у лихорадящего больного (с затемненным сознанием, тахипноэ и нормальной рентгенографией грудной клетки), то диагноз С очевиден. Обнаружение первичного септического очага может быть элементарно простым (как при синус-тромбозе), а может потребовать длительного и тщательного обследования. Возможны случаи, когда первичный септический очаг не удается обнаружить как при жизни, так и при смерти больного. Обычно диагностика С, особенно у постели больного, весьма трудна. Как правило, в течение первой недели госпитализируется только 1/2 больных С, причем у них нередко С диагностируется только в терминальной стадии.
Чтобы доказать наличие С у больного необходимы два условия:
· "плотная" бактериемия (более, чем в 50% случаев), положительные посевы крови;
· длительность бактериемии более 5 дней.
Распознавание С должно быть клиническим, упор делается на: клинические симптомы инфекции + тахикардию более 90 в мин + нарушение функции многих органов. Так, для молниеносного стафилококкового С имеется довольно характерная симптоматика. Если ждать результатов посева крови, то можно "потерять" больного.
В целом, учет: наличия предрасполагающих факторов к С, "входных ворот", бактериемии, клинических симптомов и положительного эффекта от тест-терапии позволяет правильно распознать С в 1/2 случаев.
Обнаружение возбудителя С необходимо больше для адекватной АБ терапии, а не для диагностики С. При молниеносном С необходимо осуществить: бактериальный посев из зева, микроскопию толстой капли крови, посев крови на стерильность и гемокультуру. При остром С посевы крови должны браться в течение первых 3-5 дней не менее 2 раз (лучше чаще, через 2 ч) в сутки с последующим рассеиванием материала в среды для Гр(¾), Гр(+) и анаэробов. Если уже начато лечение АБ, то шансы на высев микроба из крови незначительны. Лучше брать кровь в самом начале септицемии ¾ лихорадки и появления озноба (микроб пребывает в крови не постоянно). Позднее, в фазу септикопиемии, микроб уже фиксируется в тканях, и больной становится мало курабельным. Бактериемия может быть и у здорового человека (после удаления зуба, родов, тонзилэктомии), но она кратковременна и бессимптомная.
Посев крови должен проводиться в стерильных условиях: кожу в точке венепункции обрабатывают 2% раствором йода, а потом 70% спиртом. Используют стерильные перчатки, иглу и шприц для крови. Пробу крови необходимо сразу доставить в лабораторию. Правда, даже при строгом соблюдении этих правил процент положительных проб не превышает 60%. Отрицательная гемокультура не исключает диагноз С и не имеет самостоятельного значения. Все необходимо соотносить с клиникой, так как С понятие клиническое, а не лабораторное.
К числу дополнительных информативных тестов диагностики С относят:
· п/к введение стафилококкового анатоксина в дозе, равной 0,1 мл. По диаметру гиперемии определяют гиперчувствительность замедленного типа с стафилококковому антигену. Реакция расценивается как положительная, если диаметр гиперемии превышает 1 см;
· УЗИ брюшной полости и сердца с целью обнаружения абсцессов внутренних органов, вегетаций на клапанах сердца;
· рентгенография грудной клетки (может быть выявлена исходная пневмония, как источник С или проявления ОРДС);
· коагулограмма в динамике для верификации острого ДВС-синдрома: положительные паракоагуляционные пробы (фибриноген В, РКМФ, нафтоловая проба), снижение фибриногена и числа тромбоцитов. Вначале отмечается гиперкогуляция, а позднее ¾ гипокоагуляция и интенсификация фибринолиза.
Выделяют следующие условные критерии С:
· лихорадка;
· недостаточность функции многих органов (ОРДС, токсическая энцефалопатия, гепаторенальный синдром и др.);
· проявления ДВС-синдрома или его нарастание;
· тяжелая интоксикация;
· гипотония, тахипноэ, тахикардия;
· лейкоцитоз со сдвигом влево;
· появление септикопиемических очагов на коже больного.
Обычно наличия трех этих симптомов достаточно для постановки С и начала быстрого лечения. Диагностика С облегчается при наличии первичного очага инфекции и осложняется при его отсутствии. В целом, любая лихорадка более 5 дней (особенно гектическая), без местных проявлений и головной боли и при относительно благоприятном состоянии больного должна быть подозрительной на криптогенный С.
Дифференциальный диагноз Спроводят с любыми лихорадочными заболеваниями, но чаще с: милиарным туберкулезом легких, ДБСТ (особенно СКВ), опухолями (особенно раком печени и гипернефромой, вызывающих лихорадку вследствие поступления в кровь раковых пирогенов), лимфогранулематозом, лейкозами. Часто встречаемые ошибки в дифференциальной диагностике С и туберкулеза обусловлены следующими причинами: большим вниманием к рентгенограмме легких, чем к самому больному; необоснованной верой в неактивность старых, фиброзных кальцинатов в легких и в то, что СОЭ более 70 мм/ч не бывает при туберкулезе или в то, что малые местные изменения на рентгенографии легких не могут вызвать высокой лихорадки. После исключения С и туберкулеза легких, как причин лихорадки, в первую очередь, следует думать о СКВ (положительный эффект от ГКС, болеют чаще молодые женщины, нет гнойных очагов, часто выявляются LЕ-клетки в крови и поражения кожи в виде эритемы).
Лечение С. Сложность патологических механизмов формирования С требует комплексного лечения. Не следует ожидать заметного эффекта только от одного средства или метода, особенно при тяжелом С. Терапия С включает:
· подавление и ликвидацию микроба как первопричины болезни (этиотропные АБ);
· коррекцию заболеваний, предшествующих С (при необходимости хирургическое вмешательство в области очага инфекции);
· восполнение ОЦК;
· поддержание дыхания и гемодинамики при СШ;
· коррекцию ДВС-синдрома и нарушений гомеостаза (ацидоза, электролитного и водного баланса).
Консервативное лечение С:
1. АБ, которые при подозрении на острый С даются максимально рано. До введения АБ берут кровь на гемокультуру. Если микроб известен, то лечение С становится более специфичным. АБ практически бесполезны при хрониосепсисе (если нет положительного эффекта от АБ к 6 дню лечения, то и далее его трудно ожидать). При позитивном эффекте от АБ ранее 10 дня нормальной температуры их отменять нельзя.
2. Антикоагулянты (регуляция гипокоагуляции).
3. Антиферменты(блокирование агрессивных ферментов).
4. Экстракорпоральные методы детоксикации макроорганизма (гемосорбция, плазмоферез, УФО, лазерное облучение крови, фильтрация крови больного через селезенку свиньи).
АБ являются основой раннего и успешного лечения С. Идеально, чтобы в ранний период С был выявлен микроб, и назначен соответствующий малотоксичный АБ. Если возбудитель не обнаружен, то АБ терапия осуществляется "вслепую" (в условиях РБ более, чем в 90% случаев). Решение о начале АБ терапии эмпирическое и базируется на комплексе факторов: исходный фон (здоровый человек или имелись сопутствующие заболевания), состояние иммунитета. До установления возбудителя С лечение начинают на основании известной АБ чувствительности предполагаемого возбудителя С. Так, стафилококковый С можно верифицировать и по клинике (возникает от фурункула или гнойной раны, нет головной боли и эндотоксемии, влажный язык, имеется некоторая эйфория). Врачу важно уже по клинике предварительно решить, что возбудителем заболевания служит Гр(¾) или Гр(+) микроб, а затем подобрать начальный АБ.
Условия эффективности терапии АБ: максимально раннее их назначение (еще до формирования опасных для жизни инфекционно-токсических поражений); в/в путь введения бактерицидных АБ и в максимальных суточных дозах (в/м и оральный пути введения нецелесообразны) для создания высоких концентраций в крови и в очаге воспаления; хорошая переносимость. Единственный повод для смены АБ ¾ его неэффективность в течение 3 дней или даже ухудшение состояния больного на фоне лечения этим АБ. При начальной терапии комбинируют АБ (обычно не более двух) у больных со снижением иммунитета на фоне нейтропении, когда необходимо "закрыть" все возможные микробы до получения результатов посева крови или при наличии множественных резистентных штаммов или синегнойной палочки. Комбинация трех и более АБ заметно не повышает их терапевтический эффект, но резко усиливает токсические проявления такой "тройной" терапии. Такие новые АБ, как имипинем (меропинем), имеют широкий спектр действия и не нуждаются в комбинациях с другими АБ, так как дают адекватный терапевтический эффект в виде монотерапии.
Таблица 10
Эмпирическая терапия сепсиса при установленном первичном очаге
Таблица 11Эмпирическая АБ терапия при наличии С с неустановленным первичным очагом инфекции
Как видно из таблицы 11, стартовую терапию С при неизвестном этиологическом микробе начинают с цефалоспоринов 3-го поколения (цефтриаксон,… Программа ступенчатой эмпирической терапии АБ при С неустановленной этиологии.… После 3-5 дней стабилизации состояния больного возможен переход на оральные АБ. В этом случае предпочтительнее…Целенаправленная АБ терапия С при установленном возбудителе
Важный компонент лечения С - пассивная иммунотерапия: введение антистафилококковой плазмы (из человеческой крови) в/в по 200 мл через день (5-10… Для коррекции гемостаза сразу вводится в/в гепарин по 30000 ед в сутки (лучше… При С развивается ферментный "взрыв" (вследствие утечки клеточных ферментов и выхода бактериальных протеаз),…ЛИХОРАДКА НЕЯСНОГО ГЕНЕЗА
Л весьма часто встречается в практике врача-терапевта. Большие диагностические трудности возникают в случаях, когда Л носит длительный характер и… Установление причины длительной Л часто выходит за пределы узких… Критерии синдрома ЛНГ (Petesdorf, 1967):Механизмы развития Л.
В 7% случаев Л определяются: нарушениями терморегуляции, включающими гипоталамический синдром, конституционально обусловленную гипоталамопатию с… Таким образом, в большинстве случаев ЛНГ связана с пирогенным механизмом… Эндогенный пироген содержится в цитоплазме образующих его клеток. Это белок, как правило, лейкоцитарного происхождения…Дифференциальная диагностика ЛНГ.
· наличие и характер озноба (больной ощущает внутренний холод, дрожь в период озноба и "лязганье зубов"). Так, однократные ознобы… · выраженная потливость без ознобов отмечается при ТВС и… · переносимость Л. Она хорошо переносится при ТВС, лимфогранулематозе и лекарственных поражениях. Если высокая Л…Алгоритм диагностики диагностики
Зоонозы
инфекция (кроме ТВС) болезней, вызывающих ЛНГ ¯ Да Нет II Недооценка внелегочных формТВС
нет

 Неспецифическая III Ошибочная трактовка
Неспецифическая III Ошибочная трактовка
 инфекция клинических симптомов, неуме-
инфекция клинических симптомов, неуме-
 ние выявить главный симптом
ние выявить главный симптом
Да Нет
(гнойная инфекция
в брюшной полости, ИЭ)
Рак IV

Да Нет
(лимогранулемато, гипер-
 нефрома, гепатома) V Недооценка последовательности
нефрома, гепатома) V Недооценка последовательности
разных симптомов, их комбинаций,
недостаточно полное обследование
Иммунокомплексные
Болезни
Нет Смешанные VI болезниРисунок 6. Алгоритм диагностики ЛНГ.
Третий этап сводится к исключению неспецифической гнойной инфекции, сначала общей, а потом и очаговой. При урологической, тонзилогенной и одонтогенной инфекциях ее очаг обычно известен. При хирургическом сепсисе у лиц пожилого и старческого возраста гнойный очаг (абсцесс) следует искать в органах брюшной полости. Так, нагноительные болезни брюшной полости составляют 33% всех случаев инфекционно-воспалительных заболеваний у лиц с ЛНГ. У молодых женщин причину ЛНГ нередко необходимо искать в гениталиях (например, криминальный аборт), а у мужчин ¾ в мочеполовой сфере.
Абсцессы являются наиболее частым локальным проявлением инфекционных болезней, протекающих в форме ЛНГ. Основные факторы риска развития нагноительных заболеваний брюшной полости ¾ операции, травмы живота, наличие заболеваний кишечника и желчевыводящих путей, тяжелые фоновые заболевания (ХНК, СД, ЦП и хроническая алкогольная интоксикация). Обычно эти абсцессы возникают в брюшной полости или полости таза (например, внутри- и межкишечные, в поддиафрагмальном пространстве, в печени и селезенке).
Чаще речь идет о небольших абсцессах с атипичным течением и проявлениями. Долгое время они не дают локальных симптомов, боли или увеличения пораженного органа. Так, длительность Л при абсцессах брюшной полости может достигать трех лет. Обнаружению абсцессов в брюшной полости помогают УЗИ, КТ, лапороскопия и диагностическая лапоротомия. Основные критерии гнойного заболевания: начало с лихорадки гектического типа (повышение температуры на 2-4оС и снижение до нормы) с изнуряющими потами, повышение СОЭ, лейкоцитоз со сдвигом влево (но может быть и лейкопения), мягкая и увеличенная селезенка.
Довольно трудно диагностировать поддиафрагмальный абсцесс печени. Его критерии: боли в подреберье, связанные с дыханием или глубокой пальпацией; ослабление дыхания и притупление легочного звука в нижних отделах легких (может быть реактивный плеврит); на рентгенограммах грудной клетки выявляется высокое стояние диафрагмы, выпот в плевральную полость на стороне поражения (чаще справа), а также наличие воздуха под диафрагмой.
В терапевтической клинике у больных без явной органной патологии с ЛНГ на долю малосимптомно текущего холецистита и холангита(при этом Л может быть единственным симптомом, а боль и желтуха отсутствуют) приходится до 60% случаев. Распознаванию этой патологии помогают выявление желчно-пузырных симптомов Ортнера, Мюсси. Так, локальная болезненность как правило указывает на холецистит, а диффузная чувствительность печени ¾ на ангиохолит, холангит. Нередко повышаются ГГТ, ЩФ, АЛТ, а также выявляются определенные изменения на УЗИ. Вирусные гепатиты В, С на определенных этапах также могут проявляться только ЛНГ.
Около 10% больных с ЛНГ имеют очаговую инфекцию с локализацией в кишечнике (НЯК, БКр, лимфома толстой кишки). Часто у этих больных имеются только ЛНГ и некоторая болезненность толстой кишки, а других симптомов нет. Для верификации вышеуказанных диагнозов необходима колоноскопия с множественной биопсией кишки.
Инфекции мочевыделительной системы занимают второе место по частоте ЛНГ. При наличии почечной гнойной инфекции повышение температуры тела у больного возникает при внутри- или внепеченочной обструкции: острый или хронический пиелонефрит, паранефрит, апостематозный нефрит; простатит и абсцесс простаты (у мужчин). Характерные изменения в моче могут отсутствовать (или быть слабо выраженными). Диагностике помогают: УЗИ, рентгенография почек, экскреторная урография и КТ почек.
Если первичный очаг гнойной инфекции не найден, а в клинике преобладают: лихорадка, интоксикация, эмболии, мягкая и увеличенная селезенка, то можно думать о терапевтическом сепсисе. В первую очередь, необходимо исключить ИЭ (подробнее см. лекцию №2). Первичный ИЭ (источники его не находят) по клиническим проявлениям является болезнью-"хамелеоном". Часто Л при ИЭ заметно опережает характерные для него физикальные симптомы, гепаторенальный синдром, анемию и нефрит. Диагностика ИЭ весьма трудна, особенно у пожилых лиц и на ранних этапах, когда преобладают общие симптомы сепсиса (высокая, неправильная Л), до тех пор, пока не появляются симптомы поражения клапанов сердца (шумы). Для верификации ИЭ большое значение имеет бактериологическое обследование крови и мочи. Если результаты отрицательные, то проводят посев артериальной крови (из лучевой артерии). Могут быть ложно отрицательные результаты посева крови вследствие необходимости наличия сложных сред для длительного культивирования, а также частого, бесконтрольного использования АБ. Дополнительно проводят: рентгенографию грудной клетки, придаточных пазух носа и зубов; в/в урографию, УЗИ брюшной полости, ЭхоКГ , по показаниям ¾ лапароскопию.
Достоверный диагноз ИЭ обычно ставят при быстром формировании порока сердца (чаще появляются аортальные шумы) и симптомах вегетаций на клапанах сердца на ЭхоКГ. У пожилых больных могут возникнуть трудности в дифференциальном диагнозе с поражением клапанов атеросклеротического генеза. ИЭ, как причина ЛНГ, весьма характерен при: малообъяснимых тромбоэмболиях и рецидивирующих ТЭЛА, быстром появлении симптомов ХНК и падении уровня гемоглобина (Нв).
Четвертый этап ¾ исключение неинфекционных заболеваний. Опухоли различной локализации занимают второе место в структуре причин ЛНГ. Любая опухоль может дать ЛНГ! Весьма трудны для диагностики лихорадочные "маски" рака, если нет сопутствующих локальных симптомов. Основные трудности своевременной диагностики опухолей у больных с ЛНГ связаны с минимальными местными проявлениями или их отсутствием. Наиболее часто диагностируются лимфопролиферативные опухоли (лимфогранулематоз, лимфосаркома), рак почки и печени.
При ряде опухолей (лимфогранулематоз, гипернефрома) может быть Л на фоне нормальной СОЭ. У этих больных высокая Л (чаще утром) связана с паранеопластическими реакциями (продукцией опухолью различных пирогенов типа ИЛ-1), реже с распадом опухоли или присоединением вторичной инфекции. Обычно степень Л не зависит от размеров опухоли. Л может быть как при больших опухолях, так и при наличии малого опухолевого узла. Если имеется ЛНГ у больного опухолью, то на фоне присоединившейся интеркурентной инфекции, несмотря на снижение Л после курса АБ, сохраняются симптомы интоксикации (слабость, плохой аппетит, снижение работоспособности и веса).
Лихорадочные "маски" опухолей чаще отмечаются при раке почек и опухолях желудка, печени, кишечника (они дают суммарно до 40% всех ЛНГ опухолевого генеза) и лимфопролиферативных заболеваниях (лимфогранулематоз). Реже эти "маски" встречаются при раке бронхов, толстой кишки и поджелудочной железы.
Онкологический поиск в этих случаях включает неинвазивные методы: рентгенографию грудной клетки, ЖКТ и почек; УЗИ брюшной полости; эндоскопические обследования ЖКТ; позднее ¾ лапароскопию с биопсией печени или лимфоузлов; стернальную пункцию и КТ и ЯМР. В каждом конкретном случае программу обследования реализуют индивидуально. Так, в ряде случаев на мысль об имеющейся опухоли при ЛНГ могут наводить неспецифические синдромы (узловатая эритема, гипертрофическая остеоартропатия, мигрирующий тромбофлебит).
Опухоли однородной плотности, вызывающие ЛНГ, часто дают метастазы в брюшную полость, особенно у лиц пожилого возраста. Локализация первичного опухолевого очага может быть разной (почки, печень, поджелудочная железа, желудок и почки). Иногда этот очаг не находят даже на вскрытии.
Из гемабластозов на первое место в качестве причины ЛНГ следует поставить лимфогранулематоз, в меньшей степени неходжскинские лимфомы с локализацией в малоувеличенной селезенке и забрюшинных лимфоузлах. Критерии лимфогранулематоза ¾ волнообразная лихорадка Эпштейна (на практике у большей части больных ее нет, зато имеется неспецифическая, гектическая Л), удовлетворительное общее состояние вне периода Л, профузная потливость, кожный зуд, генерализованная лимфоаденопатия и гепатоспленомегалия, лейкоцитоз с эозинофилией, наклонность к тромбоцитозу и моноцитозу крови. При подозрении на лимфогранулематоз в план обследования входят: рентгенография грудной клетки и томография средостения, биопсия периферических лимфоузлов с определением клеток Березовского-Штенберга, КТ (для верификация внутрибрюшных лимфоузлов), лимфография (для выявления парааортральных и забрюшинных лимфоузлов).
Лейкозы также нередко вызывают ЛНГ. Часто проявления острого лейкоза путают с началом остро протекающего инфекционного заболевания. Так, острые лейкозы почти всегда сопровождаются высокой Л до 40оС. Обычно сразу поставить диагноз лейкоза бывает трудно, так как не определяются бластные клетки в крови и в костном мозге. У больных могут быть: анемия и лейкопения (прелейкоз). Вызывать ЛНГ, обусловленную присоединением инфекции, может также хронический лимфолейкоз.
Пятый этап диагностики ЛНГ заключается в исключении иммунно-комплексных заболеваний (ДБСТ), при которых многосимптомность поражения появляется, как правило, на поздних стадиях заболевания. Эти системные заболевания занимают третье место по частоте среди причин ЛНГ. Иногда могут быть смешанные болезни соединительной ткани, дающие перекрестные синдромы с клиническими симптомами: СКВ, полимиозита, системной склеродермии (волчаночный вариант).
ДБСТ (СКВ, РА, дерматомиозит и УПА) редко проявляют себя только изолированной ЛНГ. Нередко имеются сопутствующие классические скелетно-мышечные симптомы (артралгии, эритема, пурпура). Иногда Л опережает появление суставного синдрома или других системных нарушений. Важна детальная оценка всех имеющихся симптомов у больного (миалгии, мышечной слабости, головной боли). Это, на фоне повышенной СОЭ, может указать на дерматомиозит или височный артериит.
Из системных поражений соединительной ткани на первое место в качестве причины ЛНГ следует поставить УПА. При нем многосимптомность появляется значительно раньше, чем при других ДБСТ. Для УПА характерны: волнообразная Л, снижающаяся под действием НПВС и ГКС; похудание; полиорганная патология (коронариты, поражение бронхиальных сосудов с клиникой БА, абдоминальный синдром, поражение почек с быстрым развитием АГ и ХПН), полиневриты, подкожные узелки и эозинофилия.
Реже причиной ЛНГ могут быть болезнь Хортона (поражение височных артерий) или Такаясу (поражение крупных ветвей аорты) или Бюргера. Не часто в качестве первого симптома при РА могут быть ЛНГ, лимфоаденопатия и анемия.
Иногда причиной ЛНГ может быть прием лекарств (персистирующая лекарственная Л, вызывающая 3-5% всех ЛНГ). Эта Л может появляться через разные промежутки времени (дни или недели). Обычно лекарственная Л появляется на 7-9 день лечения АБ (пенициллинами, цефалоспоринами, тетрациклинами), сульфаниламидами, цитостатиками, хинидином, новокаинамидом или гидралазином. Доказать лекарственную Л бывает не всегда просто. Диагностике лекарственной Л помогают: отсутствие инфекционного соматического заболевания, незначительная эозинофилия крови, кореподобная сыпь и снижение АД. Лекарственная Л обычно хорошо переносится, но нет корреляции между высотой Л и ЧСС. Не всегда сразу после отмены препарата температура тела становится нормальной вследствие разной скорости элиминации и метаболизма лекарства. Обычно нормализация температуры тела возникает через 3-4 дня после отмены приема подозреваемого лекарства. Часто это является единственным реальным симптомом данной Л. Если ЛНГ сохраняется через 7 дней после отмены лекарства, то лекарственная природа ЛНГ маловероятна.
На шестом этапе исключают смешанные болезни (саркоидоз, повторяющиеся ТЭЛА мелких ветвей, БКр, НЯК и подострый тиреоидит). Их особенностью является атипичное течение: главный симптом ¾ Л плюс отсутствие четкой органной симптоматики. Нередким источником ЛНГ может быть саркоидоз, при котором Л (в целом она мало характерна) появляется на фоне артралгий, поражений лимфоузлов, узловатой эритемы; имеются очаги в печени. Окончательный диагноз ставят на основании биопсии кожи, лимфоузлов, мышц или печени.
Иногда больные с алкогольным гепатитом могут иметь только одну жалобу ¾ Л. Обычно у них после тяжелого запоя возникают: слабость, анорексия, тошнота, рвота, боли в правом боку, смешанная желтуха (гепатоцелюлярная и холестатическая).
Большие диагностические трудности возникают, если Л обусловлена нарушением терморегуляции. Этот вид ЛНГ обычно длительный. Л возникает чаще утром, не сопровождается изменениями крови, хорошо переносится, нет резкого потоотделения и эффекта от антипиретиков (панадола). Бывает конституционно обусловленная гипоталамопатия с расстройством терморегуляции ("привычная" Л) ¾ чаще у молодых женщин на фоне симптомов НЦД и постоянного субфебрилитета, возникающего под влиянием эмоций и ФН.
Ложную (искусственную) Л следует предположить, при исключении других причин Л, у ряда "установочных" больных. Они болезненно сосредоточены на состоянии собственного здоровья, тщательно замеряют ЧСС и температуру тела, стремятся к многократным обследованиям, часто и повторно госпитализируются, добиваются группы инвалидности. Обычно это женщины молодого и среднего возраста, "близкие" к медицине (медсестры). У этих больных нет озноба, тахикардии и потоотделения. Ложная Л обычно вызывается манипуляциями с термометром, приемом внутрь или введением под кожу, в мочевые пути разных веществ, обладающих пирогенными свойствами. Критериями этой Л являются: отсутствие связи между ЧСС и повышением температуры тела, иногда отмечается разница оральной, кожной и ректальной температур. При подозрении на ложную Л проводят одномоментное измерение температуры тела в подмышечной области и прямой кишке (здесь она на 0,5оС выше) в присутствии персонала.
Все же несмотря на тщательное, целенаправленное и повторное обследование больных с ЛНГ, около 15% из них так и остаются с нерасшифрованным синдромом ЛНГ. В ряде случаев Л спонтанно исчезает в дальнейшем и не рецидивирует. Такая ЛНГ чаще обусловлена различными инфекционно-воспалительными заболеваниями.
Этапы диагностического поиска при ЛНГ
На этом этапе обследования можно выделить следующие ситуации: Таблица 13ЛНГ (+) суставно-мышечный синдром
Таблица 14 ЛНГ (+) поражение сердечно-сосудистой системы Ревматизм …ЛНГ (+) кожные поражения
Таблица 19ЛНГ (+) увеличение селезенки
Таблица 20 ЛНГ (+) увеличение печени Хронический активный гепатит … Таблица 21Диагностический поиск у больных с изолированной ЛНГ
Выделяют две ситуации: 1. ЛНГ на фоне острофазовых воспалительных тестов (повышение СОЭ, фибриногена,… 2. ЛНГ без сопутствующих воспалительных острофазовых сдвигов.АРИТМИИ СЕРДЦА
Аритмии сердца ¾ это изменение нормальной ЧСС, регулярности и источника воздействия сердца, а также нарушение связи или последовательности… В целом, аритмии возникают в результате нарушения: автоматизма (синусовая… Последствия аритмий могут быть следующие: отрицательное влияние на психику больного (нарушения сна, ограничение…Рис. 6. Схема трансмембранного потенциала сердечной клетки.
Как видно из рис.6, имеются следующие фазы трансмембранного потенциала (j) :
0. Деполяризации (активации) ¾ кривая идет круто вверх за счет поступления ионов натрия и вторичного медленного тока ионов кальция (Са+2) внутрь клетки.
1. Начальной реполяризации (кривая идет круто вниз).
2. Плато (медленная реполяризация) ¾ уравновешивание входящего в клетку медленного потока ионов Са+2, натрия и выхода калия (К+).
3. Конечная быстрая реполяризация ¾ продолжается инактивация вхождения Са+2, натрия и выход К+.
Фазы 1-2-3 связаны прежде всего с выходом К+ во внешнюю среду.
4. Диастола ¾ сбалансированное поступление в клетку ионов в обоих направлениях.
На ЭКГ фазам 0-1-2-3 соответствует QRS (систола желудочков), а фазе 4 ¾ отрезок TQ (диастола). Выделяют следующие периоды рефрактерности сердца:
· АРП ¾ абсолютно рефрактерный период (в это время никакие импульсы не могут вызвать j действия).
· ЭРП ¾ эффективный рефрактерный период (может быть ответ на импульс).
· ОРП ¾ относительно рефрактерный период (j действия может вызвать более сильный, чем в норме, импульс).
В норме клетки миокарда имеют отрицательный заряд за счет большой разницы уровня К+ внутри и вне клетки (трансмембранный градиент К+). В фазу деполяризации идет положительный поток ионов Na+ и Ca+2 внутрь клетки (через мембрану), вызывая j действие, после его снижения до -30 мв, идет резкое изменение j до 0 (в это время ионы Na+ быстро поступают в клетку). Затем в клетке на короткое время возникает положительное j действие (до +30 мв). Позже формируется фаза реполяризации (возвращение в состояние покоя): идет быстрый и медленный выход ионов калия (К+) из клетки. В 4-ю фазу клетка готова к новому возбуждению.
Классификация аритмий (Кушаковский).
I. Нарушение образования ритма.
А. Нарушение автоматизма СУ: синусовая тахикардия (СТ), синусовая брадикардия (СБ) и синдром слабости синусового узла (СССУ).
Б. Эктопические ритмы (формируется патологический автоматизм), ряд клеток миокарда (в результате дистрофических процессов в их мембранах) начинают самовозбуждаться.
В. Эктопические ритмы, не связанные с нарушением автоматизма.
II. Нарушение проводимости (в основе блокада потока в одном или 2-х направлениях без возврата): СА блокада, AВ блокады I-II-III ст., внутрижелудочковые блокады, асистолия желудочков, синдром преждевременного возбуждения желудочков (WPW).
III. Комплексные нарушения ритма (парасистолия).
Клинические варианты: ЧСС менее 60 в мин, ЧСС более 90 в мин и явно неправильный ритм.
Электрофизиологическая основа многих аритмий (наджелудочковой тахикардии, особенно при WPW, желудочковой тахикардии ¾ ЖТ) ¾ феномен повторного входа потока, обратной связи ("re-entery"). Способствующие факторы этого феномена: повышение уровня эндогенных или экзогенных катехоламинов, электролитные нарушения, гипоксия или ишемия, механические факторы (например, высокая физическая нагрузка).
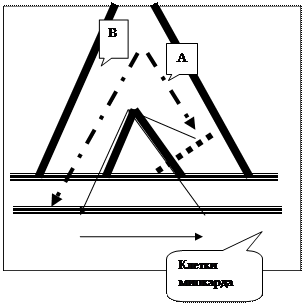 |
Рис. 7. Классическая схема re-entery в периферических волокнах Пуркинье.
Условия re-entery могут создаваться в точке соединения волокон Пуркинье с клетками миокарда (особенно в зоне ишемии) или в зоне повреждения его, или из-за интоксикации сердечными гликозидами (СГ). В основе этого феномена лежит неоднородность проведения потока, создавая благоприятные условия для повторного входа возбуждения в один и тот же участок (участки) миокарда с развитием циркуляции возбуждения (круговой волны). В основе этой "замкнутой петли" лежат 2 механизма: два пути проведения и однонаправленная блокада потока. Как видно на рис. 7, поток попадает в веточку А, где имеется участок односторонней блокады, поток идет в веточку Б. К этому времени исчезает рефрактерность веточки А, и поток идет туда ретроградно, возбуждая ее. К этому времени исчезает рефрактерность веточки Б, и поток идет туда повторно. Так формируется циркуляция потока. Если процесс ограничивается одним re-entery, возникает одна экстрасистола (ЭС), а если циркуляция волны возбуждения идет длительное время, возникает приступ тахикардии.
В целом причины тахи-брадиаритмий можно разделить на 3 класса:
1) болезни миокарда и его аномалии
2) сдвиги нейрогенной и эндогенной регуляции, изменение течения электрических процессов в специальных клетках миокарда
3) сочетание комплекса органических заболеваний сердца и регуляторных нарушений.
Классификация антиаритмических лекарств (Воган-Уильямс). В основе ее лежит способность изменять: ионные потоки в изолированных клетках миокарда, длительность j действия и автоматизм клеток сердца.
I класс (большая часть антиаритмиков относится к этому классу): блокаторы быстрых Nа+ каналов внутрь клетки, за счет этого замедляется скорость деполяризации (то есть, скорость проведения импульса в миокарде и системе Пуркинье):
1А. Мембраностабилизирующие: хинидин, новокаинамид, ритмилен = дизопирамид. Они замедляют максимальную скорость деполяризации, удлиняют j действия (QT). Из этой группы в экстренных случаях широко используется новокаинамид. Тогда как хинидин чаще применяют для стационарного лечения. Основные показания для препаратов этой группы: желудочковые аритмии, тахикардия с узким QRS, мерцательная аритмия (МА).
1В. Местные анестетики: лидокаин, мекситил. Они укорачивают QT (ускоряют реполяризацию) и слабо влияют на деполяризацию. Характерно быстрое начало действия и быстрый его конец. Эти лекарства эффективны при желудочковых тахиаритмиях, но бесполезны при наджелудочковых тахиаритмиях (мало влияют на ЧСС и проводимость).
1С: этацизин, пропафенон (ритмонорм). Они имеют длительные эффекты: замедляют деполяризацию (уменьшают подъем 0-фазы), слабо влияют на реполяризацию и на j действия, уширяют QT, сильно подавляют проводимость импульса в малых дозах. Для лечения в амбулаторных условиях весьма удобен ритмонорм, который обладает легкими свойствами b-адреноблокатора (b-АБ) и антагониста Са+2. Основные показания: желудочковые аритмии, тахикардия с узким QRS, МА.
Такие препараты, как этмозин или алапенин трудно отнести к какому-либо классу.
II класс. Блокаторы b-адренорецепторов (b-АБ): неселективные (пропранол = обзидан), кардиоселективные (атенолол и с внутренней симпатической активностью ¾ пиндолол = вискен). Они ограничивают симпатическое влияние на сердце (конкурентная блокада b-рецепторов): снижают автоматизм предсредий и желудочков, замедляют скорость А-В проводимости (повышают рефрактерность А-В узла), не влияют на QT. b-АБ чаще применяют при желудочковых аритмиях и МА. К побочным действия относятся: отрицательное ино-хронотропное действие, снижение ударного объема сердца (УОС) с последующим усилением проявлений ХНК, синдром "отмены" (после прекращения длительного приема препарата, возможно возобновление аритмий). b-АБ ¾ наименее токсичные лекарства и возможно являются наиболее сильными из антиаритмических средств. b-AБ противопоказаны при: БА, ХОЗЛ, А-В блокадах, СССУ.
III. Блокаторы каналов калия: кордарон = амиодарон, соталол = соталекс (в дозе 160 мг обладает свойствами b-АБ, а в дозе более 200 мг имеет свойства 3-го класса), бретилий = орнид. Они обладают антиадренергическими свойствами, блокируют каналы К+, удлиняют фазу реполяризации и j действия (QT). Основные показания: желудочковые аритмии, тахикардии с узким QRS, МА. К побочным действиям относят: изменения функции щитовидной железы (они противопоказаны при ее патологии), сужение полей зрения, развитие пневмонитов и фиброза легких.
IV. Антагонисты Са+2 (верапамил=изоптин). Они блокируют медленные каналы входа ионов Са+2 в клетку сердца и тем самым снижают активность СУ, замедляют проводимость в А-В узле, удлиняют рефрактерный период, не влияют на QT. Основные показания к применению ¾ тахикардия с узким QRS.
Недостатком этой классификации является то, что она не позволяет выбрать антиаритмик для лечения аритмии в клинике; кроме того, многие антиаритмики (например, кордарон или соталол) проявляют свойства нескольких классов. В настоящее время чаще используют "гамбитную" схему, дающую информацию о фармокологии антиаритмика и его влиянии на проводящую систему сердца. Эта схема удобна при оценке лекарств с похожим действием.
Антиаритмики не излечивают от аритмии (так как не ликвидируют аритмогенный субстрат), но они устраняют нарушения ритма, изменяя электрофизиологические свойства миокарда. Средняя эффективность антиаритмиков не превышает 40-60%, причем в ряде случаев (до 10%) они вызывают проаритмогенный эффект.
Обследуя больных с аритмиями, необходимо ответить на следующие вопросы:
1. Действительно ли у больного есть аритмия? Для ее верификации необходимы: тщательный сбор анамнеза (имеются ли заболевания сердца или щитовидной железы), физикальный осмотр, ЭКГ и ЭхоКГ. Так, важно уточнить: не говорили ли больному ранее, что у него имеется WPW; было ли начало приступа острым или постепенным; были ли похожие атаки аритмии в прошлом, и зарегистрированы ли они на ЭКГ; можно ли было подсчитать частоту пульса в период аритмии.
2. Каковы последствия аритмии? Наличие головокружений, слабости, обмороков, нарушения зрения, помех нормальной работоспособности, дискомфорта в грудной клетке. От этого зависит тактика лечения.
3. Имеются ли у больного проблемы в сердце? Например, врожденные пороки сердца, аневризма ЛЖ, шумы в сердце или его большие размеры.
4. Что провоцирует развитие аритмии? Когда началась аритмия, где был больной, и что он делал?
5. Что прекращает приступ (изменение положения тела, маневры или прием определенных лекарств)?
6. Какие лекарства принимает больной и как часто пьет кофе или чай, злоупотребляет ли алкоголем или курением?
7. Как лечить больного? Фармакологически, ЭИТ, хирургически или вообще не лечить?
Помощь ЭКГ в диагностике аритмий:
· Анализ зубцов P;
· Найти общий РР интервал;
· Есть ли связь между волной Р и QRS (ргулярный или нерегулярный интервал R-R);
· Анализ QRS (аритмии могут быть наджелудочковые и желудочковые);
· Сравнение данной ЭКГ со старыми;
· Анализ влияния физической нагрузки (ФН);
· Оценка эффективности массажа каротидной зоны;
· Оценка принимаемых лекарств (в ряде случаев они могут вызвать аритмии).
С точки зрения клиники выделяют 3 группы аритмий:
1. Неправильный сердечный ритм (на фоне нормы или тахисистолии в течение относительно длительного времени). Эти изменения не носят характера приступов или пароксизмов (экстрасистолия, МА).
2. Пароксизмальные нарушения ритма (различные пароксизмальные тахикардии более 90 мин).
3. Брадикардии ¾ замедленный ритм (менее 60 в мин; правильный или неправильный).
Изменение автоматизма СУ. Синусовая брадикардия (СБ) не является патологией. СБ может быть обусловлена: снижением скорости реполяризации СУ, повышением абсолютного значения j покоя и j порогового. На практике СБ выявляется при: высокой тренированности у спортсменов или у пожилых лиц (вследствие замедления собственного ритма сердца с возрастом); повышении тонуса n. vagus (ваготония) при менингите, опухолях мозга (из-за повышения внутричерепного давления); болезнях ЖКТ (язвенной и желчекаменной болезни, почечной колике); инфекциях (поздние стадии гепатита, грипп, брюшной тиф); передозировке лекарств (СГ, b-АБ, хинидин); болезнях миокарда (ОИМ нижней локализации, кардиосклероз ¾ чаще и реже ¾ миокардиты, кардиомиопатии).
Необходимость в лечении СБ возникает при: ЧСС менее 50 в мин, появлении клинических симптомов и нарушений гемодинамики.
Ригидный ритм при брадикардии может быть одним из проявлений синдрома"слабости синусового узла" (СССУ), когда импульсы из этого узла не могут активировать предсердия. Синонимы СССУ: синдром "ленивого узла", "больного СУ", отказа СУ, бради-тахикардии (периоды тахиформы МА сменяются в течение нескольких секунд асистолией, а затем снова возникает СБ). В основе СССУ (чаще является приобретенным) лежит выраженная органическая дисфункция СУ (плохая генерация импульса Р клетками) и СА узла в большей степени, обусловленная его сильными дегенеративными, морфологическими изменениями вследствие различных болезней сердца. Последние приводят к сдвигам в системе ионных потоков, формирующих синусовый ритм. В более молодом возрасте СССУ развивается при дилатационной кардиомиопатией (ДМКП), а в старшем возрасте ¾ при ИБС.
СССУ может быть первичный (истинный) и вторичный, когда дисфункция СУ обусловлена повышением ваготонии или чувствительности СУ к вагусным влияниям. При СССУ возможны самые сложные комбинации различных нарушений ритма и проводимости: остановка (отказ) СУ кратковременная или длительная с симптомами Морганьи-Адам-Стокса (МАС); стойкая брадикардия с ЧСС менее 50 в мин (в 50%), не связанная с приемом лекарств; приступы МА (брадисистолическая форма); СА блокада; миграция источника ритма в комплексе с предсердными или желудочковыми ЭС; пароксизмы предсердной тахикардии; синдром чередования тахи-брадиаритмий; посттахисистолическая депрессия ритма (то есть, медленное восстановление ритма после прекращения тахикардии, что может быть причиной обмороков); АВ блокады с синкопальным состоянием (обмороком).
Основные причины СССУ:
· Внутренние (имеется патология СУ) и внешние (функция СУ нормальная, но нарушена автономная регуляция);
· Ишемия ¾ болезни сердца (ОИМ с вовлечением СУ; ИБС, ревматические пороки сердца, ГБ; недостаточное кровообращение СУ вследствие сужения питающей его артерии; кардиомиопатии).
· Гормонально-обменные нарушения.
· Воспаление ¾ поражения сердца при ДБСТ, острой ревматической лихорадке (ОРЛ).
· Инфильтрация ¾ амилоидоз, системная склеродермия (ССД).
· Наследственная патология СУ.
· Передозировка лекарств (хинидина, СГ, b-АБ).
Как правило, СССУ возникает у лиц старше 60 лет, и в основе его лежит фиброз.
Клинические симптомы СССУ:
· обмороки (в 40-70% случаев) из-за отказа АВ узла или неадекватного УОС;
· пароксизмы головокружений (в 20%);
· сердцебиения (в 10-20%) и стенокардия;
· одышка, усталость (в 8-20%);
· отсутствие ускорения ЧСС в условиях ФН или повышения лихорадки.
Выделяют 3 формы СССУ: постоянную, преходящую и латентную (скрытую).
Диагностика СССУ комплексная и включает: тщательный анамнез, анализ ЭКГ плюс специальные неинвазивные тесты:
1. Холтеровское мониторирование (Хм) ЭКГ за 24 ч (выявляются периоды СБ с ЧСС менее 40 в мин днем и ЧСС менее 30/мин во время сна, ночью; остановки более 3 с, синдром тахи-брадикардии).
2. Фармакологическая проба с атропином (или изадрином) ¾ в/в 1-2 мг (0,02 мг/кг). При СССУ ЧСС повышается менее 25% от исходного уровня или ЧСС повышается не более 90/мин (это признак "органики"), а при вторичных дисфункциях СУ ¾ ЧСС обычно повышается более 90 в мин. Тест с атропином недостаточно специфичен, нормальный ответ не исключает наличие СССУ.
3. Электрофизиологическая оценка дисфункции СУ с помощью чрезпищеводной электрокардиостимуляции (ЧПЭС) предсердий в течение короткого времени (замеряется время восстановления СУ, время сино-атриального проведения).
4. При пробе с ФН у больных СССУ рост ЧСС составляет менее 90% от должной максимальной ЧСС (они не могут ее достичь по сравнению с контролем).
5. Стимуляция каротидного синуса справа в течение 10 с у ряда больных с СССУ вызывает асистолию более 3 с (хотя аналогичное отмечается и у лиц с гиперчувствительностью СУ).
Лечение СССУ. У больных с СССУ все антиаритмические лекарства могут вызвать выраженную брадикардию или даже асистолию. Поэтому данный синдром ¾ противопоказание к приему антиаритмиков. В целом СССУ ¾ удел кардиохирургов (обычно больному необходима постановка ИВР). При острых эпизодах брадиаритмии с клинической симптоматикой (например, обмороки) вводят атропин в/в по 0,5-1 мг, вторично через 5 мин и до достижения эффекта или суммарной дозы 3 мг (0,04 мг/кг). Иногда используют длительный оральный прием теофиллина (по 200-400 мг 2 р/д). Если нет эффекта, то используется временная электрокардиостимуляция (ЭКС).
Нарушение проведения импульсов (А-В блокады).Причинами А-В блокад являются:
· органические поражения сердца(воспалительные процессы в миокарде, рубцовые изменения А-В узла) более, чем в половине случаев. Причем, в острых случаях ¾ это чаще ОИМ, миокардиты, а при постоянных формах ¾ хроническая ИБС. У пожилых больных А-В блокады обычно вызваны ревмопороками, ИБС или ОИМ нижней локализации, тогда как у молодых ¾ воспалительными заболеваниями сердца (ОРЛ, вирусный миокардит, постмиокардитический кардиосклероз);
· передозировка лекарств: СГ, хинидин, b-АБ, кордарон, новокаинамид;
· нарушения электролитного обмена (гиперкалиемия) или некоторые патологические состояния, связанные с увеличением уровня калия в организме;
· функциональные нарушения (например, ваготония у спортсменов).
Механизмы замедления А-В проводимости: повышение j порогового в клетках проводящей системы; снижение скорости проведения импульса по одной или двум ветвям; усиление затухающего проведения в зоне нормального А-В узла или в другом участке проводящей системы.
При А-В блокаде 1-й степени до желудочков доходят все импульсы, но скорость их проведения понижена. Субъективных ощущений нет, диагностика проводится по ЭКГ (удлинение PQ более 0,20 с).
При А-В блокаде 2-й степени (не все импульсы достигают желудочков, которые могут сокращаться под действием отдельных импульсов) гемодинамика определяется основным заболеванием и сократительной способностью миокарда. Выделяют два варианта А-В блокады 2-й степени: Мобитц I с постепенным удлинением PQ и выпадением QRS с периодами Самойлова-Викенбаха (при этом типе повреждение сравнительно высокое и прогноз обычно благоприятен) и Мобитц II (соотношение Р:QRS=3:2 или 4:3, часто изменяется комплекс QRS) с низким поражением и неблагоприятным прогнозом (предвестник полной А-В блокады).
При полной поперечной А-В блокаде (3-й степени) полностью прекращается проведение импульса к желудочкам, в них появляется свой гетерогенный очаг идиовентрикулярного ритма с ЧСС менее 40 в мин (если страдает А-В узел) и менее 20 в мин, если страдает ножка пучка Гиса. Причем, чем ниже автоматизм, тем тяжелее клиника. На ЭКГ отмечается полная диссоциация: у предсердий свой ритм, а у желудочков - свой, но более медленный. При этом часто уменьшается МОК, так как повышение УОС при таком редком ритме не обеспечивает компенсации, тем более при низкой сократимости миокарда (предсердия сокращаются, а желудочки могут "стоять"). На этом фоне кровь не поступает на периферию, может развиться острая гипоксия мозга (если выпадает 6-8 комплексов) с приступами М-А-С, когда больной внезапно бледнеет, а потом синеет, теряет сознание и падает. Тоны сердца не слышны, пульс не определяется. Могут быть непроизвольные мочеиспускание и дефекация. Возможна смерть через 3-4 минуты, но часто приступ заканчивается на 1-2 минутах вследствие включения идиовентрикулярного водителя ритма желудочков. После приступа М-А-С больной обычно не помнит того, что с ним было. Синдром М-А-С часто возникает при переходе неполной А-В блокады в полную, при прогрессировании нарушений А-В проведения (при этом собственный автоматизм еще не успел выработаться). На ЭКГ в этот период отсутствует весь сердечный комплекс, нет Р, Т и QRS, вместо них видна длительная пауза, которая бывает кратной каком-либо числу промежутков R-R. Острая, преходящая полная А-В блокада нередко (в 8% случаев) развивается в начальный период ОИМ. Другим частым осложнением полной А-В блокады является прогрессирование ХНК, особенно при ФН вследствие малой ЧСС.
Если нет критического снижения ЧСС и выраженных нарушений гемодинамики, то жалоб у больного может и не быть. В остальных случаях больные отмечают жалобы на: сердцебиение, ощущение остановки сердца, упадок сил, головокружения, темные круги перед глазами, одышку и другие проявления сердечной недостаточности.
Клинически различают два варианта брадикардии: с правильным ритмом (полная А-В блокада) и неправильным ритмом (отдельные формы неполной А-В блокады). Объективно при аускультации сердца у больных с неполной А-В блокадой выявляют картину, похожую на наличие ЭС. При полной А-В блокаде (ЧСС менее 40 в мин) тоны ослаблены, периодически можно услышать "пушечный" 1-й тон вследствие одновременного сокращения желудочков и предсердий. Пульс обычно удовлетворительного наполнения и после ФН заметно не увеличивается.
Лечение А-В блокад.При обнаружении А-В блокады 2-3 степени, особенно у немолодого человека, обязательна госпитализация для установления характера блокады и основного патологического процесса. Как правило, при А-В блокаде 1-й, 2-й степени (когда большая часть импульсов все же достигает желудочков) и даже полной А-В блокаде с ЧСС более 50 в мин специального лечения не требуется. Необходим ЭКГ контроль и отмена лекарств, вызывающих замедление проводимости импульсов (антиаритмики или СГ). Показания к интенсивной терапии ¾ появление синдрома М-А-С, острая левожелудочковая недостаточность (ОЛЖН), падение АД, ангинозная боль и прогрессирующее урежение ЧСС.
Алгоритм купирования брадикардии:
Наличие жалоб, снижение АД, появление симптомов СН или обмороков,
внезапное урежение пульса менее 45 в мин
ß ß
ЭКГ Þ СБ Þ лечения не требуется,
ß необходимо наблюдение
А-В блокада 2-3 ст.
ß
дистальный тип проксимальный тип (ЧСС стабильно более 45)
ß ß
Изадрин Атропин (для уменьшения вагусного
(изопротеренол 0,1% 1 мл) влияния) в/в 0,5 - 1 мг через 5 мин
в/в, капельно 1-10 мкг/мин, до получения эффекта или достижения
(скорость зависит от АД и суммарной дозы в 3 мг (0,04 мг/кг)
ЧСС) в 250 мл 5% раствора и/или эуфиллин
глюкозы или ЭКС (лучше чрезкожная)
Вместо изадрина можно вводить другие препараты, усиливающие симпатическое влияние на проводящую систему:
· адреналин (при выраженной брадикардии и гипотонии) в/в, капельно,
1 мг в 250 мл 5% раствора глюкозы со скоростью 2 мкг/мин или норадреналин (0,2% 1,0 мл на глюкозе), или допамин (100 мг). Скорость вливания зависит от ЧСС и АД;
· эуфиллин в/в, медленно, струйно 240-480 мг;
· алупент (0,05% 1,0 мл) в/в, капельно, 5-10 мг в 300 мл физиологического раствора (скорость вливания 20 капель в мин).
При развитии приступа М-А-С используют: кулачный ритм (серия ударов кулаком по грудине с целью механического запуска сердца) ® введение 1 мг атропина (при необходимости повторно) ® адреналина (в/в, 2-10 мкг/кг) ® временную ЭКС (с помощью зонда или катетера, вводимых в правый желудочек сердца).
В ходе лечения А-В блокад нельзя назначать препараты калия и СГ. Наоборот, больным назначают дополнительно мочегонные (фуросемид, лазикс, гипотиазид), выводящие калий.
В целом, всем больным с А-В блокадой 2-3 степени, сопровождающейся: клиническими симптомами (приступы М-А-С, появление ХНК или ее усиление); стойкой брадикардией менее 40 в мин без симптоматики; периодами асистолии более 3 с; эктопическими ритмами, требующими приема лекарств, вызывающих подавление проведения импульса с последующей симптоматической брадикардией; уширением QRS более 0,14 с ¾ показана имплантация ИВР.
Нарушение внутрижелудочковой проводимости (полные и неполные блокады левой и правой ножек пучка Гиса) встречаются у 1% терапевтических больных, но их частота повышается до 15% при ОИМ. Сами по себе блокады ножек пучка Гиса мало влияют на течение основного заболевания, не приводят к существенным нарушениям гемодинамики, но могут быть предвестниками полной А-В блокады. Блокады ножек пучка Гиса, как правило, не требуют лечения, необходим лишь ЭКГ контроль.
Учащенный ритм.
Лечение СТ требует прежде всего лечения основного заболевания (то есть, устранения основного фактора). Например, при ХНК ¾ это назначение… Таблица 23Аритмии как синдром болезни
Тахиаритмии включают: частые ЭС, суправентрикулярную пароксизмальую тахикардию (СПТ), мерцательную аритмию (МА) и трепетание предсердий (ТП),… Пароксизмальные регулярные тахикардии (ПТ) чаще обусловлены механизмом… · с неизмененным комплексом QRS ¾ суправентрикулярная ПТ (СПТ);Клинические симптомы ПЖТ вариабельны (от отсутствия симптоматики до гемодинамического коллапса) и зависят от длительности ПЖТ, ЧСС и выраженности патологии сердца. Больные жалуются на: внезапное начало сердцебиений, ангинозная боль (или чувство тяжести в сердце), слабость, головокружение, обморок, симптомы ОЛЖН (вследствие потери вклада предсердий в наполнение желудочков и их ненормальной активации). Могут быть аритмический шок и симптомы ЖКТ нарушений (тошнота, рвота, метеоризм). Стабильность гемодинамики у больного не исключает наличия у него ПЖТ.
Алгоритм купирования ПЖТ (потенциально летальной аритмии). Если у больного приступ ПЖТ длится более 30 с и имеются признаки нестабильности гемодинамики (снижение АД систолического менее 90 мм рт. ст., нарастание ХНК и появление ОЛЖН), ангинозная боль или ОИМ, потеря сознания, срочно проводят ЭИТ. Если нет эффекта, то вводят в/в лидокаин или новокаинамид (или сульфат магнезии). Если нет эффекта ¾ проводят повторно ЭИТ (или ЧПЭС).
Сразу удар кулака в нижний край грудины
ß
Если больной неплохо переносит ПЖТ, и нет значимых гемодинамических нарушений вводят:
Лидокаин ¾ в/в быстро (за 1 мин), болюсом, без разведения 50-100 мг или 3-5 мг/кг (10 мл 1% раствора содержат 100 мг). Затем каждые 5 мин по 40-60 мг до достижения суммарной дозы 200 мг (20 мл раствора или 3 мг/кг). Затем постоянно в/в, капельно со скоростью 3 мг в мин в течение 30 мин (и даже на протяжении 12 ч!), но не более 600 мг/ч (60 мл 10% раствора). Лидокаин обычно хорошо переносится и дает небольшие побочные эффекты. Если нет эффекта в течение 20-30 мин (эффективность лидокаина составляет около 10%), берем другой препарат или проводим ЭИТ.
ß нет эффекта
Новокаинамид(можно начинать сразу с него)¾в/в болюс по 100 мг
(1 мл) или 10-15 мг/кг с интервалом в 5 мин (обычная скорость 50 мг/мин в зависимости от АД) до достижения положительного или побочных эффектов, или суммарной дозы 1 г (10 мл 10% раствора). Препарат вводится под постоянным контролем АД (каждые 5 мин) и длительности QRS. Можно вводить новокаинамид и в/в капельно, медленно со скоростью 20-30 мг/мин в течение 1 ч. Эффективность новокаинамида составляет около 30%. Но даже если он не купирует ПЖТ, то уменьшает скорость сокращения желудочков и улучшает переносимость больным ПЖТ.
В качестве резерва используют:
· Кордарон ¾ в/в 350-450 мг (5 мг/кг) без разведения, за 10-30 мин.
· Этмозин ¾ в/в 150 мг (4 мл 2,5% раствора) за 3 мин.
· Сульфат магния ¾ в/в 1-4 г за 2 мин (10-20 мл 25% раствора без разведения), а далее капельно 3-20 мг/мин. Он наиболее эффективен при "пируэте".
ß нет эффекта
ЭИТ
В целом для купирования ПЖТ препаратом первого ряда является лидокаин, а второго ¾ новокаинамид, мекситил, флекаинид, пропафенон.
Профилактика повторных приступов ПЖТ ¾ часто это более трудная задача, чем купирование пароксизмов ЖТ (используют препараты 1 класса А, В, С и 3 класса). Если приступы возникли на фоне ОИМ, то после купирования ПЖТ вводят в/в капельно лидокаин (если он эффективен) со скоростью 2-3 мг/мин, в течение 1-2 суток. Позднее лидокаин принимают внутрь в поддерживающих дозах, в том числе и для профилактики частых СПТ (более 4 раз в месяц) или новокаинамид (0,5 г 4 р/д), или кордарон (0,2 г 3 р/д), или ритмонорм (0,15-0,3 г 3 р/д), b-АБ, хинидин (0,2 г 2-3 р/д) или комбинацию: хинидин + b-АБ.
В целом противорецидивное лечение должно продолжаться не менее месяца после последнего пароксизма ЖТ. Сложность профилактического лечения заключается в том, что через несколько месяцев к принимаемому антиаритмику развивается толерантность, и он перестает эффективно действовать.
Если опасная для жизни ПЖТ возникла из-за повреждения миокарда (например, вследствие ОИМ), то основное внимание в лечении должно быть направлено на лечение болезней сердца (или внесердечных заболеваний).
При рецидивирующей ПЖТ и рефракторной к лечению (особенно на фоне WPW) проводят оперативное лечение: резекцию или разрушение дополнительных проводящих путей (пучка Кента), деструкцию A-В узла с навязыванием ритма кардиостимулятора (ИВР). Опасность этих операций сравнительно невелика, поэтому они могут с успехом заменить лекарственную терапию. В последнее время имплантируют автоматический антитахикардиальный кардиовертер-дефибрилятор, который постоянно "следит" за электрической активностью сердца и выявляет появление опасной тахикардии, которая эффективно ликвидируется программируемой серией электрических токовых импульсов.
Прогноз при ПЖТ вариабельный. Так, если ПЖТ возникла в течение 6 недель после ОИМ, то прогноз плохой: 75% больных умирает в течение года. В целом больные с нестабильной ПЖТ после перенесенного ОИМ имеют в 3 раза больший риск летальности, чем больные после ОИМ, но без приступов ПЖТ. Лица с ПЖТ, но без органических заболеваний сердца, имеют относительно хороший прогноз.
Таблица 24
Эффективность различных антиаритмиков при нарушениях ритма
При ФЖ(чаще возникает у больных ИБС или при ударе электрическим током)на ЭКГ регистрируются частые и беспорядочные сокращения (ундулирующая кривая… · первичной (возникает в первые 48 часов ОИМ, особенно на фоне блокад правой… · вторичной, в основе которой лежит тяжелое поражение миокарда. Эта ФЖ развивается у больных с ИБС, ХНК с тяжелым…Явно неправильный ритм
· предсердные ЭС (зубец Р предшествует QRS), которые находят у 60% здоровых лиц при Хм (они обычно не имеют симптоматики, доброкачественные и не… · из АВ узла, чаще встречаемые (на ЭКГ отрицательный Р или ретроградный,… · желудочковые (нет Р; ORS уширен, более 0,14 с и чаще похож на блокаду ножек пучка Гиса). Если частота желудочковых…Классификация желудочковых ЭС
| Класс | ЭКГ за 24 ч | ВЭП |
| Нет ЭС | Нет ЭС | |
| Изолированные, одинаковые, менее 30/ч | То же, менее 3/мин | |
| То же, но более 30/ч | То же, но более 1/мин | |
| Полиморфные | То же | |
| Групповые (две подряд), залповые (три и более подряд), неустойчивая ЖТ | То же | |
| "Ранние" (R на T) | То же |
Опасность ЭС возрастает с ростом уровней градации. Так, редкие желудочковые ЭС (суточное количество около 100-200) 1-2 класса, особенно функционального характера, не требуют лечения. Необходима нормализация режима труда и отдыха, за исключением желудочковых Э на фоне ОИМ. Зато ЭС
3-4-5 классов (практически всегда органические) являются угрожающими в плане развития ЖТ, ФЖ (что повышает риск развития смерти). Бывает достаточно одной ЭС "R на T", чтобы вызвать ФЖ. ЭС 3-4-5 классов надо лечить упорно и активно.
Клинические проявления ЭС весьма широки: от безобидных (чаще предсердных ЭС), не замечаемых больным (например, редкие, одиночные желудочковые ЭС, не вызывающие нарушений гемодинамики) до более грозных, определяемых субъективно как "замирание сердца, сердцебиение, толчки в груди". Клинически экстрасистолическая волна ¾ это преждевременный, более слабый удар сердца (и пульса соответственно). При аускультации во время ЭС слышен преждевременный, более громкий тон. Обычно "залповые" ЭС больные чувствуют, а бигеминию ¾ нет. Могут быть и обмороки при желудочковых ЭС. При их большой частоте может быть снижение коронарного кровотока на 25%. Все это может мешать работоспособности больного. При групповых ЭС могут быть головокружение, тошнота. Обычно ЭС функционального генеза (без нарушения сократимости миокарда) "ярче" воспринимаются больным. И, наоборот, при органических поражениях сердца больные ЭС часто не замечают или быстро привыкают к ним.
Лечение. В последнее время используют не продолжительный, эмпирический "перебор" лекарств, а тестирование лекарства в условиях "острого опыта" (разовая доза равняется половине суточной). Назначают больному однократно пробную дозу антиаритмика с длительной регистрацией ЭКГ: до и после приема (введения) лекарства. Проба расценивается как положительная, если частота ЭС снижается в 3 и более раз (или на 50-75% от исходного уровня) или исчезают ЭС 3-5 классов.
При лечении ЭС на фоне заболеваний сердца первостепенное значение имеет лечение основного заболевания и сопутствующих болезней, вызывающих рефлекторную ЭС (например, ЖКБ, патология щитовидной железы или хронический тонзиллит ¾ мощная рефлекторная зона); устранение пусковых факторов развития ЭС; коррекция образа жизни (ограничение приема кофе, алкоголя, отказ от курения), диеты и ФН. Выбор лекарства является последним этапом лечения ЭС, до этого проводят коррекцию вышеназванных факторов риска развития ЭС.
Большинство наджелудочковых ЭС протекают без симптомов и не требуют лечения. Но если эти ЭС вызывают сердцебиения или провоцируют появление суправентрикулярной тахикардии (СПТ), то необходимо лечение.
Обычно при наджелудочковых ЭС (часто связанных с нервным перенапряжением) используют комплекс седативных средств (валокардин, корвалол, настойка валерьяны или пустырника) плюс b-АБ в небольшой дозе. Например, пропранол в/в по 1 мг в течение 1мин, далее каждые 30 мин повышается доза на 1 мг до купирования или прием внутрь по 40 мг 3 р/д, с постепенным повышением дозы (при отсутствии эффекта) до 300 мг/д и последующим переходом на поддерживающие дозы. Цель лечения ¾ снизить неприятные ощущения, вызываемые ЭС, и предупредить пароксизмы ЖТ (ФЖ). Для этого можно назначить внутрь кордарон (400-600 мг/д) или верапамил (120-240 мг/д). Если эти лекарства не дают положительного эффекта, то применяют: новокаинамид, хинидин (если нет ХНК). У больных с наличием выраженных проявлений ХНК можно комбинировать СГ с пропранолом, но под контролем ЧСС.
Если у больного без патологии сердца возникли редкие, изолированные и бессимптомные желудочковые ЭС, то, независимо от их формы, лечения не проводят. При появлении на фоне желудочковых ЭС симптоматики, беспокоящей больного, или ухудшения его самочувствия необходима терапия (снижения частоты желудочковых ЭС). При желудочковых ЭС назначают пропранол (длительное время) внутрь 40 мг 3 р/д, особенно, если ЭС возникают: в дневное время под влиянием стрессов, ФН; на фоне СТ и гиперфункции адреналовой системы. b-АБ нельзя резко отменять (дозу плавно снижают на четверть 1 раз в 5 дней). С высоким риском внезапной смерти у больных с патологией сердца обычно связано наличие частых желудочковых ЭС. Поэтому цель лечения заключается в снижении их частоты.
Если у больного ИБС появляются острые желудочковые ЭС и гемодинамически значимые, то препаратом 1-го ряда будет лидокаин, а второго ряда ¾ новокаинамид, хинидин, В-АБ или соталол. Если эти Э хронические, гемодинамически значимые, то препаратами 1-го ряда будут лидокаин, мекситил, флекаинид, ритмонорм, b-АБ, соталол.
Если не эффективны b-АБ, то у госпитальных больных (особенно на фоне ОИМ и для профилактики возможной первичной ФЖ) вводят:
· лидокаин ¾ в/в, струйно, болюс 60-b80 мг (ударная доза=1 мг/кг) за
2 мин. Затем, через 30 мин (т.к. при в/в введении действие лидокаина через
20 мин заканчивается) еще в/в 40 мг струйно, до достижения суммарной дозы
5 мг/кг. Потом, в/в, капельно длительно 120-200 мг со скоростью 1 мг/мин, или
· кордарон ¾ в/в, медленно 450-600 мг (или внутрь 600-800 мг), или
· новокаинамид ¾ в/в, медленно 0,5-1 г (может вызвать резкое снижение АД), или
· этацизин ¾ в/в, болюс, 50-100 мг, за 5 мин (доза=0,45 мг/кг).
Кордарон, ритмилен, аймалин, этацизин эффективны как при предсердной ЭС, так и при желудочковой ЭС.
· При ЭС с брадикардией предпочтительнее ритмилен, аймалин (в/в, медленно по 2 мл 2,5%, то есть 50мг), этмозин (0,2 г 3 р/д). При недостаточной активности одного антиаритмика используют их комбинации, но… · кордарон (0,2 г 2 р/д) + ритмилен (0,1 3 р/д) или этацизин (50 мг 3 р/д).Этиология МА
Трепетание предсердий (ТП) ¾ этиология и генез развития похожи на МА. ТП почти всегда возникает у больных с органическими поражениями сердца.… Нередко в результате лечения СГ развивается интоксикация и синдром Фредерико… Осложнения МА.Если развилась пароксизмальная тахиформа МА, то часто появляются следующие осложнения:Алгоритм купирования ТП
ß ß нет да ß ßЗАБОЛЕВАНИЯ КИШЕЧНИКА
Основные сведения о физиологии пищеварения в кишечнике (без этого трудно понять причину ряда симптомов, появляющихся при болезнях кишечника).… Тонкая кишка (имея длину около 6,6 м и поверхность равную 2×108 см2)… Главная роль толстой кишки (длина около 1,25 м; диаметр от 8,5 см в слепой кишке, с постепенным уменьшением до 2,5 см…Классификация НЯК
по течению:
· острая, молниеносная (фулминантная) форма;
· хроническое, непрерывное, постоянное течение (симптомы сохраняются более 6 месяцев). Часто со временем поражается весь кишечник. Встречается в 10% случаев;
· хроническое рецидивирующее (в период ремиссий нет симптоматики).
По степени тяжести:
· легкая (в основном -- проктит);
· средняя (прокто-сигмоидит);
· тяжелая (тотальный колит).
Клиника НЯК вариабельна. Так, у большинства больных в течение первого года болезни после первого приступа (в половине случаев легкого) начинаются рецидивы болезни. Это указывает на переход в хроническую стадию. Обычно средний период от начала болезни до постановки диагноза составляет один год (диагноз НЯК ставится, как правило, только в больнице).
Выраженность клиники зависит от распространенности процесса. Так, при ограниченных формах (например, язвенный прокто-сигмоидит) клиника выражена слабо (могут быть ректальные кровотечения или позывы-тенезмы). У многих больных воспаление распространяется в восходящем направлении. В 85% случаев НЯК протекает по форме в виде легкой или средней степени тяжести, по типу преходящих эпизодов обострения заболевания.
Хроническая рецидивирующая форма НЯК (самая частая). Начало постепенное, течение циклическое: обострения (их длительность 4-12 недель) сменяются ремиссиями разной длительности. По мере прогрессирования болезни обострения становятся все более длительными, а ремиссии ¾ короче.
Легкая форма НЯК (проктит, прокто-сигмоидит) имеет следующие основные симптомы: диарею с макроскопически видимой кровью ("прожилками" или небольшими ректальными кровотечениями), слизью и гноем. Могут быть периодические кишечные колики. Количество дефекаций до 6 раз в день, температура тела нормальная, потеря веса не превышает 10%. Нет общих симптомов: тахикардии, выраженной анемии и повышения СОЭ (оно менее 20 мм/ч). Общее состояние хорошее. При эндоскопии кишечника выявляют: отек, гиперемию и контактную кровоточивость.
Средняя тяжесть НЯК: количество дефекаций 6-10 раз в день (нередко ¾ "срочные", по ночной схеме), температура тела = 38оС, потеря массы тела ¾ 10-20%; СОЭ превышает 20 мм/ч; Нв снижается (за счет кровопотерь) до 100 г/л. Стул ¾ полуоформлен, с постоянной примесью небольшого объема крови. Возникают схваткообразные боли в животе перед дефекацией. В период обострения общее самочувствие плохое. Объективно: болезненность по ходу толстого кишечника. Эндоскопия: язвы, эрозии, слизь, гной, псевдополипы. Внекишечные симптомы встречаются редко (практически их нет).
Тяжелая форма НЯК: профузная диарея боле 10 раз в день; кал жидкий с большим количеством крови, слизи и гноя. Температура тела более 38оС; тахикардия, выражена железодефицитная анемия (Нв менее 100 г/л) сложного генеза; СОЭ более 30 мм/ч; лейкоцитоз (20-30×109/л) со сдвигом влево; потеря массы тела более 20%; снижение альбуминов (за счет потери белка через кишечник вследствие изъязвлений). Выявляются: абдоминальные боли, анорексия и обезвоживание. Часто отмечаются внекишечные проявления НЯК: артрит, узловатая эритема и др. Возможно развитие кишечных осложнений: токсическая мегаколон, перфорация толстой кишки.
Физикальный осмотр неспецифичен: может быть незначительное вздутие живота (за счет заглатывания воздуха, проникновения газа при пищеварении в кишечнике, жизнедеятельности кишечной микрофлоры и повышенного поступления газа из крови в кишечник); болезненность по ходу толстого кишечника (чаще в левом нижнем квадранте); урчание, переливание и плеск по ходу кишечника. Для НЯК характерны следующие синдромы ("колитный" симптомокомплекс):
3. Болевой (неспецифичен, но всегда присутствует).
4. Воспалительный: общий: (лихорадка, ускорение СОЭ, лейкоцитоз) и местный (лейкоциты, гной и кровь в кале).
5. Диспептический(неспецифичен, но всегда есть неприятный вкус, горечь и сухость во рту, отрыжка, тошнота, чувство дискомфорта в животе).
6. Моторно-эвакуационных и секреторно-экскреторных нарушений (экссудативная диарея) вследствие изменения движения воды и электролитов, нарушения резервуарной функции и ускорения перистальтики кишок. Характерны ложные позывы, а на поздних стадиях ¾ ощущение неполного опорожнения.
7. Кишечной аутоинтоксикации (слабость, головная боль, плохой сон, снижение работоспособности, астенизация) ¾ есть всегда, но с разной степенью выраженности.
8. Дисбиоза вследствие присоединения вторичной инфекции (стафилококка, протеуса, кандид и др.).
9. Иммунных нарушений (только при тяжелых формах) с внекишечной симптоматикой (артрит, узловатая эритема, гингивит).
10. Мальабсорбции (только при тяжелых формах) с диспротеинемией, потерей белка, нарушением электролитного баланса за счет потери жидкости (более 5 л в день).
По данным ирригоскопии при НЯК выявляют: язвенные дефекты, (как неровность контура кишечника или как депо бария) псевдополипоз, отсутствие или неравномерность гаустр (симптом "водопроводной трубы"), укорочение кишечника. Морфологические изменения при НЯК заключаются в поражении слизистого и подслизистого слоев.
Критерии диагностики НЯК:
· специфичные (диарея и/или ректальной крови более 6 недель, воспаление слизистой с геморрагиями и/или изъязвлениями по данным эндоскопии);
· типичные (эндоскопические и клинические).
ОсложненияНЯК:
Местные:
· токсическое, быстрое расширение толстой кишки до диаметра более 6 см на фоне выраженной интоксикации (токсическая мегаколон), которое формируется у 2-10% госпитализированных лиц (если произошла перфорация кишки, то летальность превышает 30% ¾ необходима срочная операция);
· перфорация толстой кишки (в результате перерастяжения и истончения стенки, повышения давления в просвете кишки) с развитием перитонита. Диагностика перфорации толстой кишки затруднена вследствие снижения порога болевой чувствительности на фоне выраженной интоксикации;
· кишечное кровотечение (массивное, редко без наличия выраженной активности процесса) из-за флебитов стенки кишки и ее изъязвления;
· сужение и полипоз кишки; развитие вторичной кишечной инфекции (кишечный сепсис);
· повышение вероятности развития рака толстой кишки в 8-30 раз на фоне длительно (более 10 лет) и непрерывно протекающего НЯК. Причем, многие ранние проявления рака кишки на фоне НЯК (незначительная ректальная кровоточивость, нарушения функции кишечника) трудно интерпретировать. Так, изъязвления и псевдополипы часто скрывают небольшие раковые опухоли.
Общие: поражение суставов (в 20% случаев) и кожи по типу узловатой эритемы (17%), зрения (увеит, иридоциклит) и печени.
Быстрое прогрессирование тяжелой атаки и неэффективность консервативной терапии служат показанием к операции. Ее характер и объем (колпроэктомия, субтотальная резекция толстой кишки), даже при успешном исходе, приводят к инвалидизации и социальной дезадаптации больного.
БКр (синонимы: гранулематозный терминальный илеит, сегментарный энтерит) характеризуется поражением тонкого и толстого кишечника. БКр ¾ неспецифический воспалительный, гранулематозный процесс (распространяющийся на все слои кишечной стенки), локализующийся в любом органе (от рта до прямой кишки), но чаще в терминальном отделе повздошной кишки и приводящий к образованию гранулем, некротических участков, продольных язв с последующим рубцеванием и сужением просвета кишки, формированием фистул, свищей (чаще в конечном отделе повздошной кишки) между различными частями ЖКТ (например, кишка-вагина; кишка-уретра).
БКр чаще болеют мужчины молодого возраста (у 25% болезнь начинается до 20 лет), распространенность ¾ 30-50 больных на 100.000 населения. Выявляют 2-6 новых случаев БКр в год на 100.000 населения. Чаще процесс локализуется в терминальной части тонкого кишечника (его вовлечение обуславливает нарушение всасывания питательных веществ) или начальном отделе толстого кишечника (в 45%); изолированное поражение тонкой кишки или только толстой кишки встречается у трети больных, а поражение только прямой кишки ¾ у 10-20% больных. Патология аноректальной области (трещины, свищи и язвы) встречается у 30-40% больных.
Этиология и патогенез БКр похожи на таковой при НЯК, но при БКр большую роль играет микробный фактор: бактерии (сальмонелла, шигелла, компилобактер), их метаболиты и вирусы. Механизмы запуска БКр ¾ первичное антигенное (микробное) влияние на иммунную систему тонкого кишечника, продолжительное воздействие различных неспецифических механизмов.
Патоморфология БКр: воспалительный процесс распространяется на все слои кишки (трансмурально); сегментарно ("скачками"); воспаление имеет протяженность от 3 см до 1 м; у половины больных прямая кишка не поражается (тогда как при НЯК ¾ всегда). По мере прогрессирования воспаления стенка кишки утолщается, ее просвет суживается, может развиться кишечная непроходимость. Гистологические данные: фиброз всех слоев кишечника; трещины и гранулемы, располагающиеся в подслизистом слое (поэтому эти гранулемы часто и не попадают в биопсийные пробы).
Клиника БКр тесно связана с локализацией воспалительного процесса. Выделяют: острую форму, внешне напоминающую острый аппендицит (боли, лейкоцитоз, лихорадка, метеоризм, поносы, иногда с кровью) и хроническую.
Общие симптомы. В начальных фазах хронической БКр симптоматики, как правило, нет. В типичных случаях БКр начинается с общих симптомов: выраженной общей слабости, снижения работоспособности и веса (за счет нарушения абсорбции ¾ иногда это первый симптом БКр), чувства дискомфорта, болей в правом нижнем квадранте. Может быть и лихорадка (до 50% случаев) в течение 2-4 дней, когда температура тела не превышает 38оС. У трети больных это может быть единственным симптомом БКр (проводят дифференциальный диагноз ЛНГ). Позднее присоединяются анорексия, тошнота, рвота, проявления синдрома мальабсорбции: гиповитаминозы, сухость кожи, дерматит, выпадение волос, трещины в углах рта, боли в костях и судороги (вследствие обеднения солями кальция) и др. У трети детей выявляется задержка роста (обусловленная диффузным поражением тонкого кишечника) и слабое развитие вторичных половых признаков.
Местные симптомы.При отсутствии стеноза кишечника появляются: нехарактерные периодические боли, а позднее ¾ постоянные тупые боли (иногда принимают характер колик); умеренная диарея с полужидким, часто пенистым стулом, иногда с прожилками крови, более 6 раз в сутки. Если в процесс не вовлечена прямая кишка, то тенезмов нет. При обширном поражении кишечника появляются: стеаторея (плохо переваривается жир), что придает калу сероватую окраску и мазевидную консистенцию; вздутие и урчание живота. При стенозировании кишечника (в трети случаев за счет фиксации суженной кишки) появляются симптомы частичной кишечной непроходимости: схваткообразные боли, тошнота, рвота и задержка газов и стула. При пальпации живота отмечается умеренная болезненность и в трети случаев опухолеподобное образование в правом нижнем квадранте.
Внекишечные проявления БКр: анемия (чаще вторичная, из-за скрытых кровопотерь из кишечника, недостаточного поступления железа с пищей или пониженной его абсорбцией), дефицит витамина В12, лихорадка, снижение веса, артриты, анорексия, афтозный стоматит, поражение глаз (ирит, увеит). При БКр весьма часты аноректальные свищи (открывающиеся в эту область), межпетлевые или с другими органами, и абсцессы. У значительной части больных БКр первым симптомом болезни могут быть упорные трещины в области заднего прохода, околоректальные абсцессы и свищи. При БКр хирургические вмешательства часто малоэффективны вследствие высокой частоты рецидивов.
Частые осложнения БКр: сужения просвета кишки (стенозы), острая или хроническая кишечная непроходимость, перфорация (но редко, т.к. стенка кишки утолщается), абсцессы и перитонит. Редкие осложнения: кишечные кровотечения, токсическая дилатация кишки (но более редко, чем при НЯК). При БКр в 3 раза повышается вероятность развития рака кишечника.
Лабораторные данные при БКр малоспецифичны и отражают распространенность и тяжесть патологического процесса. В общем анализе крови отмечают: гипохромную анемию, лейкоцитоз, повышение СОЭ (более 30 мм/ч). В биохимическом анализе крови определяют: снижение альбуминов, рост а2 и j-глобулинов, снижение уровня калия, кальция, железа (при обширном поражении тонкого кишечника и упорных поносах). Ирригоскопия выявляет резкое сужение просвета терминального отдела повздошной кишки (по типу "натянутой струны" или "веревочки"), продольные язвы и свищи; псевдополипоз с изъязвлениями и мелкими дефектами наполнения придают вид "булыжной мостовой". Эндоскопия: афтозные эрозии и язвы (появляются рано), в нормальной или воспаленной слизистой; глубокие, продольные (вдоль оси кишки) трещины и язвы; сужение просвета кишки, сегментарность воспаления. Всем больным с хроническими поносами и ректальной кровоточивостью необходимо делать колоноскопию. Учитывая возможность поражения верхних отделов ЖКТ при БКр (в 15% случаев), показано проведение и фиброгастроскопии.
Критерии диагностики БКр:
· специфичные ¾ позитивные гистоморфологические данные (гранулеммы, гигантские клетки), полученные при операции или аутопсии;
· типичные (обнаружение сегментарного поражения кишечника при лапороскопии и воспалительно-деструктивного процесса или фистул при рентгеноскопии кишечника).
Длительность БКр составляет от полугода до 20 лет. Летальность колеблется от 5 до 15% и чаще обусловлена кровотечениями.
Дифференциальный диагноз ХВЗК:
1. Классические инфекции, вызывающие острый колит: сальмонелла, шигелла, йерсения, компилобактер, кишечная палочка, клостридиум. В анамнезе у этих больных отмечаются: поездки в развивающиеся страны; пользование водой из естественных источников; питание в кафе быстрого обслуживания, банкеты и пикники; прием морских продуктов, особенно в сыром виде;
2. Кишечные инфекции, передаваемые сексуально ("синдром кишки гомосексуалиста, проститутки") ¾ нейсерия гонорея, сифилис, простой герпес.
Для исключения пунктов 1 и 2 необходим анализ культуры стула.
3. Патология сосудов (ишемия, васкулит).
4. Рак кишечника.
5. Дивертикулярная болезнь кишечника.
6. Длительный прием лекарств.
Когда другие причины патологии кишечника исключены, проводится дифференциальный диагноз между НЯК и БКр. Конечная верификация делается эндоскопически (с гистологией) и с учетом данных ирригоскопии.
Лечение ХВЗК
Диета не играет существенной роли в подавления воспаления в кишечнике при ХВЗК (одной диетой вылечить ХВЗК нельзя). В целом при ХВЗК нет четких… При обострении ХВЗК больные не должны кушать "все", обычное питание… В тяжелых случаях (при неэффективности жидкой диеты, сохранении симптомов активности воспаления в верхних отделах…ГЛОМЕРУЛОНЕФРИТЫ
Подробно клинику гломерулонефритов (синоним: нефриты), как воспалительное поражение клубочков, описал в 1827 английский врач Брайт. Гломерулонефрит… ГН ¾ иммунно-воспалительное заболевание с преимущественным и начальным… Распространенность ГН. В практике врача ГН встречаются не так часто, как, например, ИБС или ХОЗЛ, но их медицинское и…Патогенез ОПГН
ОПГН ¾ классический пример иммунно-комплексного воспаления: АнГ (В-гемолитический стрептококк) поступает в кровь ® формируется иммунный… Иммунологическое повреждение при ОПГН можно разделить на 4 главных типа:… 1. Образование обычных антител. Комплекс АнГ-АТ может оседать на почечной мембране (так как она имеет богатую…Клиника ОПГН
По клиническому течению выделяют 4 формы ОПГН: · циклическая(развернутые симптомы); · затяжная ¾ постепенное развитие болезни; медленное нарастание отеков; мало выражены АГ и гематурия;…Рис. 8. Течение ОПГН
Прогноз ОПГНу взрослых менее благоприятен, чем у детей (так как у них более выражена острота болезни и почечная недостаточность). У половины взрослых болезнь медленно прогрессирует (рис. 8), возникают необратимые повреждения, функция почек ухудшается (сохраняется стойкая протенурия и/или гематурия), медленно прогрессирует гломерулосклероз и почечная недостаточность с АГ. Такая эволюция ОПГН более вероятна в случаях тяжело протекающего заболевания. Так, у лиц, вроде бы уже выздоровевших от ОПГН (полностью или частично), впоследствии (даже спустя 20-30 лет после перенесенного ОПГН) могут развиться: протеинурия, АГ и ХПН. Такое развитие болезни связано со склерозом клубочков и сосудов (по данным биопсии) и отражает последствия внутриклубочковой гипертонии. Так, при ОПГН часть клубочков повреждается необратимо, но при этом КФ вначале сохраняется в норме за счет гиперфильтрации в непораженных клубочках. Эта защитная реакция и способствует последующему повреждению стенки капилляров клубочка.
Таким образом, ОПГН ¾ потенциально прогрессирующее заболевание у взрослых (менее, чем в 50% случаев). Поэтому больные, перенесшие ОПГН, должны наблюдаться на диспансерном учете (постоянный контроль за АД, протеинурией и функцией почек). Первые 6 месяцев эти больные осматриваются каждый месяц, а позднее ¾ 1 раз в 3 месяца. При нормальных клинико-лабораторных тестах больной через 2 года может сниматься с диспансерного учета.
Хронический гломерулонефрит(ХГН) (медленно-прогрессирующий). ХГН ¾ это большая группа морфологически разнородных, длительно текущих, двухсторонних иммунно-воспалительных заболеваний преимущественно клубочкового аппарата почек (но также канальцев и интерстициальной ткани). В основе ХГН лежат близкие по характеру механизмы развития и патоморфологические изменения, приводящие к:
· стойким нарушениям состава мочи (протеинурии и/или гематурии);
· склерозированию (сморщиванию) паренхимы почек с постепенной, но неуклонной гибелью нефронов;
· развитию АГ;
· постепенному (в течение нескольких лет), но необратимому снижению функции (скорости КФ) с выходом на терминальную ХПН (со снижением числа нефронов менее 10% от нормы).
Этиология ХГН ¾ чаще идиопатическая (ее устанавливают только у 10% больных):
1. Инфекция:у трети больных ХГН ¾ следствие плохо леченного ОПГН (либо недиагностированного). Так, у части больных ХГН в анамнезе был ОПГН. Инфекция может быть как бактериальная (чаще b-гемолитический стрептококк группы А), так и вирусная (вирусы гриппа, гепатита В и С, Эпстайн-Бара).
2. Ятрогенные факторы ¾ принимаемые долгое время лекарства: пенициллины; соли золота, лития, ртути; анальгин и фенацетин. Лекарства могут "запустить" новый патологический процесс с поражением почек. В целом АБ и анальгетики чаще приводят к развитию острого или хронического тубуло-интерстициального нефрита.
· Опухоли. АнГ опухоли являются провоцирующим фактором развития ХГН (паранеопластический синдром). ХГН-болезнь иммунного ответа. Например, ХГН нередко развивается при бронхогенном раке, раке почки или лимфогранулематозе. Так, если ХГН появился после 50 лет, то следует искать "где-то" рак. Часто удаление опухоли приводит к обратному развитию ХГН.
· ДБСТ:СКВ (люпус-нефрит), системная склеродермия, УПА, геморрагический васкулит.
· Сывороточная болезнь(ХГН нередко возникает после повторного введения вакцин или сывороток).
· Простуда и переохлаждения(простудный нефрит).
· Воздействие органических растворителей (свинец, кадмий, бензол, анилиновые краски. Долго красил пол и окна, а позднее развился ХГН).
Таким образом, этиология ХГН может быть разной, но клиническая симптоматика достаточно стандартна (протеинурия, гематурия, остронефритический синдром или НС, АГ и ХПН, в том числе и быстро прогрессирующая).
Патогенез ХГН.ХГН чаще развивается как первично хроническое заболевание и значительно реже является исходом ОПГН. В основе ХГН лежат иммунопатологические механизмы (образуются ИК к БМ), а из неиммунных факторов большая роль принадлежит внутрисосудистому свертыванию крови (гиперкоагуляция + нарушения фибринолиза). Морфологически в области БМ находят отложения ИК, состоящие из иммуноглобулина и комплемента. Они образуются в крови или непосредственно в почечной ткани ИК (АнГ + АТ). Отложение ИК комплексов на БМ клубочков с фиксацией на них комплемента (С3) является иммунокомплексным механизмом развития ХГН. БМ сосудов, эндотелия и эпителия почечных клубочков повреждается ИК и/или аутоантителами. Характер иммунных отложений может быть различным: если их много и отложения грубые, то возникает тяжелое поражение БМ. Иногда может меняться белковый состав самой БМ.
Развиваются: хроническое продуктивное воспаление в почечных клубочках как интра- так и экстракапиллярно (в капсуле Шумлянского-Боумена), склерозирование клубочков и гибель нефронов.
По сути, ХГН ¾ токсикоаллергическое заболевание, которое на 80% связано с иммунными механизмами. ГН - это проявление индивидуальной реакции (сверхчувствительности), которая в ряде случаев имеет генетические предпосылки.
Под действием этиологического неспецифического фактора происходит бурная аллергическая реакция соединения АнГ+АТ (Ig M,G) с образованием ИК и присоединением к ним активированного комплемента (рис.9). ИК могут быть как свободно циркулирующие (ЦИК), так и фиксированные на БМ клубочков. В ответ на иммунные нарушения в почечных клубочках развиваются различные изменения, проходящие ряд стадий. При пассивном заносе ЦИК в клубочки или образовании иммунных депозитивов (ИК) в почках запускается цепь воспалительных реакций: повышается хемотаксис ПЯЛ, активируются медиаторы тканевого воспаления и повреждения, внутрисосудистое свертывание крови (нарушения гемостаза в патогенезе ХГН являются связующим звеном между иммунитетом и воспалением), формируются белые и красные тромбы в микроциркуляции и депозиты фибрина в стенке капилляров клубочков и их тромбирование. Активное образование и выброс цитокинов сопровождаются ответной реакцией со стороны гломерулярных клеток. В результате их взаимодействия с этими медиаторами возникает выраженная клеточная пролиферация с выделением активных радикалов и ферментов, накоплением и расширением мезангиального матрикса, что способствует нарушениям функции почек и склеротическим изменениям.
Это способствует нарушению структуры и функциональной целостности клубочковых капилляров (нарушается мезангиальный матрикс), что приводит к развитию иммунного воспаления клубочков и БМ с последующим нарушением фильтрации (повышается селективная проницаемость для белков плазмы крови и стимулируется миграция эритроцитов и лейкоцитов из внутрисосудистого пространства). Дистрофия нефрона приводит к фиброзу канальцев интерстиция с последующим склерозированием клубочков и гибелью нефрона (выключению из функционирования).
Таким образом, на генетическую предрасположенность накладывается воздействие АнГ (экзо- или эндогенного), а далее формируется обычная иммунная реакция с образованием ИК. Последние запускают нарушения микроциркуляции. В дальнейшем прогрессировании ХГН важную роль приобретают медиаторы воспаления, неиммунные механизмы и механизмы самопрогрессирования, постепенно ведущие к склерозу многих нефронов. Из механизмов самопрогресирования можно выделить две группы:
· иммунно-воспалительные ¾ образование АТ к БМ клубочков (и фиксацией АТ к БМ), с последующим повреждением БМ и образование ЦИК, откладывающихся на БМ и повреждающих ее. Персистирование и хронизация иммунного механизма обусловлены персистированием этиологического фактора, снижением местного фагоцитоза и неадекватным иммунным ответом. Персистирование иммунных механизмов приводит и к нарушениям в системе микроциркуляции.
· неиммунные:
1. Повреждение канальцев при длительной протеиурии.
2. По мере прогрессирования поражения почек функцию выпавших склерозированных нефронов берут на себя оставшиеся нормальные нефроны. При этом в сохранившихся нефронах повышается клубочковая фильтрация (вследствие роста внутриклубочкового давления из-за потери массы функционирующей фильтрующей поверхности), что повреждает клубочек и ведет к его склерозированию (гломерулосклероз) и интерстициальному фиброзу. Последние определяют скорость появления ХПН у больного с ХГН.
3. Повышение АД ухудшает функцию сохранившихся клубочков, что также способствует их склерозированию.
В итоге нарастают гломерулосклероз и интерстициальный фиброз, которые и определяют приближение ХПН, но ее темпы нарастания различные у разных больных ХГН.
 |
Рис. 9. Схема патогенеза ХГН.
Таким образом, на всех этапах ХГН ведущую роль играет персистирование этиологического фактора, правда, известного лишь у 1 из 10 больных. Имеется точка зрения, что развитие у больного ОГН или ХГН зависит в частности и от:
1. Количества бактериальных АнГ, попавших в кровь.
2. Степени и продолжительности фиксирования АнГ в почечной ткани.
3. Количества АТ, образовавшихся в организме.
Так, однократное (или незначительное) попадание АнГ в кровь при интенсивном образовании АТ формирует ОГН. Тогда как повторяющиеся попадания АнГ в организм на фоне слабого образования АТ вызывают развитие ХГН.
Патоморфология ХГН:
· макроскопически: почки уменьшены в размере, ткань уплотнена (вследствие гибели паренхимы ¾ почечных нефронов). В терминальной стадии ХПН развивается вторично-сморщенная почка ("нефритическая").
· микроскопически ¾ картина хронического склерозирующего ГН: гиалиноз, фокальная или диффузная пролиферация клеток мезангия, сегментарные или глобальные повреждения клубочков (их запустевание); атрофия канальцев; интерстициальный фиброз; сужение просвета артерий, приводящее к прогрессивному снижению почечного кровотока и вторичное запустевание лимфатических сосудов.
Классификация ХГН
· первично-хронический (инфекционный и неинфекционный) ¾ бывает чаще (в 80%). Возникает без видимых предшествующих заболеваний (например, в анамнезе нет указаний на ОПГН). Начало болезни незаметное, скрытое. Иногда может "идти" как скрыто протекающий ОПГН. Переход ОГН в ХГН протекает по-разному, у 20% больных ХГН ¾ результат перенесенного ранее ОПГН. У одних больных симптоматика ОПГН полностью не исчезает (сохраняются микроскопическая гематурия и слабая протенурия; уровень креатинина и АД в норме), а постепенно оформляется в картину ХГН (например, через несколько лет начинает появляться АГ и заметная протеинурия на фоне нормальных значений креатинина). Тогда как у других больных симптомы ОПГН исчезают на много лет (латентный период), и потом появляется клиника ХГН. Результаты исследований сильно разнятся и зависят от тяжести болезни.
· вторично-хронический ¾ как следствие перенесенного ранее ОГН или возникший на фоне СКВ, УПА, ИЭ др.
Клиника и морфология этих двух форм ХГН идентичные.
Клиника ХГН
Клинические формы ХГН (Тареев, 1958) 1. Латентная(нефрит с изолированным мочевым синдромом) ¾ самая частая… 2. Нефротическая (НС) встречается в 20% случаев. В большинстве случаев чистого НС (без нефритического синдрома) в…Нефармакологическая терапия ХГН
При сохранении функции почек больным нужна полноценная диета. Но при появлении выраженной клиники (НС, АГ, изменений мочевого осадка), длительное… Обязательны выявление и воздействие на очаги инфекции: радикальное лечение…Фармакологическая терапия ХГН
 |
Учитывая, что патогенез ХГН складывается из трех этапов (иммунный, воспаление и гиперкоагуляция), то и лечение должно влиять на: иммунное звено (ГКС и цитостатики); гиперкоагуляцию (антиагреганты и антикоагулянты); воспаление (НПВС ¾ аспирин, индометацин).
Рис. 10. Патогенетическая терапия ХГН
Для подавления активности ХГН используют три группы лекарств: ГКС, цитостатики и циклоспорин А. Имуннодепрессанты ¾ основное средство патогенетической терапии ХГН, так как повреждение клубочков инициируется образованием АТ и отложением ИК в БМ клубочков. Применение ГКС патогенетически обосновано, так как они обладают противовоспалительным и иммунносупрессивным действием (снижают выработку АТ, лейкотриенов и порозность капилляров). Все это способствует повышению диуреза, снижению отеков и мочевого синдрома (цилиндурии, протеинурии), а также гиперхолестеринемии. Но, как показывает практика, ГКС эффективны лишь у половины больных ХГН. Эффективность ГКС снижается по мере удлинения стажа ХГН. Так, если длительность ХГН составляет более 5 лет, то эффективность ГКС ¾ низкая. В целом, показания к назначению ГКС в основном морфологические, а не клинические. Например, впервые возникший НС с высокой протеинурией, без АГ и гематурии, СКВ-нефрит, БПГН, латентный ХГН в фазе обострения.
Лучше использовать преднизолон (или метилпреднизолон) длительно, по усредненной схеме: в суточной дозе 60 мг/д (или 1 мг/кг веса) в течение 3 недель. Затем постепенно дозу снижают на 5 мг в течение 4 дней (с 60 до 40 мг), позднее ¾ еще более медленно, по 1/2 таб в 3 дня, в течение 8 недель. Оставляют минимально поддерживающую дозу (10 мг/д) на протяжении 6 месяцев. Можно использовать и альтернативную схему приема ГКС (через день), при которой меньше угнетается кора надпочечников.
Могут быть три варианта отмены ГКС:
· ГКС не помогают (через 3 недели приема нет эффекта).
· ГКС дают большой положительный эффект (исчезли НС, протеинурия). В этих случаях лучше полностью отменить ГКС. Далее проводят лечение другими поддерживающими средствами.
· ГКС помогли, но недостаточно (исчезли отеки, нормализовался белковый спектр крови, но мочевой синдром сохранился). В этом случае переходят на поддерживающие дозы ГКС (10-20 мг/д в течение полугода и более).
При высокой активности ХГН или БПГН используют пульс-терапию, быстро достигая высоких уровней ГКС: в/в капельно вводят 1000 - 3000 мгт преднизолона 3 дня подряд (суммарная доза 3-9 г). Потом назначают 40 мг преднизолона орально.
Обычно ГКС используют при:
· мезангиопролиферативном ХГН (где минимальные изменения клубочков);
· в меньшей степени при мембранозном ХГН (где мало выражено склерозивание почечной ткани).
Лечение ГКС мало эффективно при MPGN и FSG, так как при этих формах преобладает пролиферация в клубочках. Основной недостаток ГКС ¾ это гормонозависимость, возникающая тогда, когда ГКС дают длительно и в малой дозе (при этом повышается и риск развития осложнений). Поэтому ГКС следует давать больному в оптимальной дозе, но как можно кратковременнее, тогда ГКС-зависимость не разовьется.
ГКС противопоказаны при:
· ХПН, амилоидозе, диабетическом нефроангиосклерозе;
· наличии осложнений (ЯБ, АГ);
· паранеопластической нефропатии.
Цитостатики (Ц) используются реже, чем ГКС, вследствие большей тяжести побочных эффектов. Ц подавляют реакцию АГ - АТ и конечные иммунные реакции, уменьшают клеточную пролиферацию, миграцию нейтрофилов и лимфоцитов.
Показания для применения Ц (практически те же, что и для ГКС): активные формы ХГН, НС в комбинации с АГ, ГКС-резистентные формы ХГН или ГКС-зависимый НС, наличие противопоказаний к приему ГКС или развитие осложнений ГКС-терапии.
Из Ц лучше использовать:
· азотиоприм (имуран) в суточной дозе 100-200 мг (1,5-3 мг/кг/д). Недостатки азотиоприма: слабый противовоспалительный эффект и подавление костного мозга (лейкопения). Так, если число лейкоцитов становится менее 4×109/л, то доза препарата снижается в 2 раза.
· циклофосфамид (циклофосфан) назначают чаще, обычно в суточной дозе 200 мг (2мг/кг). Недостатками препарата являются: угнетение всех активно-пролиферирующих клеток (кроветворные, гонады) с последующим развитием лейкопении, тромбоцитопении; увеличение подверженности инфекциям (легочной, урологической) или обострение латентной инфекции, ТВС Ц назначают по 200 мг в течение 5 недель, потом дозу снижают до 100 мг (дают еще 5 недель). Через 10 недель лечения дозу снижают до 50 мг и ее дают еще 8 месяцев. Одно из условий эффективности Ц ¾ длительность лечения. Дозу циклофосфамида подбирают индивидуально, добиваясь снижения числа лейкоцитов (до 3,5×109/л, но не ниже 3,0×109/л). Необходим контроль уровня лейкоцитов, нейтрофилов, тромбоцитов в крови каждые 2-3 дня. При снижении числа лейкоцитов менее 3*109/л и росте печеночных ферментов лечение Ц прекращается. Если число лейкоцитов не снижается, то препарат не эффективен.
При высокой активности ХГН, быстром росте уровня сывороточного креатинина (особенно у лиц с быстро нарастающей ХПН) проводят пульс-терапию циклофосфамидом (в/в в дозе 10-20 мг/кг массы тела, 1 раз в месяц, в течение 6 месяцев), на 14 день необходим контроль уровня лейкоцитов. В ряде случаев это позволяет выйти на ремиссию ХГН и избежать серьезных осложнений. Лучший эффект Ц получен при MN, где ГКС мало эффективны.
Противопоказаниями к приему Ц: терминальная стадия ХПН, сопутствующая инфекция, лейкопения, амилоидоз, повышенная чувствительность к Ц.
При патологии, требующей быстрого положительного эффекта, прибегают к комбинации Ц+ГКС (так, эта комбинация повышает успех лечения ХГН с НС до 70%). Здесь введение ГКС ценно, так как они начинают действовать уже через 12-72 ч, а Ц ¾ только через 2-3 недели. Если эффект от приема ГКС+Ц мал (или его нет), используют плазмоферез (удаляются нефротоксические ЦИК, воспалительные медиаторы, активированные факторы комплемента и свертывания). В большинстве случаев сочетание повышенного уровня креатинина в крови (более 5 мг/%) со снижением размеров почек делают лечение ГКС и Ц бесперспективным.
Антиагреганты(курантил и трентал) и антикоагулянты(гепарин) тормозят прогрессирование ХГН путем воздействия на процессы локальной внутрисосудистой и внутриклубочковой коагуляции (улучшается микроциркуляция). Так, гепарин дополнительно снижает протеинурию и пролиферацию мезенгиальных клеток, оказывает слабое иммуносупрессивное и противовоспалительное действие. Гепарин показан при обострении любых клинических и морфологических форм ХГН. Гепарин обычно применяют в сочетании с антиагрегантами, вводят по 10000 ед. п/к утром и вечером. Потом дозу уменьшают до 5000 ед/д и дают несколько месяцев.
Иногда, через 5-6 недель гепарин заменяют фенилином (так, чтобы ПИ был на уровне 50%). В ряде случаев гепарин вводят сразу в/в, капельно в дозе 1 мг/кг массы тела, каждые 6 ч, а потом его вводят п/к. Доза гепарина считается адекватной, если через 5 часов после п/к введения время свертывания увеличилось в 2 раза. Применение гепарина противопоказано при: склонности к кровотечениям (кроме ДВС-синдрома), снижении КФ менее 30 мл/мин (при норме ¾ 120 мл/мин).
Курантил (дипиридамол) усиливает перфузию ишемизированных клубочков, умеренно снижает протеинурию.и гематурию. Курантил также показан при всех формах ХГН. Его назначают как в виде монотерапии, так и в комбинации с гепарином и аспирином в больших дозах (400-600 мг/д, 5-10 мг/кг веса) и длительно, не менее года. Показания к назначению трентала(0,3 г/д)те же, что и для курантила.
Нередко комбинируют курантил с аспирином, что потенциирует антиромботический эффект друг друга и увеличивает "время жизни" почек до наступления терминальной ХПН.
Для лечения тяжелых форм ХГН (БПГН) используют четырехкомпонентную комбинацию: азотиаприм (2 мг/кг/д)+гепарин (20000-40000 ед/д)+курантил (10 мг/кг)+ГКС (30-40 мг/д).
НПВС(салицилаты, индометацин, ибупрофен) тормозят миграцию лейкоцитов, меняют синтез простогландинов (тем самым уменьшается воспаление). В настоящее время имеется точка зрения, что НПВС не влияют на суть патологии при ХГН. НПВС показаны при: латентном ХГН (когда нет показаний к активной терапии, а необходимо лишь снизить протеинурию) и умеренной активности ХГН. Обычно назначают индометацин (по 100-150 мг/д) длительно (годы). По мере увеличения диуреза и снижения отеков, дозу НПВС уменьшают, но при отсутствии положительного эффекта опять повышают. Комбинации аспирин+курантил и варфарин+курантил эффективны только при MPGN.
Лечение морфологических вариантов ХГН:
· мембранозная нефропатия (MN) имеет благоприятное течение, ХПН формируется редко. Поэтому активную терапию (например, больных с небольшой протеинурией) можно не проводить. Но при стойкой протеинурии больному назначают: ГКС (преднизолон в больших дозах ¾ 2 мг/кг/д, в течение 6 месяцев) или циклофосфамид (0,2-0,5 мг/кг/д, в течение 1 месяца; потом на 1 месяц делают перерыв). Иногда комбинируют ГКС и Ц.
· мезангио-пролиферативный (MPGN). При этом варианте нет эффекта от ГКС и Ц (они даже повышают АД), поэтому больным длительно, годами назначают курантил+аспирин (1 г/д), которые замедляют падение КФ. На поздних этапах этой формы ХГН показаны гемодиализ и пересадка почек.
· минимальные изменения клубочков (MCD). Здесь ГКС ¾ средство выбора (курс 8 недель). У 95% больных этим достигается ремиссия (исчезают отеки и протеинурия): у 70% в течение 2 недель, у 90% ¾ в течение 1 месяца. Если нет эффекта от ГКС, назначают Ц.
· фокальный гломерулосклероз (FSG) ¾ это наиболее резистентная к лечению форма ХГН. Проводят симптоматическое лечение: короткие курсы ГКС, ИАПФ (для контроля АД) и коррекцию липидного обмена (соответствующей диетой).
· БПГН требует раннего (до того как развились тяжелые поражения клубочков) и активного лечения по 4-х компонентной схеме (Ц + ГКС + курантил + гепарин). По сути БПГН - это неотложное состояние, и успех лечения зависит от максимально раннего начала лечения и адекватной, большой дозы лекарств. При неэффективности 4-х компонентной схемы проводят плазмоферез и гемодиализ. При развитии анурии проводимое лечение неэффективно.
Если не определен морфологический вариант ХГН, проводят по-синдромную терапию отдельных проявлений ХГН.
Особенности лечения клинических вариантов ХГН
· латентный¾ лучше обойтись без лекарств, так как неизвестна реакция почек на лекарства. Иногда назначают курантил и индометацин.
· гипертонический ¾ также редко требует активной терапии. ГКС и НПВС противопоказаны. Ограничивают прием соли и назначают гипотензивные средства (эналаприл, верапамил, атенолол) для снижения АД диастолического до уровня менее 95 мм рт. ст. (ибо АГ усиливает прогрессирование ХГН), курантил и трентал. Важно плавно (во избежание ухудшения кровотока в почках), но до нормы, снижать АД, так как АГ ведет к прогрессированию ХГН. При АД систолическом более 180 и АД диастолическом более 120 мм.рт.ст. назначают комбинацию гипотензивных средств (ИАПФ ¾ эналаприл, рамиприл, лазортан) плюс салуретиков (гипотиазид, бринальдикс, фуросемид до 200 мг/д). При выраженной активности (НС+АГ) применяют Ц (в ряде случаев гепарин+курантил) несколько месяцев на фоне гипотензивной терапии. Иногда АГ ¾ следствие лечебного приема ГКС. Контроль АГ предотвращает быстрое развитие ХПН (потери функции почек) и острые осложнения АГ (судороги, энцефалопатию, ОЛЖН) у больного.
· Смешанный¾ необходимы: ограничение соли, жидкости, прием гипотензивных средств и салуретиков. Причем, при больших отеках (если скорость КФ изменена мало) начинают с тиазидовых мочегонных (гипотиазид), а при их малой эффективности назначают петлевые диуретики в постепенно возрастающих, дробных дозах (фуросемид от 40 мг до 600 мг/д). При больших отеках (НС), но при отсутствии признаков ХПН, назначают комбинацию мочегонных: салуретики (гипотиазид)+калий-сберегающие диуретики (верошпирон). У больных ХГН салуретики обладают меньшим эффектом, чем при ХНК. При высокой активности процесса комбинируют Ц+гепарин+курантил. Больному можно давать фрукты и овощи, где много калия (абрикосы, персики, сливы, картофель, помидоры, свекла, орехи). ИАПФ снижают потери белка с мочой за счет снижения давления внутриклубочкового и задержки жидкости. При выраженной ХПН салуретики противопоказаны вследствие возможного развития гипокалиемии и гипонатриемии.
· Гематурический ¾ не требует лечения (не поддается ему).
При анемии, если она выражена (Нв менее 70 г/л), переливают эритроцитарную массу. Назначают также тестостерон (в/м 300мг 1 раз неделю в течение 3-6 месяцев), рекомбинантный эритропоэтин (в дозе 720 ед. в неделю), реокорм (п/к в начальной дозе 20 МЕ/кг 3 раза в неделю).
При электролитных нарушениях: гипонатриемии ¾ дают внутрь хлористый натрий или в/в физиологический раствор; гипернатриемии ¾ проводят гемодиализ; гипокалиемии ¾ назначают соли калия внутрь или в/в.
Критерии эффективности леченияХГН:
· полная ремиссия ¾нормализация АД, уровня белка в крови и холестерина; отсутствие отеков, протеинурии, гематурии;
· частичная ремиссия¾ стойкое снижение АД, протеинурии (более, чем в 10 раз), гематурии и холестерина.
· отсутствие эффекта¾ все показатели сохраняются на исходном уровне.
· процент больных с 5-й и 10-й выживаемостью.
Физиотерапевтическое лечение(диатермия, УВЧ на область почек и др.) назначают после оценки функции почек.
Санаторно-курортное лечение: поездка в Крым, в Байрам-Али (или другие сухие, жаркие курорты), но при АГ менее 160/100. Оттуда надо возвращаться в теплое время, так как возвращение в холодное время приводит к повторному обострению.
ВТЭопределяется видом работы, состоянием болезни и наличием ХПН. Так, больные с ХГН (без нарушения функций почек и сердца) могут работать, если работа не связана с высокой ФН или постоянным контактом с холодом и сыростью. Но если у больного появляется ХПН, ему назначают 3 группу инвалидности. При простудных заболеваниях (грипп, ОРЗ) больной должен адекватно выдерживаться на больничном листе, и перед его закрытием необходимо делать повторные анализы мочи.
Продолжительность жизни больных ХГН колеблется в широком диапазоне. Прогрессирование ХГН пропорционально выраженности протеинурии. Такие симптомы, как снижение удельного веса мочи и задержка азотистых шлаков свидетельствуют о необратимости поражения почек. Оценка прогноза ХГН во многом связана с этиологией болезни и тем, является ли ХГН первичным или вторичным. Правильная тактика лечения ХГН улучшает прогноз болезни и на многие годы отдаляет терминальную ХПН.
ХРОНИЧЕСКИЙ ПИЕЛОНЕФРИТ И ХРОНИЧЕСКАЯ ПОЧЕЧНАЯ НЕДОСТАТОЧНОСТЬ
В истоках ХП лежит возвратная или персистирующая инвазия лоханки, чашечек и форникального аппарата почки, связанная с местным действием… Выделяют первичный и вторичный ХП: · первичный(необструктивный) развивается у лиц с не измененными мочевыми путями, без предшествующего урологического…Рис. 11. Схема патогенеза хронического пиелонефрита.
У женщин уропатогены способны мигрировать из прямой кишки во влагалище, способствуя колонизации уретры и мочевого пузыря, с последующим достижением инфекции почечной ткани. Кроме того, большая часть женщин с частыми обострениями ХП имеет колонизацию промежности кишечной палочкой. Особо вирулентные микробы (плазмокоагулирующие виды стафилококка) могут фиксироваться и размножаться в ткани почек без дополнительных благоприятных условий. Кроме того, эндотоксический эффект, вызывающий снижение перистальтики гладких мышц мочевых путей, приводит к нарушению уродинамики, формированию лоханочно-почечного рефлюкса и облегчает продвижение бактерий вверх по стенке мочеточника, в почку.
Генетические дефекты у больных ХП проявляются большей плотностью рецепторов слизистой мочевых путей к условно-патогенной флоре ("сожителям").
Для реализации ХП нужен и "второй удар" (неспецифические механизмы), то есть нарушение уродинамики или снижение резистентности макроорганизма. ХП ¾ это болезнь, сочетающая нарушение уродинамики (рефлюксная нефропатия) и инфекцию. Последняя ¾ пусковой фактор иммунного ответа. При нарушении уродинамики появляется застой мочи в лоханке. В ней в нормальных условиях давление низкое, и за счет этого моча "вытягивается" из почечной ткани. Повышение давления в лоханке приводит к нарушению этого процесса. На фоне имеющихся выраженных рефлюксов инфицированная моча (содержащая ИК, в составе которых в роли АнГ выступает инфекция) идет из лоханки обратно в венозное русло почечной ткани. Заброс ИК в сосочковую зону благоприятствует воспалительной реакции в почках. Таким образом, воспалительный процесс иммунной природы начинается в мочевыводящих путях, а позднее переходит на почечную ткань.
Обычно у больного с ХП имеется комбинация общих и местных предрасполагающих факторов. Как правило, интермитирующая инфекция мочевых путей (с началом во взрослые годы), приводит позднее к ХПН, даже в отсутствие обструкции мочевых путей, СД и рефлюксов. Наличие бактериурии, даже в бессимптомной форме, заметно повышает летальность от ХП.
Патанатомия ХП. На секции у каждого десятого умершего (у пожилых ¾ у каждого пятого) выявляется ХП, так как при жизни он часто не распознается. При ХП главные изменения находят в интерстиции: формируется склероз и рубцевание клубочков (вследствие неспецифического нарушения оттока первичной мочи из них), со временем склерозируется вся паренхима почки ("пиелонефритически сморщенная" почка). Идет сочетание патологических процессов различного возраста: от инфильтрации до полного склероза, в связи этим функциональные способности почек ограничиваются. При ХП поражается не только мозговой слой почки (сосочки и интерстиций), но и сосуды клубочков, хотя они долгое время и остаются интактными. Обычно ХП ¾ двухстороннее, но асимметричное поражение почек. В 20% случаев ХП остается до конца односторонним заболеванием (чаще правой почки).
Выделяют три последовательных морфологических стадии ХП:
1. Развитие очаговых интерстициальных инфильтратов и атрофия канальцев, но клубочки интактны.
2. Склероз интерстициальных инфильтратов, атрофия канальцев плюс поражения клубочков и сосудов.
3. Сморщенная почка на "финише" болезни. Макроскопически она уменьшена в размерах, с крупными рубцами на поверхности, ЧЛС деформирована, имеется атрофия и замещения соединительной тканью канальцев. Паренхима почки резко истончена, а в финале болезни почка имеет лишь "тонкую стенку".
Клиника ХП многообразная (ХП ¾ "хамелеон") и зависит от распространенности и локализации процесса, от его природы, стадии и активности инфекции, а также от наличия сопутствующих заболеваний. Так, нередко при поражении одной почки, часто вплоть до ее сморщивания, ХП не проявляется клинически. Как правило, ХП является следствием ранее перенесенного острого пиелонефрита. Вне обострения клиника ХП весьма скудная. Лишь целенаправленный опрос больных помогает выявить характерные симптомы ХП: неприятные ощущения (боли) в пояснице, эпизоды немотивированного субфебрилитета и познабливаний, нарушения мочеотделения (поллакиурия, никтурия) и мочеиспускания (дизурия).
При ХП выделяют 4 почечных (мочевой, болевой, поллакиурический, интоксикационный) и 2 внепочечных синдрома (АГ, анемический).
Мочевой синдромчасто бывает изолированным. В анализах мочи выявляют: лейкоциты обычно 4-8/1 (их количество указывает на выраженность обострения), которые "уходят" в мочу из интерстиция почек и воспалительной слизистой мочевых путей. Только повторные исследования мочи дают представление об истинной лейкоцитурии, которая не постоянна и может исчезать. Лейкоцитуриябывает следующей: 0-5/1 ¾ латентная (в 25% случаев), 5-10/1 (в 40%) и более 10/1 (в 25% случаев). Лейкоцитурия может быть почечной (преобладают лимфоциты) вследствие ХГН, НС или амилоидоза почек или внепочечной (доминируют нейтрофилы), из-за наличия ХП, цистита, уретрита и простатита.
Эритроцитурия при ХП чаще развивается вследствие капилляро-канальциевого блока и разрыва канальцев капилляров и реже ¾ из-за форникальных кровотечений в области сосочков или наличия МКБ. Как правило, эритроцитурия более или менее постоянна, ее вариации следующие: 0-5/1 (в 20% случаев), 5-10/1 (в половине случаев) и более 10/1 (в 25%). У 10% больных ХП отмечается макрогематурия.
Цилиндурия при ХП встречается редко. Вследствие выраженной изменчивости осадок мочи следует исследовать многократно и лучше по Адис-Каковскому (информативность пробы Ничепоренко мала).
При обострении ХП осадок мочи может приобретать количественные и качественные свойства, характерные для острого пиелонефрита. На далеко зашедших стадиях ХП мочевой осадок становится скудным.
Оценка плотности мочи (проба Зимницкого) весьма информативна, особенно в фазу обострения. Снижение удельного веса мочи (гипостенурия) ¾ серьезный симптом, указывающий на поражение почечной ткани и снижение концентрации мочи. На поздних стадиях ХП появляется изостенурия (постоянно низкий удельный вес мочи). Нередко, на протяжении многих лет, при ХП отмечается только снижение удельного веса мочи (особенно при проведении пробы с сухоядением), а лейкоциты и эритроциты не выявляются.
Может определяться и умеренная протеинурия (до 1 г/д). Обычно при латентном ХП у 75% больных в сутки теряется до 1 г белка, тогда как при рецидивирующей форме ХП эти потери выше (2-3 г/д).
Бактериурияв моче также часто встречается при ХП. Причем, однократные исследования на бактериурию мало информативны. Ее лучше оценивать в разных ситуациях (переутомление, провокации и др.), тогда бактериурия выявляется у половины больных. Как правило, после двух-трех дней лечения АБ моча становится стерильной. Анализ мочи следует проводить сразу вследствие того, что АБ выделяются также с мочой и действуют в той емкости, где хранится моча.
В период обострения ХП характерныполлакиурия(частое мочеиспускание) и полиурия,когдаобъем выделяемой мочи превышает 2-3 л/д (что больше, чем у здорового).Последнее обусловлено снижением удельного веса мочи. Полиурия обнаруживается весьма рано и длится весь период болезни. Раз больной много выделяет мочи, то потребность в приеме жидкости увеличивается (появляется жажда). На стадии ХПН обычно развивается олигоурия - предвестник уремии. При ХП нередко встречается дизурия(частое и болезненное мочеиспускание), и чувство жжения в конце акта мочеиспускания, обусловленные повышением чувствительности рецепторов, заложенных в слизистой мочевого пузыря.
В БАК рано определяют снижение альбуминов, повышение a1 a2-глобулинов и уровня мочевины (в 80% случаев). Последний, по мере прогрессирования ХП, становится постоянно высоким. Весьма редко ХП долго протекает с нормальным уровнем мочевины.
Болевой синдром.При ХП больные часто жалуются на постоянные, тупые неприятные ощущения (боли) в пояснице (чаще двухсторонние вследствие растяжения лоханок) или ощущение "холода" в пояснице (поэтому ее часто укутывают). У половины больных могут быть боли по типу почечных колик.
Интоксикационный синдром проявляется:
· познабливаниями (они не всегда адекватны повышению температуры);
· частой субфебрильной лихорадкой при малой активности процесса (нередко в период обострения ХП у больных нет лихорадки);
· лейкоцитозом и повышением СОЭ в период обострения. У ряда больных ХП после перенесенного ОРВИ долго держится высокая СОЭ;
· общей слабостью (инфекционной астенией), ощущением разбитости, повышенной утомляемостью и снижением работоспособности. Эти неспецифические симптомы встречаются у 80% больных ХП. Реже отмечается диспепсическая симптоматика (снижение аппетита, тошнота).
Долгое время ХП может протекать лишь с отдельными фрагментами почечной патологии (например, с изолированным мочевым синдромом).
Из внепочечных синдромов нередко (у 40% больных) выявляется АГ с частой сопутствующей головной болью (реже она связана с интоксикацией). Причем, у каждого третьего больного ХП имеется комбинация ХП и ГБ. Другой синдром ¾ гипохромная анемия (у 5% больных), обусловленная интоксикацией. Эта анемия часто возникает при отсутствии признаков ХПН и плохо лечится.
Клиника ХП.
Со временем, под влиянием внешних факторов, ХП начинает проявляться клинически. Может появиться немотивированная АГ, вначале транзиторная, а позднее… У большей части больных с латентной формой ХП при целенаправленном… При объективном обследовании могут определяться некоторая пастозность век по утрам или лица, их бледность (отеков нет,…Прогноз и исходы ХП.
Через 10 лет рецидивирующего течения ХП нормальная функция почек определялась только у 20% больных, у 35% снижался удельный вес мочи, а у 45% лиц… Исходы ХП: смерть от уремии вследствие ХПН, развивающейся медленно и… Обычно вначале ХП периоды ремиссий могут быть длительными, что может ложно напоминать выздоровление. Со временем,…Применение АБ в зависимости от вида микроба
Важное значение имеет рН мочи, в которой АБ действует. Так, ряд АБ сохраняет свою активность в узком диапазоне рН мочи. Ампициллин максимально… Кроме того, надо учитывать антагонизм (например, тетрациклинов с… Для эмпирического лечения (внутрь) периодических обострений ХП используются следующие режимы:Рис. 12. Алгоритм лечения АБ обострения хронического пиелонефрита.
Если эффект от АБ незначителен, то добавляют неспецифическую стимулирующую терапию (продигиозан, пирогенал, пентоксил) и препараты, улучшающие почечный кровоток (трентал, курантил, гепарин). Диуретики не используют в лечении ХП из-за спонтанной полиурии и реальной возможности водно-электролитных нарушений. Проводят также симптоматическую терапию АГ (ИАПФ) и анемии (железосодержащие препараты, витамин В12, эритропоэтин). Назначают физиотерапевтические процедуры (вне обострения).
После ликвидации обострения ХП больной в течение первого года находится на диспансерном учете и получает многомесячное противорецидивное лечение: чередование курсов АБ (при отсутствии явного обострения их назначают в малых дозах) с растительными противовоспалительными диуретиками (зверобой, шалфей, ромашка, шиповник, брусника) в промежутках между этими курсами.
Примерная схема длительного (от 3 месяцев до нескольких лет) противорецидивного лечения ХП: в 1-ю неделю месяца питье уросептиков (клюквенный морс или отвар шиповника) ® во вторые две недели прием отвара лекарственных трав (существенно не влияющих на бактериурию, но улучшающих уродинамику): брусничный лист, ромашка, березовые почки, полевой хвощ, плоды можжевельника или сложные сборы "фитолизин", "урофлюкс" ® в последнюю неделю месяца прием АБ (меняется каждый месяц). Можно использовать и другую схему: 1-я неделя (бисептол по 2 таб. на ночь) ® 2-я неделя (уросептики) ® 3-я неделя (5-НОК) ® 4-я неделя (левомицетин по 1 таб. на ночь).
Важное место в противорецидивном лечении больных ХП вне обострения, с достаточной функцией почек и без выраженной АГ (АД не должно превышать 170/100 мм рт. ст.) отводят санаторно-курортному лечению: сухой, теплый климат Южного берега Крыма и питье минеральных вод (Трускавец, Железноводск, Карловы Вары).
ВТЭ. В период обострения ХП дается больничный лист на 15-20 дней, а при обострении средней тяжести ¾ на 30-35 дней (из них стационарное лечение ¾ 20-25 дней). В латентный период ХП или на компенсированной стадии заболевания больные практически трудоспособны, но им следует избегать профессий с высокой вероятностью простуд и ФН. При появлении ХПН трудоспособность больных ХП резко снижается, им определяют III группу инвалидности (она зависит от степени ХПН).
Хроническая почечная недостаточность ¾это клинический синдром, обусловленный необратимым, значительным и прогрессирующим повреждением почек (гибелью нефронов) со снижением их функции менее, чем 20% от нормы вследствие различных патологических состояний. При ХПН уменьшенное число нефронов использует все свои возможности для поддержания гомеостаза организма. ХПН необратима, прогрессирует, проходя три стадии: снижение почечного резерва ® почечная недостаточность (продукты метаболизма накапливаются в крови) ® терминальная стадия (почки не способны поддерживать гомеостаз).
Терминология ХПН:
· ХПН ¾ общий термин, описывающий необратимое падение скорости КФ в течение нескольких лет;
· азотемия ¾ повышение уровня мочевины и креатинина в крови;
· уремия ¾ фаза ХПН (независимо от ее этиологии), при которой появляются признаки выраженной почечной патологии (неврологическая симптоматика, сердечно-сосудистый, гематалогический и др. синдромы). Обычно при этом скорость КФ падает до 10 мл/мин;
· терминальная фаза ХПН ¾ снижается количество нефронов менее 10% от нормы. Таким больным показана постоянная заместительная терапия (гемодиализ) или пересадка почки.
При ХПН нарушаются основные гомеостатические функции почек по поддержанию постоянного объема жидкости, ионного состава и КЩС:
· развивается азотемия (из-за снижения КФ);
· нарушаются КЩС (метаболический ацидоз) и электролитный состав (снижение содержания кальция, но повышается ¾ фосфора и калия);
· формируются АГ и анемия;
· нарушается синтез и выделение вазоактивных веществ (ренина, простогландинов, ангиотензина).
Морфологический эквивалент ХПН ¾ нефросклероз (замещение нормальной почечной ткани рубцовой), который становится выраженным при повышении уровня креатинина в крови до 0,2 мМ/л (норма -- 0,08-0,1 мМ/л). Морфология ХПН однотипна: преобладают фибропластические процессы с замещением нефронов соединительной тканью. На оставшиеся нефроны ложится повышенная нагрузка, что приводит к их структурным изменениям. Это ¾ основной неиммунный механизм прогрессирования ХПН.
Почки обладают большими компенсаторными возможностями. Так, даже гибель 50% нефронов (или снижение КФ на 90%) может не проявляться клиникой ХПН. Только снижение числа нефронов до 30% (при этом КФ падает до 30 мл/мин; норма -- 120 мл/мин), приводит к задержке в организме больного мочевины, креатина и др. азотистых шлаков. Хотя на этой стадии ХПН может протекать все еще без симптоматики, но почечный резерв настолько снижается, что любой внезапный стресс (инфекция, обструкция мочевых путей, уменьшение приема жидкости) может вызвать дальнейшее снижение функции почек и появление явной уремии. Обычно у больного развивается явная ХПН при падении КФ менее 20% от нормы.
Причины развития ХПН:
· Ренальные:
Первое место занимает СД (вследствие диабетического нефроангиосклероза), обуславливающий 35% всех причин терминальной ХПН. У 1/3 больных СД (особенно 1-го типа) обычно через 10 лет развивается терминальная ХПН.
Второе место ¾ у ГБ(дает 30% всех терминальных ХПН) за счет нефросклероза почечных артерий. ХПН на фоне ГБ прогрессирует, как правило, медленно. Нередко при комбинации у больных ГБ и ХПН врачу трудно решить, что первично, а что вторично.
На третьем месте располагаются прогрессирующие формы ХГН (MN, MPGN, FSG), обуславливающие 15% всех терминальных ХПН.
На остальные причины приходится 20% всех терминальных ХПН. Так, из наследственных причин ХПН следует отметить врожденный поликистоз почек, а из системных заболеваний, поражающих почки, ¾ СКВ (люпус-нефрит), УПА, ССД (склеродермическая почка), гранулематоз Вегенера, синдром Гудпасчера и амилоидоз почек. Более редкие причины ХПН ¾ МКБ с ХПН, рефлюксные уропатии и нефропатии, обусловленные приемом лекарств.
· Преренальные: первичное поражение сосудов почек (двухсторонний стеноз почечных артерий);
· Постренальные: длительная обструкция мочевыводящих путей (врожденная, ДГПЖ, опухоли мочевой системы).
Медленно прогрессирующая ХПН чаще встречается при ХП, поликистозе почек, тогда как быстро прогрессирующая ¾ при сочетанных нарушениях (например, уродинамики на фоне СКВ).
Патогенез ХПН.Независимо от этиологии поражения почек, снижение их функции идет за счет трех механизмов: уменьшения количества функционирующих нефронов и скорости КФ в каждом из них (как результат, снижается суммарная КФ), их сочетание. Дополнительно формируется поражение интерстиция, окружающего нефрон. Снижение числа функционирующих нефронов до критического уровня приводит к изменению биохимических констант почек (например, уровня мочевины или креатинина в крови) и тяжелым нарушениям обмена (развивается уремия). Оставшиеся нефроны усиленно функционируют для компенсации гомеостаза. Позднее их функция нарушается (вследствие повышения тока плазмы и гидростатического давления), что проявляется фокальным гломерулосклерозом. Поэтому ХПН прогрессирует, даже если устраняется причина, ее вызвавшая (хирургическая коррекция рефлюкса или лечение АБ). В целом, на фоне ХПН развиваются тяжелые дистрофические процессы во всех внутренних органах.
Метаболические последствия ХПН могут быть разными:
· нарушается регуляция баланса натрия и воды. Так, почки могут плохо удалять натрий (особенно на фоне приема избыточного количества соли с пищей). Это приводит к задержке жидкости во внеклеточном пространстве, последующим отекам и АГ. В других случаях, наоборот, почки плохо удерживают натрий, что благоприятствует солевому истощению (появляются сухость, слабость и гипотония). Теряется также способность почек к образованию мочи с высоким и низким удельным весом;
· развивается гиперкалиемия из-за задержки ионов калия. В норме, до 95% поступаемого в организм калия выделяется почками. Несмотря на прогрессирование ХПН, у многих больных, вплоть до терминальной стадии, поддерживается близкий к нормальному уровень калия в крови. Обычно у больных ХПН гиперкалиемия (более 5,0 мМ/л) появляется при снижении КФ менее 15 мл/мин. Усиливать гиперкалиемию при ХПН могут: повышенный метаболизм (вследствие лихорадки, инфекции), избыточное поступление калия с пищей, прием калий-сберегающих мочегонных (верошпирон), ацидоз и олигоурия. При уровне калия менее 6 мМ/л клинических симптомов обычно нет. Но при превышения этого уровня появляются опасные для жизни аритмии сердца (главный поражаемый орган ¾ сердце). На ЭКГ при этом отмечается увеличение зубца Т и уширение комплекса QRS. При увеличении уровня калия в крови до 7,5 мМ/л, снижается соотношение вне- и внутриклеточного калия, клетки сердца полностью теряют способность к возбудимости (j покоя сравнивается с j действия мембран клеток). У больного развиваются: резкая брадикардия (особенно часто на фоне предшествующих поражений сердца), вплоть до асистолии (на ЭКГ в финале отмечают безволновую ЭКГ), и мышечные параличи;
· нарушается КЩС,формируется метаболический ацидоз из-за роста содержания ионов водорода в организме больного (вследствие снижения суточного образования буферов ниже уровня, необходимого для поддержания баланса ионов). Обычно выраженные нарушения КЩС возникают при падении КФ менее, чем 25% от нормы. Признак тяжелого ацидоза ¾ дыхание Кусмауля. Этот ацидоз частично компенсируется костной тканью. Это способствует появлению ее патологии (остеомаляция, остеосклероз), что на фоне нарушения метаболизма витамина Д благоприятствует последующим самопроизвольным переломам.
· изменяется минеральный обмен ¾развиваются гипокальциемия за счет плохой абсорбции и потерь кальция с калом (вследствие того, что витамин Д, необходимый для реабсорбции кальция, не может конвертироваться в активную форму) и гиперфосфатемия (из-за плохого выделения почками);
· снижается выработка эритропоэтинапочками, что приводит к анемии;
· активируются прессорные механизмыпочек, способствующие стабилизации АГ.
В генезе уремического синдрома важную роль играют уремические токсины, обуславливающие интоксикацию ("средние молекулы" ¾ осколки аминокислот, полипептиды, олигосахара, которые частично образуются из пищевых белков, метаболитов жизнедеятельности кишечных бактерий) и продукты извращенных обменных процессов в организме. Так, повышенное выделение паратгормона способствует остеодистрофии и полинейропатии. При уремии нарушено выведение "средних молекул", но они достаточно выводятся при гемодиализе (их уровень уменьшается более, чем на 25% от исходного). Мочевина и креатинин не являются токсическими продуктами.
Таблица27
Классификация ХПН (С.И. Рябов, 1976)
| Стадия | Фаза | Название | Лабораторные критерии | Форма | Группа | |
| Креатинин | КФ | |||||
| А Б | Латентная | Менее 0,18 мМ/л | более 50% от нормы | Обратимая | ||
| II | А Б | Азотемическая | 0,19-0,44 0,45-0,7 | 20-50% 10-20% | Стабильная Прогрессирующая | |
| III | А Б | Уремическая | 0,72-1,24 более 1,25 | Менее 10% Менее 5% | 2, 3 |
0 ¾ необходимо лечение основного заболевания; 1 ¾ назначение малобелковой диеты и консервативные методы терапии; 2 ¾ гемодиализ и пересадка почки; 3 ¾ показано проведение только симптоматической терапии.
На первой, латентной стадии ХПН (доазотемической) нет клинических проявлений (А ¾ нет нарушений фильтрации и реабсорбции, Б ¾ есть нарушения фильтрации и реабсорбции). Вторая стадия ХПН ¾ азотемическая (А ¾ клиники нет, но есть азотемия, Б ¾ имеются начальные клинические проявления). Третья стадия ¾ уремическая (А ¾ умеренных клинических проявлений, Б - выраженных клинических проявлений). Такие показатели, как уровни мочевины, остаточного азота, электролитов, КЩС, АД и анемия мало зависят от степени ХПН. Главное в оценке и диагностике ХПН ¾ выраженность гипостенурии и повышение креатинина в крови. Обычно при нарушении функции почек стойкое повышение уровня мочевины и креатинина наблюдается при снижении КФ менее 40% от нормы.
Клиника ХПН развертывается постепенно и часто оценивается ретроспективно. В ней выделяют следующие клинические синдромы ХПН:
· нарушения КЩС и электролитного обмена (это самый главный синдром). Так, фосфат кальция, откладываясь в мягких тканях (кожа, сердце, суставы, сухожилия, мышцы и сосуды), вызывает появление кожного зуда (часто мучительного), мышечной слабости и аритмий. Появляются изменения в скелете (почечная остеодистрофия) с симптоматикой: боли, тофусы ("уремическая подагра"), частые переломы костей вследствие остеомаляции;
· сердечно-сосудистыйпри котором формируется резкая АГ (из-за избыточной продукции ренина) с последующим развитием: ангиопатии сетчатки глаз, энцефалопатии, ГЛЖ, приступов ОЛЖН, вплоть до развития ОЛ или ХНК. Определяются напряженный пульс, усиленный верхушечный толчок; выслушиваются глухой I тон, акцент 2-го на аорте и сосудистые шумы. На фоне высокой АГ резко повышаются темпы развития атеросклероза (отчасти вследствие сопутствующей ХПН дислипидемии) и шансы развития ОИМ или инсульта. В ответ на накопление уремических токсинов в перикарде, нередко внезапно развивается сухой (чаще) или экссудативный перикардит (с тампонадой);
· поражение ЖКТ.Первымипоявляются диспепсические нарушения (тошнота, мучительная рвота, приводящая к дегидротации, анорексия, обложенный язык). Позднее присоединяются поражения (воспаление и кровоизлияния) слизистых ЖКТ, появляются признаки гастрита, энтерита, колита (с похуданием, поносами) и образование язв на всем протяжении ЖКТ, от рта до прямой кишки (например, язвы желудка отмечаются у 1/4 больных с уремией). Нарушается функция печени (гепатит) и поджелудочной железы;
· неврологический(уремическая энцефалопатия вследствие накопления уремических токсинов) с поражением ЦНС. Вначале появляется астения: слабость, повышенная утомляемость, потеря интереса к окружающему и памяти, нарастающая апатия, головные боли, извращение сна (днем сонливость, вечером бессонница), а позднее ¾ спутанность сознания и мышления, подергивание отдельных групп мышц, мышечный тремор, генерализованные судороги. Может развиться и периферическая полинейропатия (вследствие аккумуляции средних молекул в периферических нервах) с утратой сухожильных рефлексов, слабостью в ногах, вялой тетраплегией;
· дерматологический ¾сухиеибледно-желтоватые кожные покровы, одутловатость лица, расчесы вследствие кожного зуда, после испарения пота на коже остается тонкий слой белого порошка ("уремический иней");
· иммунных нарушенийс лимфоцитопений, нарушением функции лейкоцитов, атрофией лимфоидных структур и повышенной восприимчивостью к инфекции;
· гематологическийс развитием нормохромной анемии, иногда очень тяжелой (вследствие уменьшения выработки эритропоэтина почками), со снижением функциональных способностей тромбоцитов на фоне их нормального числа (за счет воздействия на костный мозг уремических токсинов и функционирования тромбоцитов в кислой плазме) и появлением аномального гемостаза. Все это способствует появлению геморрагического диатеза (подкожные гематомы) и даже геморрагий (носовых, маточных или в ЖКТ);
· мочевой ¾ появляются гипо-изостенурия, полиурия, в терминальной стадии ¾ олигурия; мочевой осадок скудный (немного эритроцитов в поле зрения, протеинурия);
· эндокринныйс формированием вторичного гипопаратиреоза, гиперлактинемии, изменением функции гипофиза и половых желез (импотенция, аменоррея, неспособность выносить беременность).
Таким образом, клинические проявления ХПН весьма вариабельны.
В латентной стадии(начинается при гибели 70% функционирующих нефронов) возможно появление: полиурии, никтурии (больной мочится 2-3 раза ночью), увеличения количества выпиваемой жидкости до 3 л/д и жажды (больной ставит на ночь около постели стакан воды). Отмечаются астения (слабость, снижение трудоспособности) и извращение сна. Кожа становится сухой, вялой и шелушащейся. На УЗИ выявляется уменьшение размеров почки, а на изотопной ренографии ¾ кривые становятся плоскими и вытянутыми.
Во второй стадии ХПН с явными нарушениями функции почек (погибло более 90% всех нефронов), появляются поражения многих органов (но без значительного нарушения их функции) с выраженной внепочечной клинической симптоматикой (уремическое легкое, резкая анемия, нарушения ЖКТ и др). Это главное отличие от первой стадии ХПН. Объективно определяются: сухая кожа, бледно-желтый цвет лица, "синяки" на руках и ногах. Появляется запах мочи изо рта, но не мочевины, которая не пахнет. Моча становится светлой, с низким удельным весом. У 80% больных формируется тяжелая АГ, отягощающаяся ОЛЖН, нарушениями ритма сердца, ретинопатией. Рентгенологически определяются остеопороз и остеомаляция.
В третьей, терминальной стадии ХПН (количество функционирующих нефронов менее 10% от нормы) возникает декомпенсация не только почек, но и других органов. Характерна следующая последовательность полиурия ® олигоурия ® анурия. У больных отмечаются: выраженная анемия, фибринозный перикардит (с шумом трения перикарда) или выпотной (с одышкой), уремический отек легких (на рентгенографии грудной клетки видны "облаковидные инфильтраты"), который не купируется в/в введением лазикса. Поверхность альвеол покрывается пленкой, что приводит к нарушениям газообмена и тяжелому ацидозу. Резко усиливается неврологическая симтоматика ¾ появляются судорожные подергивания, энцефалопатия, вплоть до уремической комы, тяжелая миопатия (больной не может стоять на ногах). Весьма часто наслаивается банальная инфекция (пневмония), что еще больше отягощает функционирование почек. Развиваются множественные эндокринные нарушения.
Диагностика ХПНнесложная и проводится по:
· увеличению уровня креатинина в крови;
· снижению размера почек по данным УЗИ или рентгенографии;
· плоским и рястянутым кривым на изотопной ренографии.
Течение и прогноз ХПН.Она может нарастать медленно, годами, с длительными ремиссиями, во время которых больной трудоспособен. Иногда под действием ряда факторов (алкогольная интоксикация, тяжелая инфекция, беременность), ХПН приводит к быстрой, за 3-5 дней гибели больного (это более характерно для ХП). Для прослеживания за темпами прогрессирования ХПН оценивают в динамике (годами) обратную величину уровня креатинина в крови (1/КК), учитывая, что скорость КФ=1/КК.
Лечение ХПН.
Назначается диета (стол №7), при которой суточное выделение мочевины определяет потребление белка (при расщеплении 100 г белка образуется 30 г… Малобелковая диета замедляет прогрессирование ХПН, тогда как, наоборот,… В начальной стадии ХПН больному дают до 10 г/д соли. Ее ограничивают при наличии АГ и НС. Проводится и коррекция…СПИСОК СОКРАЩЕНИЙ
ОГЛАВЛЕНИЕ
стр.
Хроническая недостаточность кровообращения ..................................................................... 3
Инфекционный эндокардит ..................................................................................................... 42
Сепсис в клинике внутренних болезней ................................................................................ 74
Лихорадка неясного генеза .................................................................................................... 103
Аритмии сердца ....................................................................................................................... 127
Заболевания кишечника ......................................................................................................... 166
Гломерулонефриты ................................................................................................................. 196
Хронический пиелонефрит и хроническая
почечная недостаточность ...................................................................................................... 231
Список сокращений ................................................................................................................ 259
– Конец работы –
Используемые теги: Избранные, Лекции, внутренним, болезням0.081
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: ИЗБРАННЫЕ ЛЕКЦИИ ПО ВНУТРЕННИМ БОЛЕЗНЯМ
Что будем делать с полученным материалом:
Если этот материал оказался полезным для Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов